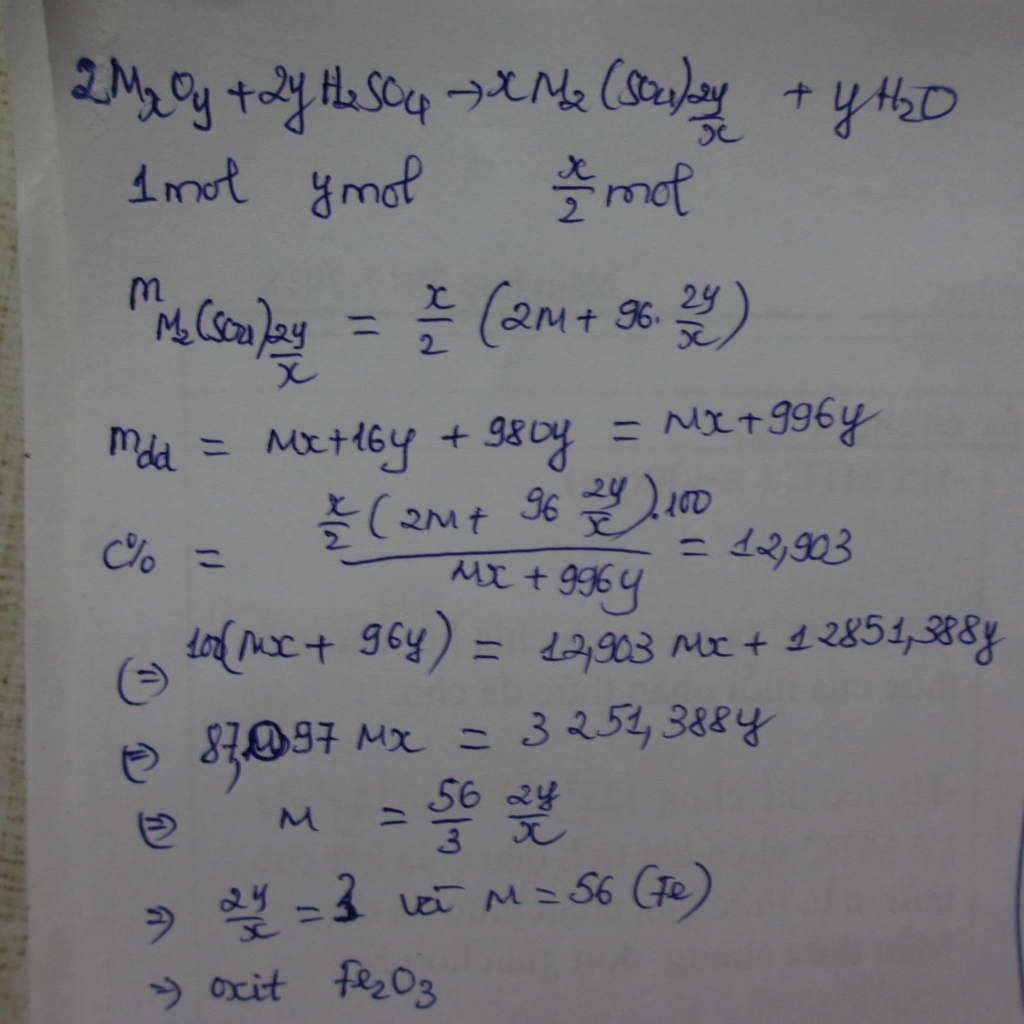Những câu hỏi liên quan
1) khi hòa tan 21g kim loại(II) trong dd H2SO4 loãng dư thu được 8,4l H2(đktc) và dd A. Cho kết tinh muối trong dd A thu được 104,25g tinh thể hidrat hóa
a) Cho biết tên kim loại
b) CTPT của tinh thể
2)Để hòa tan 8g oxit kim loại R(III) cần 300ml đ HCl 1M. xác định tên oxit kim loại( biết R2O3+HCl--RCl2+H2O)
3)Công thức tổng quát của oxit kim loại Rlà RxOy. Nếu tỉ lệ khối lượng của R so với oxit là 7:3 thì công thức phân tử của oxitkim loại trên là gì?
Đọc tiếp
1) khi hòa tan 21g kim loại(II) trong dd H2SO4 loãng dư thu được 8,4l H2(đktc) và dd A. Cho kết tinh muối trong dd A thu được 104,25g tinh thể hidrat hóa
a) Cho biết tên kim loại
b) CTPT của tinh thể
2)Để hòa tan 8g oxit kim loại R(III) cần 300ml đ HCl 1M. xác định tên oxit kim loại( biết R2O3+HCl-->RCl2+H2O)
3)Công thức tổng quát của oxit kim loại Rlà RxOy. Nếu tỉ lệ khối lượng của R so với oxit là 7:3 thì công thức phân tử của oxitkim loại trên là gì?
Xem thêm câu trả lời
Khi hòa tan 21g kim loại hóa trịII vào trong dung dịch H2SO4 loãng thu được 8,4 l H2 và dung dịch A khi cho hết tinh muối trong dung dịch A thì thu được 104,25 g tinh thể hidrat
cho biết tên kim loại
xác định công thức của tinh thể muối hidrat hóa
nH2= nR= 0.375
--> M<R>= 21/0.375=56: Fe
nFeSO4.nH2O=nFe=0.375
--> 152*0.375+18n*0.375=104,25
-->n=7
--> FeSO4.7H2OnH2= nR= 0.375
--> M<R>= 21/0.375=56: Fe
nFeSO4.nH2O=nFe=0.375
--> 152*0.375+18n*0.375=104,25
-->n=7
--> FeSO4.7H2O
Đúng 0
Bình luận (0)
b2 . Cho 11,1g hh kim loại hoá trị II, oxit và muối sunfit của kim loại đó tan vào dd H2SO4 loãng vừa đủ thì thu đc dung dịch A và thoát ra 3,36l khí (đktc). Cho Ba(OH)2 dư vào dd A thì đc kết tủa B, nung B ở nhiệt độ cao thì còn lại 71,6625g chất rắn. Mặt khác, cho 14,8g hh vào 0,4l dd CuSO4 1M. Sau pư lọc bỏ chất rắn, rồi cô cạn dung dịch thì thu đc 62g chất răna) Tìm kim loạib) Tìm m mỗi chất trong hh đầu
Đọc tiếp
b2 . Cho 11,1g hh kim loại hoá trị II, oxit và muối sunfit của kim loại đó tan vào dd H2SO4 loãng vừa đủ thì thu đc dung dịch A và thoát ra 3,36l khí (đktc). Cho Ba(OH)2 dư vào dd A thì đc kết tủa B, nung B ở nhiệt độ cao thì còn lại 71,6625g chất rắn. Mặt khác, cho 14,8g hh vào 0,4l dd CuSO4 1M. Sau pư lọc bỏ chất rắn, rồi cô cạn dung dịch thì thu đc 62g chất răn
a) Tìm kim loại
b) Tìm m mỗi chất trong hh đầu
khi hòa tan 21 g một kim loại hóa trị 2 trong dung dịch h2so4 dư người ta thu dc 8.4 l khí h2 và dung dịch A. khi cho kết tinh muối trong dung dịch A thì dc 104.25 g tinh thể hidrat hóa
a. cho bt tên kim loại
b xác định CTHH của tinh thể muối hidrat đó
Gọi kim loại hóa trị 2 là A
nH2 = 8.4/22.4=0.375mol
A + H2SO4 -> ASO4 + H2
(mol) 0.375 0.375 0.375 0.375
mH2 = 0.375*2=0.75g
mH2SO4 = 0.375*98=36.75g
Áp dụng định luật bảo toàn khối lượng
mA + mH2SO4 = mASO4 + H2
=> mASO4 = 21 + 36.75 - 0.75 = 57g
MASO4 = m/n = 57/0.375=152
A + 96 =152
-> A = 56 (Fe)
b) gọi CTHH của tinh thể là FeSO4.nH2O
nFeSO4.nH2O = nFeSO4 = 0.375mol
MFeSO4.nH2O = m/n= 104.25/0.375=278
MFeSO4.nH2O = 278
152+ 18n = 278
18n= 126
n= 7
Vậy. CTHH của tinh thể muối hidrat là FeSO4.7H2O
Đúng 0
Bình luận (0)
Hoà tan một lượng muối cacbonat của kim loại hoá trị III bằng dung dịch H2SO4 nồng
độ 16%. Sau khi khí không thoát ra nữa, thu được dung dịch chứa 20% muối sunfat tan. Xác
định kim loại đó.
GIÚP MÌNH VỚI Ạ!!!!!!!!!!!!!!!!!!!!!!!!!!
\(Đặt.muối:A_2\left(CO_3\right)_3\\ n_{A_2\left(CO_3\right)_3}=a\left(mol\right)\Rightarrow n_{H_2SO_4}=3a\left(mol\right)\\ m_{ddH_2SO_4}=\dfrac{3a.98.100}{16}=1837,5a\left(g\right)\\ A_2\left(CO_3\right)_3+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3CO_2+3H_2O\\ m_{ddsau}=\left(M_A.2+180\right).a+1837,5a-44a.3=1885,5a+2M_A.a\left(g\right)\\ Vì:C\%_{dd.muối.sunfat}=16\%\\ \Leftrightarrow\dfrac{\left(2M_A+288\right).a}{\left(1885,5+2M_A\right).a}.100\%=16\%\\ \Leftrightarrow M_A=8,14\left(loại\right)\)
Không có kim loại thỏa
Đúng 0
Bình luận (0)
Hoà tan 3,2g Oxit kim loại hoá trị III bằng 200g dung dịch H2SO4 loãng. Khi thêm vào hoà tan 1 oxit kim loai htri IV biết rằng hoà tan 8g oxit này bằng 300ml dd H2SO4 1M. sau p/ứ trung hoà lượng axit còn dư bằng 50g dd NaOH 24%. tìm cthỗn hợp sau phản ứng 1 lượng CaCO3 vừa đủ thấy 0,0224dm3 CO2 ở đktc sau đó cô cạn dung dịch thu được 9,36g muối sunfat khô. Tìn công thức õit kim loại và C% H2SO4
Dùng 500 ml dung dịch H2SO4 1,2 m để hoà tan hết lượng kim loại sắt. Phản ứng tạo thành sắt (II) sunfat và khí hiđro: a) Viết phương trình hoá học của phản ứng? b) Tính khối lượng muối sắt (II) sunfat thu được? c) Tính thể tích khí H2 thoát ra (Ở ĐKTC)? d) Dẫn toàn bộ khí H2 thu được ở trên qua bột CuO đun nóng. Tính khối lượng điều chế được?
Đọc tiếp
Dùng 500 ml dung dịch H2SO4 1,2 m để hoà tan hết lượng kim loại sắt. Phản ứng tạo thành sắt (II) sunfat và khí hiđro: a) Viết phương trình hoá học của phản ứng? b) Tính khối lượng muối sắt (II) sunfat thu được? c) Tính thể tích khí H2 thoát ra (Ở ĐKTC)? d) Dẫn toàn bộ khí H2 thu được ở trên qua bột CuO đun nóng. Tính khối lượng điều chế được?
a) PTHH : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
b) \(n_{H_2SO_4}=C_MV=1,2\cdot0,5=0,6\left(mol\right)\)
PTHH : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,6 0,6 0,6
\(\Rightarrow m_{FeSO_4}=n_{FeSO_4}M_{FeSO_4}=0,6\cdot152=91,2\left(g\right)\)
c) Từ câu b \(\Rightarrow n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow V_{H_2}=n_{H_2}.22,4=0,6\cdot22,4=13,44\left(l\right)\)
d) PTHH : \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,6 0,6
\(\Rightarrow m_{Cu}=n_{Cu}M_{Cu}=0,6\cdot64=38,4\left(g\right)\)
Đúng 2
Bình luận (0)
a)\(PTHH:Fe+H_2SO_4\xrightarrow[]{}FeSO_4+H_2\)
b)Đổi 500ml = 0,5l
Số mol của H2SO4 là:
\(C_{MH_2SO_4}=\dfrac{n_{H_2SO_4}}{V_{H_2SO_{\text{4 }}}}\Rightarrow n_{H_2SO_4}=C_{MH_2SO_4}.V_{H_2SO_4}=1,2.0,5=0,6\left(mol\right)\)
\(PTHH:Fe+H_2SO_4\xrightarrow[]{}FeSO_4+H_2\)
Tỉ lệ : 1 1 1 1 (mol)
Số mol : 0,6 0,6 0,6 0,6(mol)
Khối lượng sắt(II)sunfat thu được là:
\(m_{FeSO_4}=n_{FeSO_4}.M_{FeSO_{\text{4 }}}=0,6.152=91,2\left(g\right)\)
c) Thể tích khí H2 thoát ra là:
\(V_{H_2}=n_{H_2}.22,4=0,6.22,4=13,44\left(l\right)\)
d)\(PTHH:CuO+H_2\xrightarrow[]{t^0}Cu+H_2O\)
tỉ lệ :1 1 1 1 (mol)
số mol :0,6 0,6 0,6 0,6 (mol)
Khối lượng CuO điều chế được là:
\(m_{CuO}=n_{CuO}.M_{CuO}=0,6.80=48\left(g\right)\)
Đúng 1
Bình luận (2)
Cho m gam hỗn hợp X chứa tan hoàn toàn trong dung dịch chứa 1,025 mol
H
2
S
O
4
Sau phản ứng thu được 5,04 lít (đktc) hỗn hợp khí Y gồm hai khí trong đó có một khí hoá nâu trong không khí và dung dịch Z chỉ chứa các muối sunfat trung hoà (không chứa muối
F
e
3
+
). Biết tỉ khối của Y so với
H
2
là 31/3. Cho
B...
Đọc tiếp
Cho m gam hỗn hợp X chứa ![]() tan hoàn toàn trong dung dịch chứa 1,025 mol
H
2
S
O
4
Sau phản ứng thu được 5,04 lít (đktc) hỗn hợp khí Y gồm hai khí trong đó có một khí hoá nâu trong không khí và dung dịch Z chỉ chứa các muối sunfat trung hoà (không chứa muối
F
e
3
+
). Biết tỉ khối của Y so với
H
2
là 31/3. Cho
B
a
C
l
2
vào dung dịch Z vừa đủ để kết tủa hết ion sunfat, sau khi các phản ứng xảy ra xong cho tiếp
A
g
N
O
3
dư vào thì thu được x gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của tổng x + m là
tan hoàn toàn trong dung dịch chứa 1,025 mol
H
2
S
O
4
Sau phản ứng thu được 5,04 lít (đktc) hỗn hợp khí Y gồm hai khí trong đó có một khí hoá nâu trong không khí và dung dịch Z chỉ chứa các muối sunfat trung hoà (không chứa muối
F
e
3
+
). Biết tỉ khối của Y so với
H
2
là 31/3. Cho
B
a
C
l
2
vào dung dịch Z vừa đủ để kết tủa hết ion sunfat, sau khi các phản ứng xảy ra xong cho tiếp
A
g
N
O
3
dư vào thì thu được x gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của tổng x + m là
A. 389,175
B. 585,000
C. 406,800
D. 628,200
Đáp án D
![]()
chứa H 2 và NO với số mol
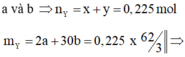
Giải hệ có: a = 0,75 mol; b = 0,15 mol
![]()
![]()
Bảo toàn nguyên tố Nitơ:![]()
Bảo toàn nguyên tố Fe:
![]()
Bảo toàn điện tích + nguyên tố Al:
![]()
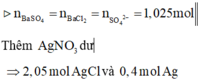
=> x = 567,2 (g) => x+ m = 52 + 567,2 = 628,2 (g)
Đúng 0
Bình luận (0)
Bài 1 Hòa tan 3,2 gam oxit M2Om trong một lượng vừa đủ dd H2SO4 10% thu được dd muối Sunfat 12,9%. Cô cạn dd muối rồi l làm lạnh dd thấy thoát ra 7,868 gam tinh muối sunfat với hiệu suất muối kết tinh là 70%. Hãy xác định công thức của tinh thể ngậm nước