Câu 1. Dùng 100 tấn quặng pirit sắt chứa 72% FeS2 để điều chế H2SO4. Cho toàn bộ axit thu được tác dụng vs Cu điều chế CuSO4.5H2O sau đó pha thành dd CuSO4 để trừ nấm thực vật. Tính m (tấn) CuSO4.5H2O thu được. biết hiệu suất cả quá trình là 80%.
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch H 2 S O 4 98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% F e S 2 (hiệu suất toàn quá trình là 80%) là
A. 0,80 tấn
B. 1,60 tấn
C. 1,25 tấn
D. 2,00 tấn
Trong công nghiệp, axit sunfuric được điều chế từ quang pirit sắt. Khối lượng H2SO4 điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% FeS2 ( hiệu suất toàn quá trình là 80%) là:
A. 1,568 tấn
B. 1,96 tấn
C. 1,25 tấn
D. 2,00 tấn
Đáp án A.
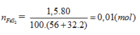
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
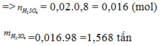
trong công nghiệp người ta điều chế H2SO4 từ quặng pirit sắt có thành phần chính là FeS2 theo sơ đồ sau FeS2->SO2->SO3->H2SO4.tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2 .Biết hiệu của cả quá trình là 80%
\(m_{FeS_2}=\dfrac{1.60}{100}=0,6\left(tấn\right)\)
=> \(m_{FeS_2\left(pư\right)}=\dfrac{0,6.80}{100}=0,48\left(tấn\right)\)
Cứ 1 mol FeS2 điều chế được 2 mol H2SO4
=> 120g FeS2 điều chế được 196g H2SO4
=> 0,48 tấn FeS2 điều chế được 0,784 tấn H2SO4
=> \(m_{ddH_2SO_4}=\dfrac{0,784.100}{98}=0,8\left(tấn\right)\)
\(m_{FeS_2}=0.6\left(tấn\right)=0.6\cdot10^3\left(kg\right)\)
\(n_{FeS_2}=\dfrac{0.6\cdot10^3}{120}=\dfrac{10^3}{200}\left(kmol\right)\)
Dựa vào sơ đồ phản ứng :
\(n_{H_2SO_4}=2n_{FeS_2}=2\cdot\dfrac{10^3}{200}=\dfrac{10^3}{100}=10\left(kmol\right)\)
\(m_{H_2SO_4\left(tt\right)}=10\cdot\dfrac{98}{80\%}=1225\left(kg\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{1225}{98\%}=1250\left(kg\right)=12.5\left(tấn\right)\)
Tính khối lượng quặng pirit sắt (chứa 80% FeS2) cần dùng để điều chế 9,8 tấn H2SO4. Biết hiệu suất của cả quá trình là 75%.
tính khối lượng sắt pirit (FeS2) cần dùng để điều chế 49 tấn dd h2so4 98% biết hiệu suất toàn quấ trình là 78%
4FeS2 + 11O2 --to--> 2Fe2O3 + 8SO2
SO2 + O2 --to--> SO3
SO3 + H2O --> H2SO4
Theo phương trình, cứ 1 mol FeS2 thì tạo ra 2 mol H2SO4
=> cứ 0,245 mol FeS2 thì tạo ra 0,49 mol H2SO4
=> cứ 29,4g FeS2 thì tạo ra 48,02g H2SO4
=> cứ 29,4g FeS2 thì tạo ra 49g dd H2SO4 98%
=> cứ 29,4 tấn FeS2 thì tạo ra 49 tấn dd H2SO4 98%
Do hiệu suất của quá trình là 78%
=> mFeS2 (thực tế) = \(\dfrac{29,4.100}{78}=37,692\left(tấn\right)\)
từ 2,4 tấn quặng pirit sắt chứa 60% fes2.Điều chế được bao nhiêu lít dd h2so4 70%.(Ddd=1,8g/ml),biết H đạt 80%
Đổi 2,4 tấn = 2400 kg
Ta có: \(n_{FeS_2}=\dfrac{2400\cdot60\%}{120}=12\left(kmol\right)\)
Bảo toàn nguyên tố: \(n_{H_2SO_4\left(lý.thuyết\right)}=2n_{FeS_2}=24\left(kmol\right)\)
\(\Rightarrow n_{H_2SO_4\left(thực\right)}=24\cdot80\%=19,2\left(kmol\right)\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{19,2\cdot98}{70\%}=2688\left(kg\right)\)
\(\Rightarrow V_{H_2SO_4}=\dfrac{2688}{1,8}\approx1493,3\left(l\right)\)
Từ một tấn quặng pirit sắt chứa 20% tạp chất, điều chế H2SO4 theo phương pháp tiếp xúc theo các giai đoạn sau:
FeS2 --90%--> SO2 --64%--> SO3 --80%--> H2SO4
Tính khối lượng dd H2SO4 72% điều chế được?
mFeS2 = 1.\(\dfrac{80}{100}\) = 0,8 tấn
nFeS2 = \(\dfrac{0,8}{120}\) = \(\dfrac{1}{150}\) mol/ tấn
2FeS2 + \(\dfrac{11}{2}\)O2 \(^{to}\rightarrow\) Fe2O3 + 4SO2 \(\uparrow\)
\(\dfrac{1}{150}\)-------------------------->\(\dfrac{1}{75}\)
- do H = 90% => nSO2(thực tế) = \(\dfrac{1}{75}.\dfrac{90}{100}\) = 0,012mol/tấn
2SO2 + O2 \(^{to}\rightarrow\) 2SO3
0,012------------>0,012
- do H = 64 % => nSO3(thực tế) = 0,012. \(\dfrac{64}{100}\) = 0,00768 mol/ tấn
SO3 + H2O -> H2SO4
0,00768------->0,00768
- do H = 80 % => nH2SO4 = 0,00768 . 80% = 0,006144 mol/tấn
=> mH2SO4 = 0,006144 . 98 = 0,602112 tấn = 602,112 kg
=>mH2SO4(72%) = 602,112 . 72% = 433,52064 kg
viết phương trình hoác học điều chế axit sunfuric từ quặng pirit sắt .từ 10 tấn quặng pirit sắt (chứa 98,2S2) có thể điều chế được bao nhiêu tấn H2SO4 98%. cho biết hiệu suất của toàn bộ quá trình điều chế là 75%
Từ một tấn quặng pirit sắt chứa 20% tạp chất, điều chế H2SO4 theo phương pháp tiếp xúc theo các giai đoạn sau:
FeS2 --90%--> SO2 --64%--> SO3 --80%--> H2SO4
Tính khối lượng dd H2SO4 72% điều chế được?
m(FeS2)=(100%-20%).1=0,8(tấn)
4 FeS2 + 11 O2 -to,xt-> 2 Fe2O3 + 8 SO2
\(mSO2\left(LT\right)=\dfrac{0,8.512}{480}=\dfrac{64}{75}\left(tấn\right)\\ \rightarrow mSO2\left(TT\right)=\dfrac{64}{75}.90\%=\dfrac{96}{125}\left(tấn\right)\)
SO2 + 1/2 O2 \(⇌\) SO3
\(mSO3\left(LT\right)=\dfrac{\dfrac{96}{125}.80}{64}=\dfrac{24}{25}\left(tấn\right)\\ mSO3\left(TT\right)=\dfrac{24}{25}.64\%=\dfrac{384}{625}\left(tấn\right)\)
SO3+ H2O -> H2SO4
\(mH2SO4\left(LT\right)=\dfrac{\dfrac{384}{625}.98}{80}=\dfrac{2352}{3125}\left(tấn\right)\\ mH2SO4\left(TT\right)=\dfrac{2352}{3125}.80\%=\dfrac{9408}{15625}\left(tấn\right)\)
=> \(mddH2SO4\left(72\%\right)=\dfrac{\dfrac{9408}{15625}.100}{72}=0,836\left(tấn\right)\)
m(FeS2)=(100%-20%).1=0,8(tấn)
4 FeS2 + 11 O2 -to,xt-> 2 Fe2O3 + 8 SO2
mSO3(LT)=96125.8064=2425(tấn)mSO3(TT)=2425.64%=384625(tấn)���3(��)=96125.8064=2425(�ấ�)���3(��)=2425.64%=384625(�ấ�)
SO3+ H2O -> H2SO4
mddH2SO4(72%)=940815625.10072=0,836(tấn)