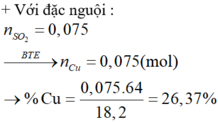Cho m (g) hỗn hợp X gồm Fe và S tác dụng hết vs dung dịch HCl thu được 5,6 (l) H2 ở điều kiện tiêu chuẩn. Cũng cho m (g) hỗn hợp trên tác dụng vs NaOH (dư) thì sau phản ứng còn 5,6 (g) chất rắn. Tính % khối lượng các kim loại trong hỗn hợp X

Những câu hỏi liên quan
Cho 2,96 g hỗn hợp gồm Cu Fe tác dụng với 500 ml dung dịch HCl sau phản ứng thu được 672 ml khí điều kiện tiêu chuẩn tính V Clo sau phản ứng vừa hết 2,96 g hỗn hợp trên
nH2 = 0,672/22,4 = 0,03 (mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
nFe = 0,03 (mol)
mFe = 0,03 . 56 = 1,68 (g)
mCu = 2,96 - 1,68 = 1,28 (g)
nCu = 1,28/64 = 0,02 (mol)
PTHH:
2Fe + 3Cl2 -> (t°) 2FeCl3
0,03 ---> 0,045
Cu + Cl2 -> (t°) CuCl2
0,02 ---> 0,02
nCl2 = 0,045 + 0,02 = 0,065 (mol)
VCl2 = 0,065 . 22,4 = 1,456 (l)
Đúng 3
Bình luận (0)
Cho 5,92 g hỗn hợp gồm Fe và Fe2O3 vào 500 ml dung dịch HCl xM sau phản ứng thu được 448 ml khí điều kiện tiêu chuẩn a) Tính x b) nếu cho 5,92 gam hỗn hợp trên tác dụng với khí Cl2 dư Tính khối lượng Cl2 phản ứng
Fe+2HCl->FeCl2+H2
0,02-0,04--------------0,02
Fe2O3+6HCl->2Fecl3+3H2O
0,03-----0,18 mol
n H2=\(\dfrac{0,448}{22,4}\)=0,02 mol
=>m Fe=0,02.56=1,12g
=>m Fe2O3=4,8g=>n Fe2O3=\(\dfrac{4,8}{160}\)=0,03 mol
=>x=CMHCl=\(\dfrac{0,22}{0,5}\)=0,44M
b)
2Fe+3Cl2-to>2FeCl3
0,02---0,03
=>m Cl2=0,03.71=2,13g
Đúng 3
Bình luận (0)
Cho 14,4g hỗn hợp gồm Mg,Fe , Cu tác dụng vs dd H2SO4 đặc nguội . Sau phản ứng thu 4,48lit SO2, dung dịch X và 5,6 g chất rắn ko tan % theo khối lượng của Cu?
Fe không tác dụng với H2SO4 đặc nguội
=> mFe = 5,6 (g)
Gọi số mol Mg, Cu là a, b (mol)
=> 24a + 64b = 14,4 - 5,6 = 8,8 (1)
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Mg + 2H2SO4 --> MgSO4 + SO2 + H2O
a---------------------------->a
Cu + H2SO4 --> CuSO4 + SO2 + H2O
b--------------------------->b
=> a + b = 0,2 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{14,4}.100\%=38,89\%\\\%m_{Mg}=\dfrac{0,1.24}{14,4}.100\%=16,67\%\\\%m_{Cu}=\dfrac{0,1.64}{14,4}.100\%=44,44\%\end{matrix}\right.\)
Đúng 5
Bình luận (0)
Hỗn hợp X gồm 5,6 gam Fe, 16 gam
Fe
2
O
3
và m gam Al. Nung X ở nhiệt độ cao trong điều kiện không có không khí, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một tác dụng với dung dịch
H
2
SO
4
loãng (dư), thu được 3a mol khí
H
2
. Phần hai phản ứng với dung dịch NaOH dư, thu...
Đọc tiếp
Hỗn hợp X gồm 5,6 gam Fe, 16 gam Fe 2 O 3 và m gam Al. Nung X ở nhiệt độ cao trong điều kiện không có không khí, thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau. Phần một tác dụng với dung dịch H 2 SO 4 loãng (dư), thu được 3a mol khí H 2 . Phần hai phản ứng với dung dịch NaOH dư, thu được a mol khí H2. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A. 5,40
B. 7,02
C. 8,1
D. 10,2
Cho 6,4 g hỗn hợp X gồm Mg,Al phản ứng với dung dịch axit sunfuric loãng dư thu được 7,28 lít khí ở điều kiện tiêu chuẩn a) Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp.b) nếu cho 12,9 g hỗn hợp X trên tác dụng với dung dịch axit sunfuric đặc nóng dư thì thu được bao nhiêu lít khí SO2 là sản phẩm khử duy nhất (đktc)
Sửa đề: 6,4 gam hh \(\rightarrow\) 6,45 gam hh
a) Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow24a+27b=6,45\) (1)
Ta có: \(n_{H_2}=\dfrac{7,28}{22,4}=0,325\left(mol\right)\)
Bảo toàn electron: \(2a+3b=0,65\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=n_{Mg}=0,1\left(mol\right)\\b=n_{Al}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1\cdot24}{6,4}\cdot100\%=37,5\%\\\%m_{Mg}=62,5\%\end{matrix}\right.\)
b) Ta thấy với 6,45 gam hh thì có 0,1 mol Mg và 0,15 mol Al
\(\Rightarrow\) Trong 12,9 gam hh thì chứa 0,2 mol Mg và 0,3 mol Al
Gọi \(n_{SO_2}=x\left(mol\right)\)
Bảo toàn electron: \(2\cdot0,2+3\cdot0,3=2x\) \(\Rightarrow x=n_{SO_2}=0,65\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,65\cdot22,4=14,56\left(l\right)\)
Đúng 2
Bình luận (0)
gọi số mol của Mg là x mol ; Al là y mol => 24x + 27y =6,4
n khí = 7,28/22,4=0,325 mol
bảo toàn e ta có
Mg + H2SO4 --> MgSO4 + H2
x x mol
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
y 3/2 y mol
=> x + 3/2y=0,325
=> x=11/120 mol ; y=7/45 mol
=> mMg11/120*24=2,2g => %mMg = 2,2*100/6,4=34,375%
=>%mAl=100-34,375=65,625%
Đúng 0
Bình luận (2)
a) Nung hỗn hợp gồm Fe và S trong bình kín không chứa không khí đến khi phản ứng hoàn
toàn thu được hỗn hợp rắn X . Cho toàn bộ X tác dụng với dung dịch HCl dư thu được 3,36 lit hỗn
hợp khí ở điều kiện tiêu chuẩn. Hỗn hợp khí này có tỷ khối so với hiđro là 19/3. Tính thành phần
% theo khối lượng của S trong hỗn hợp ban đầu
Tiến hành phản ứng nhiệt 13,4 g hỗn hợp A(gồm Al và Fe2O3).Sau khi làm nguội hòa tan hỗn hợp thu được bằng dung dịch HCl, dư thấy bay ra 5,6 l khí ở điều kiện tiêu chuẩn. Tính khối lượng Al và Fe2O3 trong hỗn hợp a
\(2Al+Fe_2O_3\xrightarrow[t^0]{}Al_2O_3+2Fe\)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow n_{H_2}=n_{Fe}=n_{Al}=0,25mol\)(ktm đề)
⇒Al phải dư, Fe2O3 hết
\(n_{Al}=a;n_{Fe_2O_3}=b\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(2Al+Fe_2O_3\rightarrow Al_2O_3+2Fe\)
\(\Rightarrow\left\{{}\begin{matrix}27a+160b=13,4\\3a+4b=6b+0,25.2\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}27a+160b=13,4\\3a-2b=0,5\end{matrix}\right.\\ \Rightarrow a=0,2;b=0,05\)
\(m_{Al}=0,2.27=5,4g\\ m_{Fe_2O_3}=13,4-5,4=8g\)
Đúng 0
Bình luận (0)
Cho 12,8 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 l loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, Chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37% B. 42,86% và 48,21% C. 48,21% và 42,56% D. 48,21% và 9,23%
Đọc tiếp
Cho 12,8 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 l loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, Chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%
B. 42,86% và 48,21%
C. 48,21% và 42,56%
D. 48,21% và 9,23%
Cho 8,3g hỗn hợp kim loại Fe và Al tác dụng với dung dịch HCL dư thu được dung dịch X và 5,6 lít H2(đktc) Cho dung dịch X tác dụng với lượng dư NaOH thu được m gam kết tủa.Nung kết tủa trong không khí đến khối lượng không đổi thu được a gam chất rắn.Viết PTPƯ và tính m,a
Các PTHH :
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(4Fe\left(OH\right)_2+O_2\xrightarrow[]{t^o}2Fe_2O_3+4H_2O\)
\(2Al\left(OH\right)_3\xrightarrow[]{t^o}Al_2O_3+3H_2O\)
Kết tủa thu được gồm Fe(OH)2 và Al(OH)3
Đặt : \(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(\Rightarrow56a+27b=8,3g\left(1\right)\)
\(Bte:2n_{Fe}+3n_{Al}=2n_{H2}=2a+3b=2.\dfrac{5,6}{22,4}=\left(2\right)\)
Từ(1),(2) \(\Rightarrow\left\{{}\begin{matrix}a=0,1=n_{Fe\left(OH\right)2}\\b=0,1=n_{Al\left(OH\right)3}\end{matrix}\right.\)
\(\Rightarrow m_{kết.tủa}=m_{Fe\left(OH\right)2}+m_{Al\left(OH\right)3}=0,1.90+0,1.78=16,8\left(g\right)\)
\(Bt\left(Al\right):n_{Al}=n_{Al2O3}=0,1\left(mol\right)\)
\(Bt\left(Fe\right):n_{Fe}=n_{Fe2O3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Chất.rắn}=0,1.160+0,1.102=26,2\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (1)
Đầu tiên, chúng ta sẽ viết các phương trình phản ứng cho mỗi bước của quá trình.
Bước 1: Phản ứng giữa hỗn hợp Fe và Al với dung dịch HCl: HCl (dung dịch) + Fe (kim loại) → FeCl2 (dung dịch) + H2 (khí)
2HCl + Fe → FeCl2 + H2
Bước 2: Phản ứng giữi dung dịch X với NaOH tạo kết tủa: X (dung dịch) + 2NaOH → 2NaX (dung dịch) + H2O (lỏng) + Al(OH)3 (kết tủa)
Bước 3: Nung kết tủa Al(OH)3 trong không khí: 2Al(OH)3 → Al2O3 + 3H2O
Bây giờ, chúng ta sẽ tính toán m và a.
Bước 1: Tính lượng H2 thoát ra.
Trước hết, chúng ta cần biết lượng mol của Fe trong hỗn hợp. Công thức của FeCl2 là Fe2+ (một cation sẽ tạo ra 1 mol H2 khi phản ứng với HCl). Vì vậy, số mol của Fe là bằng số mol H2.
Khối lượng mol của H2 là 2 g/mol, vì vậy số mol H2:
n(H2) = 5.6 l / 22.4 l/mol (ở điều kiện tiêu chuẩn) = 0.25 mol
Do đó, số mol Fe = 0.25 mol.
Khối lượng mol của Fe là 55.85 g/mol, vậy khối lượng của Fe là:
m(Fe) = 0.25 mol × 55.85 g/mol = 13.96 g
Bước 2: Tính lượng kết tủa Al(OH)3.
Al(OH)3 có khối lượng mol là 78 g/mol, và theo phương trình phản ứng ta thấy rằng mỗi mol Al(OH)3 tạo ra một mol kết tủa. Vì vậy, số mol Al(OH)3 tạo ra là bằng số mol NaOH đã sử dụng.
Số mol NaOH đã sử dụng được tính theo số mol H2O được tạo ra khi NaOH phản ứng. Một mol NaOH phản ứng với một mol H2O.
n(Al(OH)3) = n(NaOH) = n(H2O) = 0.25 mol
Khối lượng của Al(OH)3:
m(Al(OH)3) = 0.25 mol × 78 g/mol = 19.5 g
Bước 3: Nung kết tủa Al2O3 trong không khí.
Khối lượng của Al2O3 không thay đổi sau quá trình nung. Vì vậy, a = 19.5 g (cùng với m(Al(OH)3)).
Tóm lại:
m = 19.5 g (kết tủa Al(OH)3)a = 19.5 g (sau khi nung thành Al2O3)
Đúng 0
Bình luận (0)