
Những câu hỏi liên quan
Đồng thau là một hợp kim của Cu và Zn. Lấy một mẫu đồng thau chia thành 2 phần bằng nhau. + Phần 1: Cho vào h2SO4 dư thu được 1g rắn không tan. + Phần 2 Luyện thêm 4g Al vào thu được hỗn hợp B trong đó phần trăm khối lượng của Zn nhỏ hơn 33.3% so với phần trăm khối lượng Zn trong mẫu hỗn hợp ban đầu. a) Tính thành phần phần trăm Cu trong mẫu đồng thau biết khi ngâm hợp kim B vào NaOH sau 1 thời gian khí bay ra vượt quá 6 lít (đktc) b) Từ hợp kim B, muốn có hợp kim C chứa thành phần phần trăm về...
Đọc tiếp
Đồng thau là một hợp kim của Cu và Zn. Lấy một mẫu đồng thau chia thành 2 phần bằng nhau. + Phần 1: Cho vào h2SO4 dư thu được 1g rắn không tan. + Phần 2 Luyện thêm 4g Al vào thu được hỗn hợp B trong đó phần trăm khối lượng của Zn nhỏ hơn 33.3% so với phần trăm khối lượng Zn trong mẫu hỗn hợp ban đầu. a) Tính thành phần phần trăm Cu trong mẫu đồng thau biết khi ngâm hợp kim B vào NaOH sau 1 thời gian khí bay ra vượt quá 6 lít (đktc) b) Từ hợp kim B, muốn có hợp kim C chứa thành phần phần trăm về khối lượng của các kim loại tương ứng là 20% Cu, 50% Zn và 30% Al thì phải luyện thêm các kim loại với lượng nhỏ nhất là bao nhiêu gam
cần gấp trong 1 tiếng nx
ạ
Chia mẫu hợp kim X gồm Zn và Cu thành 2 phần bằng nhau : - Phần 1 : Cho tác dụng với dung dịch HCl dư thấy còn lại 1 gam không tan. - Phần 2 : Luyện thêm 4 gam Al thì được hợp kim X trong đó hàm lượng % của Zn trong Y giảm 33,33% so với X. Tính thành phần % của Cu trong hợp kim X biết rằng nếu ngâm hợp kim Y trong dung dịch NaOH một thời gian thì thể tích khí H2 vượt quá 6 lít (đktc). A. 16,67% B. 50% C. 25% D. 37,5%
Đọc tiếp
Chia mẫu hợp kim X gồm Zn và Cu thành 2 phần bằng nhau :
- Phần 1 : Cho tác dụng với dung dịch HCl dư thấy còn lại 1 gam không tan.
- Phần 2 : Luyện thêm 4 gam Al thì được hợp kim X trong đó hàm lượng % của Zn trong Y giảm 33,33% so với X.
Tính thành phần % của Cu trong hợp kim X biết rằng nếu ngâm hợp kim Y trong dung dịch NaOH một thời gian thì thể tích khí H2 vượt quá 6 lít (đktc).
A. 16,67%
B. 50%
C. 25%
D. 37,5%
Giải thích: Đáp án A
P1 : 1g không tan chính là Cu. Còn lại là x g Zn
=> %mZn = 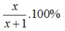
P2 : Thêm 4g Al vào => %mZn = 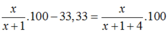
=> x = 1g => %mCu(X) = 16,67%
Đúng 0
Bình luận (0)
Chia mẫu hợp kim X gồm Zn và Cu thành 2 phần bằng nhau : - Phần 1 : cho tác dụng với dung dịch HCl dư thấy còn lại 1 g không tan - Phần 2 : Luyện thêm 4g Al thì được hợp kim X trong đó hàm lượng % của Zn trong Y giảm 33,33% so với X. Tính thành phần % của Cu trong hợp kim X biết rằng nếu ngâm hợp kim Y trong dung dịch NaOH một thời gian thì thể tích khí H2 vượt quá 6 lit (dktc) A. 16,67% B. 50% C. 25% D. 37,5%
Đọc tiếp
Chia mẫu hợp kim X gồm Zn và Cu thành 2 phần bằng nhau :
- Phần 1 : cho tác dụng với dung dịch HCl dư thấy còn lại 1 g không tan
- Phần 2 : Luyện thêm 4g Al thì được hợp kim X trong đó hàm lượng % của Zn trong Y giảm 33,33% so với X.
Tính thành phần % của Cu trong hợp kim X biết rằng nếu ngâm hợp kim Y trong dung dịch NaOH một thời gian thì thể tích khí H2 vượt quá 6 lit (dktc)
A. 16,67%
B. 50%
C. 25%
D. 37,5%
Đồng thau là một hợp kim của Cu và Zn. Lấy một mẫu đồng thau chia thành 2 phần bằng nhau.
+ Phần 1: Cho vào h2SO4 dư thu được 1g rắn không tan.
+ Phần 2 Luyện thêm 4g Al vào thu được hỗn hợp B trong đó phần trăm khối lượng của Zn nhỏ hơn 33.3% so với phần trăm khối lượng Zn trong mẫu hỗn hợp ban đầu.
a) Tính thành phần phần trăm Cu trong mẫu đồng thau biết khi ngâm hợp kim B vào NaOH sau 1 thời gian khí bay ra vượt quá 6 lít (đktc)
b) Từ hợp kim B, muốn có hợp kim C chứa thành phần phần trăm...
Đọc tiếp
Đồng thau là một hợp kim của Cu và Zn. Lấy một mẫu đồng thau chia thành 2 phần bằng nhau.
+ Phần 1: Cho vào h2SO4 dư thu được 1g rắn không tan.
+ Phần 2 Luyện thêm 4g Al vào thu được hỗn hợp B trong đó phần trăm khối lượng của Zn nhỏ hơn 33.3% so với phần trăm khối lượng Zn trong mẫu hỗn hợp ban đầu.
a) Tính thành phần phần trăm Cu trong mẫu đồng thau biết khi ngâm hợp kim B vào NaOH sau 1 thời gian khí bay ra vượt quá 6 lít (đktc)
b) Từ hợp kim B, muốn có hợp kim C chứa thành phần phần trăm về khối lượng của các kim loại tương ứng là 20% Cu, 50% Zn và 30% Al thì phải luyện thêm các kim loại với lượng nhỏ nhất là bao nhiêu gam
a)
Gọi khối lượng của Zn trong đồng thau là : a(g)
Zn+ H2SO4→ ZnSO4+ H2↑
1(g) chất rắn không tan là: Cu
Ta có PT:\(\frac{a}{a+1}.\frac{1}{3}=\frac{a}{a+1+4}\)
⇒ a= 1 (g)
%Cu (đồng thau)=11+111+1 .100%= 50%
b)
Trong B:
%Cu=\(\frac{1}{6}\) .100%= 16,67%
%Zn=\(\frac{1}{6}\).100%= 16,67%
%Al= 100%- 2. 16,67%=66,66%
⇒ Để có tỉ lệ như đề bài yêu cầu thì phải :
Tăng mCu lên: x (g)
Tăng mZn lên : y (g)
mAl giữ nguyên
Ta có :
\(\frac{x+1}{x+y+6}.100\%=20\%\)
\(\frac{y+1}{x+y+6}\text{.100%= 50%}\)
⇒ x=\(\frac{5}{3}\) (g) ; y=\(\frac{17}{3}\) (g)
A là mẫu hợp kim gồm Cu, Zn. Chia đôi A
- Phần 1 hoà tan bằng HCl dư thấy còn 1 g không tan.
- Phần 2 thêm vào 4 g Cu để được hỗn hợp B thì % lượng Zn trong B nhỏ hơn % lượng Zn trong A là 33,33%
a) Viết các PTHH
b) Tính % lượng Cu trong A, biết khi ngâm B vào dd NaOH thì sau một thời gian, thể tích khí hiđro thoát ra vượt quá 0,6 lít (đktc)
c)từ hợp kim B muốn có hợp kin C chứa 80%Cu,50%Zn và 30%Al
Đọc tiếp
A là mẫu hợp kim gồm Cu, Zn. Chia đôi A
- Phần 1 hoà tan bằng HCl dư thấy còn 1 g không tan.
- Phần 2 thêm vào 4 g Cu để được hỗn hợp B thì % lượng Zn trong B nhỏ hơn % lượng Zn trong A là 33,33%
a) Viết các PTHH
b) Tính % lượng Cu trong A, biết khi ngâm B vào dd NaOH thì sau một thời gian, thể tích khí hiđro thoát ra vượt quá 0,6 lít (đktc)
c)từ hợp kim B muốn có hợp kin C chứa 80%Cu,50%Zn và 30%Al
a, \(Zn+2HCl\rightarrow ZnCl_2H_2\)
b, Mỗi phần : \(\left\{{}\begin{matrix}Cu:x\left(g\right)\\Zn:y\left(g\right)\end{matrix}\right.\)
\(\Rightarrow x=1\) ( Cu không tan trong HCl)
\(\%_{Zn}=\frac{y.100}{y+1}\)
Phần 2: \(m_{Cu}=5\left(g\right)\)
\(\%m_{Zn}=\frac{y.100}{y+5}\Rightarrow\frac{y.100}{y+1}-\frac{y.100}{y+5}=33,33\)
\(\Leftrightarrow100y\left(y+5\right)-100y\left(y+1\right)=33,33\left(y+1\right)\left(y+5\right)\)
\(\Leftrightarrow33,33\left(y^2+6y+5\right)=400y\Rightarrow\left[{}\begin{matrix}y=1\\y=5\end{matrix}\right.\)
Vậy B \(\left[{}\begin{matrix}5\left(g\right)Cu,5\left(g\right)Zn\left(1\right)\\5\left(g\right)\left(Cu\right),1\left(g\right)Zn\left(2\right)\end{matrix}\right.\)
TH1: \(n_{Zn}=\frac{1}{13}\left(mol\right)\)
\(Zn+2NaOH\rightarrow Na_2ZnO_2+H_2\)
1/13_______________________1/13
\(\Rightarrow V_{H2}=1,723>0,6\left(TM\right)\)
TH2: \(n_{Zn}=\frac{1}{65}\left(mol\right)=n_{H2}\)
\(\Rightarrow V_{H2}=0,34\left(l\right)< 0,6\left(l\right)\left(Loai\right)\)
Vậy \(\left\{{}\begin{matrix}1\left(g\right)Cu\\5\left(g\right)Zn\end{matrix}\right.\) ( mỗi phần A)
\(\Rightarrow\%m_{Cu}=\frac{1.100}{6}=16,67\%\)
c, Xem lại đề
Chia 14,3g hỗn hợp 3 kim loại: Zn, Mg, Al thành 2 phần bằng nhau:
-Phần 1: hòa Tan hoàn toàn trong dung dịch HCl, giải phóng 5,6 lít khí (đktc) tạo ra a(g) hỗn hợp muối clorua.
-Phần 2: đem đốt cháy hoàn toàn bằng oxi tạo ra b(g) hỗn hợp 3 oxit.
tính giá trị a và b
Gọi số mol Zn, Mg, Al trong mỗi phần là x, y, z (mol)
=> 65x + 24y + 27z = 7,15 (1)
- P1:
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
x--->2x------->x------>x
Mg + 2HCl --> MgCl2 + H2
y----->2y------->y---->y
2Al + 6HCl --> 2AlCl3 + 3H2
z---->3z-------->z------>1,5z
Theo PTHH: nHCl = 2.nH2 = 0,5 (mol)
a = mmuối = mkim loại + mCl = 7,15 + 0,5.35,5 = 24,9 (g)
Có: x + y + 1,5z = 0,25
- P2
PTHH: 2Zn + O2 --to--> 2ZnO
x---->0,5x
2Mg + O2 --to--> 2MgO
y--->0,5y
4Al + 3O2 --to--> 2Al2O3
z--->0,75z
=> \(n_{O_2}=\dfrac{1}{2}\left(x+y+1,5z\right)=\) 0,125 (mol)
b = moxit = mkim loại + mO2 = 7,15 + 0,125.32 = 11,15 (g)
Đúng 3
Bình luận (0)
Chia 14,3g hỗn hợp 3 kim loại: Zn, Mg, Al thành 2 phần bằng nhau:
-Phần 1: Tan hoàn toàn trong dung dịch HCl, giải phóng 5,6 lít khí (đkc) và tạo ra a(g) hỗn hợp gồm 3 muối
-Phần 2: Bị oxi hoá hoàn toàn thu được b(g) hỗn hợp 3 oxit.
tính a và b
Chia 14,3g hỗn hợp 3 kim loại: Zn, Mg, Al thành 2 phần bằng nhau:
-Phần 1: Tan hoàn toàn trong dung dịch HCl, giải phóng 5,6 lít khí (đkc) và tạo ra a(g) hỗn hợp gồm 3 muối
-Phần 2: Bị oxi hoá hoàn toàn thu được b(g) hỗn hợp 3 oxit.
tính a và b
Theo gt ta có: $n_{H_2}=0,25(mol)$
Bảo toàn H ta có: $n_{HCl}=0,5(mol)\Rightarrow a=7,15+0,5.35,5=24,9(g)$
Bảo toàn e ta có: $n_{e}=0,5(mol)\Rightarrow n_{O_2}=0,5:4=0,125(mol)$
$\Rightarrow b=7,15+0,125.32=11,15(g)$
Đúng 2
Bình luận (0)
Chia 14,3g hỗn hợp 3 kim loại: Zn, Mg, Al thành 2 phần bằng nhau:
-Phần 1: Tan hoàn toàn trong dung dịch HCl, giải phóng 5,6 lít khí (đkc) và tạo ra a(g) hỗn hợp muối clorua.
-Phần 2: Bị oxi hoá hoàn toàn thu được b(g) hỗn hợp 3 oxit.




















