Khử hoàn toàn 8 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao. Hãy tính thể tích khí hiđro (đktc) cần dùng.(Cho Cu = 64; O = 16)
Khử hết 4 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao. Thể tích khí hiđro (ở đktc) cần dùng là
PTHH: \(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)=n_{H_2}\) \(\Rightarrow V_{H_2}=0,05\cdot22,4=1,12\left(l\right)\)
Khử hoàn toàn 8 gam đồng (II) oxit bằng khí hiđro ở nhiệt độ cao.Số gam đồng thu đc là ( Cu = 64, O = 16)
\(n_{CuO}=\dfrac{8}{80}=0,1mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,1 0,1 ( mol )
\(m_{Cu}=0,1.64=6,4g\)
nCuO=mCuO/MCuO=880=0,1(mol)
PTHH: CuO+H2→Cu+H2O
.............1.............1...............................
.............0,1...........0,1...........................
VH2(ĐKTC)=nH2⋅22,4=0,1⋅22,4=2,24(l)
tham khảo
nCuO=mCuO/MCuO=880=0,1(mol)
PTHH: CuO+H2→Cu+H2O
.............1.............1...............................
.............0,1...........0,1...........................
VH2(ĐKTC)=nH2⋅22,4=0,1⋅22,4=2,24(l)
Dùng khí hiđro để khử toàn bộ hỗn hợp gồm 24,0 gam đồng(II)oxit và 16,0 gam sắt(III)oxit ở nhiệt độ cao. Thể tích khí hiđro (ở đktc) dùng để khử hết hỗn hợp oxit trên là
`CuO+ H_2 -> Cu+ H_2O`
`0,03 ----0,03` mol
`Fe_2O_3+ 3H_2 ->2Fe + 3H_2O`
`0,1-------0,3` mol
`n_(CuO) = 2,4/80 =0,03` mol
`n_(Fe_2O_3)=16/160 =0,1` mol
`=> V_(H_2)=(0,3+0,03).22,4=7,392 l`
\(a)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Cu} = n_{CuO} = \dfrac{4}{80} = 0,05(mol)\\ \Rightarrow m_{Cu} = 0,05.64 = 3,2(gam)\\ b)\\ n_{H_2} = n_{CuO} = 0,05(mol)\\ V_{H_2} = 0,05.22,4 = 1,12(lít)\)
Khử 0,8g đồng (II) oxit bằng khí hiđro. (Cho Cu = 64; H = 1; O = 16; Cl = 35,5).Hãy: a/Tính số gam đồng kim loại thu được? b/Tính thể tích khí hiđro (đktc) cần dùng? c/Để có lượng H2 đó phải lấy bao nhiêu gam Fe cho tác dụng vừa đủ với bao nhiêu gam dd axit HCl 20
`n_[CuO]=[0,8]/80=0,01(mol)`
`H_2 + CuO` $\xrightarrow{t^o}$ `Cu + H_2 O`
`0,01` `0,01` `0,01` `(mol)`
`a)m_[Cu]=0,01.64=0,64(g)`
`b)V_[H_2]=0,01.22,4=0,224(l)`
`c)`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,01` `0,02` `0,01` `(mol)`
`@m_[Fe]=0,01.56=0,56(g)`
`@m_[dd HCl]=[0,02.36,5]/20 . 100=3,65(g)`
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
nCuO = 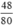 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính khối lượng đồng thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
Đốt cháy hoàn toàn 12,8 gam đồng trong lọ chứa khí oxi
a) Viết PTHH xảy ra.
b) Tính khối lượng đồng(II)oxit thu được.
c) Tính thể tích khí Hidro (đktc) cần dùng để khử hoàn toàn lượng đồng (II)oxit trên ở nhiệt độ cao.
Cho 13g kẽm phản ứng hoàn toàn với dung dịch axit clohiđric(dư).
1)tính thể tích khí hiđro sinh ra (ở đktc)
2)nếu dùng toàn bộ lượng khí hiđro sinh ra ở trên đem khử hoàn toàn 12g bột cuO ở nhiệt độ cao thì sau phản ứng thu được bao nhiêu gam đồng
1.\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
2.\(n_{CuO}=\dfrac{12}{80}=0,15mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,15 < 0,2 ( mol )
0,15 0,15 ( mol )
\(m_{Cu}=0,15.64=9,6g\)