Nêu các ứng dụng của ba kim loại: sắt, nhôm, vàng mà em biết; chỉ rõ mối liên lệ giữa tính chất và ứng dụng của chúng.

Những câu hỏi liên quan
Hãy nêu phương pháp hoá học để nhận biết ba kim loại : sắt, nhôm và đồng. Viết các phương trình hoá học.
Dùng dung dịch kiềm (thí dụ NaOH) :
- Cho 3 kim loại tác dụng với dung dịch NaOH, kim loại nào tác dụng với NaOH cho khí H 2 bay ra là Al.
2Al + 2NaOH + 2 H 2 O → 2NaAl O 2 + 3 H 2
- Cho 2 kim loại còn lại tác dụng với dung dịch HCl, kim loại nào cho khí H 2 bay ra là Fe, còn Cu không phản ứng.
Fe + 2HCl → Fe Cl 2 + H 2
Đúng 0
Bình luận (0)
Có 3 kim loại là nhôm, bạc, sắt. Hãy nêu phương pháp hóa học để nhận biết từng kim loại. Các dụng cụ hóa chất coi như có đủ. Viết các phương trình hóa học để nhận biết.
Lấy mỗi kim loại một ít làm mẫu thử Cho các mẫu thử tác dụng với dung dịch NaOH Mẫu thử nào có bọt khí bay ra là nhôm 2Al +2NaOH +2H2O →2NaAlO2 +3H2 ↑ Hai mẫu thử còn lại cho tác dụng dd HCl Mẫu nào có khí thoát ra là Fe, chất còn lại là Ag không phản ứng. Fe + 2HCl → FeCl2 + H2
Đúng 2
Bình luận (0)
Lấy mỗi chất một ít ra từng ống nghiệm riêng biệt để làm mẫu thử cho mỗi lần thí nghiệm :
Cho NaOH vào các mẫu thử nếu :
+Khí thoát ra :Al.
+Không hiện tượng là Ag , Fe .
-Tiếp tục cho dung dịch AgNO3 vào hai ống nghiệm chứa dung dịch Ag,Fe nếu :
-Có khí bay lên là Fe .
-Không hiện tượng : Ag
Fe + 2HCL ->FeCl2+ H2.
Cho các phát biểu sau: (a) Cho kim loại Ba tác dụng với dung dịch CuSO4, thu được kim loại Cu. (b) Phương pháp trao đổi ion làm mềm được nước cứng toàn phần. (c) Phèn chua được dùng để làm trong nước đục. (d) Nhôm và sắt tác dụng với khí clo dư theo cùng tỉ lệ mol. (e) Nhôm là kim loại nhẹ, có nhiều ứng dụng trong đời sống và sản xuất. Số phát biểu đúng là A. 3. B. 2. C. 5. D. 4.
Đọc tiếp
Cho các phát biểu sau:
(a) Cho kim loại Ba tác dụng với dung dịch CuSO4, thu được kim loại Cu.
(b) Phương pháp trao đổi ion làm mềm được nước cứng toàn phần.
(c) Phèn chua được dùng để làm trong nước đục.
(d) Nhôm và sắt tác dụng với khí clo dư theo cùng tỉ lệ mol.
(e) Nhôm là kim loại nhẹ, có nhiều ứng dụng trong đời sống và sản xuất.
Số phát biểu đúng là
A. 3.
B. 2.
C. 5.
D. 4.
Cho các phát biểu sau: (a) Cho kim loại Ba tác dụng với dung dịch CuSO4, thu được kim loại Cu. (b) Phương pháp trao đổi ion làm mềm được nước cứng toàn phần. (c) Phèn chua được dùng để làm trong nước đục. (d) Nhôm và sắt tác dụng với khí clo dư theo cùng tỉ lệ mol. (e) Nhôm là kim loại nhẹ, có nhiều ứng dụng trong đời sống và sản xuất. Số phát biểu đúng là A. 3. B. 2. C. 5. D. 4.
Đọc tiếp
Cho các phát biểu sau:
(a) Cho kim loại Ba tác dụng với dung dịch CuSO4, thu được kim loại Cu.
(b) Phương pháp trao đổi ion làm mềm được nước cứng toàn phần.
(c) Phèn chua được dùng để làm trong nước đục.
(d) Nhôm và sắt tác dụng với khí clo dư theo cùng tỉ lệ mol.
(e) Nhôm là kim loại nhẹ, có nhiều ứng dụng trong đời sống và sản xuất.
Số phát biểu đúng là
A. 3.
B. 2.
C. 5.
D. 4.
Đáp án D
(b) Phương pháp trao đổi ion làm mềm được nước cứng toàn phần.
(c) Phèn chua được dùng để làm trong nước đục.
(d) Nhôm và sắt tác dụng với khí clo dư theo cùng tỉ lệ mol.
(e) Nhôm là kim loại nhẹ, có nhiều ứng dụng trong đời sống và sản xuất.
Đúng 0
Bình luận (0)
Câu 3: (2,0 điểm)
Để tiến hành thí nghiệm tác dụng của kim loại nhôm với oxi và kim loại sắt với lưu huỳnh. Em hãy cho biết:
a/ Cách tiến hành thí nghiệm và nêu các hiện tượng xảy ra.
b/ Viết phương trình hoá học và rút ra kết luận.
a) (-) Nhôm và oxi Lấy bột nhôm bỏ vào 1 miếng bìa cứng . Khum tờ giấy chứa bột nhôm , rắc nhẹ bột nhôm trên ngọn lửa đèn cồn .
Hiện tượng: Có những hạt loé sáng do bột nhôm tác dụng với oxi, phản ứng toả nhiều nhiệt.
Chất tạo thành màu trắng sáng là nhôm oxit Al2O3
Giải thích: Vì xảy ra phản ứng nhôm tác dụng với oxi trong không khí.
(-) Sắt và lưa huỳnh Trộn bột sắt và bột lưa huỳnh rồi cho vào ống nghiệm ,Hơ ống nghiệm trên đèn cồn .
Hiện tượng: Khi đun hỗn hợp trên ngọn lửa đèn cồn, sắt tác dụng mạnh với lưu huỳnh hỗn hợp cháy nóng đỏ, phản ứng toả nhiều nhiệt.
Chất tạo thành có màu đen (không bị nam châm hút).
Giải thích: Vì xảy ra phản ứng sắt tác dụng với lưu huỳnh.
b) PTHH : 4Al + 3O2 → Al2O3→ Trong PƯHH nhôm đóng vai trò là chất khử.
PTHH : Fe + S → → FeS Hỗn hợp sắt và lưu huỳnh trước phản ứng có màu xám.
a)
(+) Nhôm và oxi
Lấy bột nhôm bỏ vào 1 miếng bìa cứng . Khum tờ giấy chứa bột nhôm , rắc nhẹ bột nhôm trên ngọn lửa đèn cồn .
(+) Sắt và lưa huỳnh
Trộn bột sắt và bột lưa huỳnh rồi cho vào ống nghiệm ,Hơ ống nghiệm trên đèn cồn .
b)
PTHH :
4Al + 3O2 \(\rightarrow\) 2Al2O3
PTHH :
Fe + S \(\rightarrow\) FeS
P/s : Em ms lp 8 nên ko bt đúng hay sai
Đúng 0
Bình luận (0)
Cho các kim loại sau : đồng, sắt, nhôm, bạc. Cho biết các kim loại thoả mãn những trường hợp sau : Tác dụng được với dung dịch axit và dung dịch kiềm
Nhôm tan được trong dung dịch axit và dung dịch kiềm.
2Al + 6HCl → 2Al Cl 3 + 3 H 2
2Al + 2NaOH + 2 H 2 O → 2NaAl O 2 + 3 H 2
Đúng 0
Bình luận (0)
Bài 1: Nếu có một hộp đựng viên bi sắt nhỏ và bình chia độ. Hãy nêu phương án để xác định gần đúng thể tích của một viên bi
Bài 2: a. Dựa vào tính chất nào mà kim loại đồng, kim loại nhôm lại được sử dụng làm dây điện? b. Tại sao đồng dẫn điện tốt hơn nhôm nhưng dây điện cao thế lại thường được sử dụng vật liệu nhôm chứ không sử dụng vật liệu đồng? c. Có nên để nhiều cây xanh trong phòng ngủ kín hay không? Tại sao?
Đọc tiếp
Bài 1: Nếu có một hộp đựng viên bi sắt nhỏ và bình chia độ. Hãy nêu phương án để xác định gần đúng thể tích của một viên bi
Bài 2: a. Dựa vào tính chất nào mà kim loại đồng, kim loại nhôm lại được sử dụng làm dây điện? b. Tại sao đồng dẫn điện tốt hơn nhôm nhưng dây điện cao thế lại thường được sử dụng vật liệu nhôm chứ không sử dụng vật liệu đồng? c. Có nên để nhiều cây xanh trong phòng ngủ kín hay không? Tại sao?
cho cùng 1 số mol các kim loại đồng, kẽm, nhôm, sắt tác dụng hết với dd HCl thì kim loại nào cho nhiều khí hidro nhất? A) Sắt B) Kẽm C) Đồng D) Nhôm
Đặt số mol phản các kim loại phản ứng là 1 mol
\(Cu+HCl-/\rightarrow\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ \Rightarrow n_{H_2}=n_{Zn}=1\left(mol\right)\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ \Rightarrow n_{H_2}=\dfrac{3}{2}n_{Al}=1,5\left(mol\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ \Rightarrow n_{H_2}=n_{Fe}=1\left(mol\right)\)
=> Chọn D
Đúng 2
Bình luận (0)
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng. a) Viết các phương trình phản ứng. b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất? c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Đọc tiếp
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
a) Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4loãng → FeSO4 + H2
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
b) Giả sử cho cùng một khối lượng là a g kim loại kẽm sắt và nhôm
Zn + H2SO4 → ZnSO4 + H2 (1)
Fe + H2SO4loãng → FeSO4 + H2 (2)
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2 (3)
Ta có 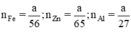
Theo pt nH2 (1) = nZn = 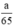 mol
mol
nH2 (2) = nFe = 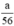 mol
mol
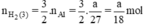
Như vậy ta nhận thấy 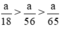 ⇒ nH2 (3) > nH2 (2) > nH2 (1)
⇒ nH2 (3) > nH2 (2) > nH2 (1)
Như vậy cho cùng một lượng kim loại tác dụng với axit H2SO4 loãng dư thì nhôm cho nhiều khí hidro hơn, sau đó đến sắt và ít nhất là kẽm
c) Nếu thu được cùng một lượng khí hidro thì khối lượng kim loại ít nhất là nhôm, sau đó đến sắt, cuối cùng là kẽm.
Đúng 1
Bình luận (0)
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng. a) Viết các phương trình phản ứng b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit thì kim loại nào cho nhiều khí hiđro nhất ?c) Nếu thu được cùng một thể tích khí Hiđro thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất ?
Đọc tiếp
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit thì kim loại nào cho nhiều khí hiđro nhất ?
c) Nếu thu được cùng một thể tích khí Hiđro thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất ?
a)
\(Zn+H2SO4\rightarrow ZnSO4+H2\)
\(2Al+3H2SO4\rightarrow Al2\left(SO4\right)3+3H2\)
\(Fe+H2SO4\rightarrow FeSO4+H2\)
b) giải sử khối KL cùng là \(m\left(g\right)\)
\(\Rightarrow n_{Zn}=\frac{m}{65}\Rightarrow n_{H_2}=\frac{m}{65}\)
\(\Rightarrow n_{Al}=\frac{m}{27}\Rightarrow n_{H_2}=1,5.\frac{m}{27}\)
\(\Rightarrow n_{Fe}=\frac{m}{56}\Rightarrow n_{H_2}=\frac{m}{56}\)
\(\Rightarrow Al\)
c) Giả sử : \(n_{H_2}=0,15mol\)
\(\Rightarrow n_{Zn}=0,15mol\Rightarrow m=9,75g\)
\(\Rightarrow n_{Al}=0,1mol\Rightarrow m=2,7g\)
\(\Rightarrow n_{Fe}=0,15mol\Rightarrow m=8,4g\)
\(\Rightarrow Al\)
Đúng 1
Bình luận (0)

















