câu 1 mô tả sự hình liên kết cộng hóa trị theo nguyên tắc dùng chung electron để tạo ra lớp vỏ electron của nguyên tố khí hiếm ( áp dụng cho các phân tử đơn giản như H2,Cl2,NH2,H2O,CO2,N2)

Những câu hỏi liên quan
Câu 616. Theo quy tắc octet (bát tử): Trong quá trình hình thành liên kết hóa học, nguyên tử các nguyên tố nhóm Á có xu hướng tạo thành lớp vỏ ngoài cùng cóA. 8 electron tương ứng với khí hiểm gần nhất.B. & electron tương ứng với khi hiếm gần nhất ( hoặc 2 electron tương ứng với khí hiểmHelium.).C. 2 electron tương ứng với kim loại gần nhất.D. 6 electron tương ứng với phi kim gần nhất.Câu 617. Nguyên tử nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khi hiếm argon khi tham...
Đọc tiếp
Câu 616. Theo quy tắc octet (bát tử): Trong quá trình hình thành liên kết hóa học, nguyên tử các nguyên tố nhóm Á có xu hướng tạo thành lớp vỏ ngoài cùng có
A. 8 electron tương ứng với khí hiểm gần nhất.
B. & electron tương ứng với khi hiếm gần nhất ( hoặc 2 electron tương ứng với khí hiểm
Helium.).
C. 2 electron tương ứng với kim loại gần nhất.
D. 6 electron tương ứng với phi kim gần nhất.
Câu 617. Nguyên tử nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khi hiếm argon khi tham gia hình thành liên kết hóa học
A. Fluorine.
B. Oxygen.
C. Hydrogen.
D. Chlorine.
Câu 618: Liên kết ion là liên kết được tạo thành
A. bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
B. bởi cặp electron chung giữa 1 nguyên tử kim loại và 1 nguyên tử phi kim.
C. bởi cặp electron chung giữa 2 nguyên tử phi kim điển hình.
D. bởi cặp electron chung giữa 2 nguyên tử kim loại.
Câu 619: Liên kết ion thường được tạo thành giữa
A. kim loại điển hình (Na, K...) và phi kim điển hình (F, Cl, O...).
B. kim loại và phi kim bất kỳ.
C. hai phi kim có chênh lệch độ âm điện không đáng
kể.
D. hai phi kim có chênh lệch độ âm điện tương đối (1,7 > Ax>0,4
Câu 620: Liên kết ion trong KC1 là do
A.kali và clo chung 1 electron tạo thành cặp electron chung lệch về phía kali
B. kali và cho góp chung 1 electron tạo thành cặp electron chung lệch về phía cho.
C. nguyên tử kali có nhường electron tạo anion, nguyên tử clo nhận electron tạo cation.
D. nguyên tử kali có nhường electron tạo cation, nguyên tử clo nhận electron tạo anion.
Câu 621: Bản chất liên kết trong phân tử NaCl là
A. liên kết ion.
B. liên kết cộng hóa trị có cực.
C. liên kết cộng hóa trị không cực.
D. liên kết phối trí (cho nhận).
Câu 622: Chất nào dưới đây có liên kết ion :
A. Cl₂
B. HCI
C. NaF
D. O₂
Câu 623: Dãy các chất đều chứa liên kết ion là:
B. Na O, MgO, HCI
D. O2, NaCl, KCI
A. Cl₂, NaCl, H₂O
C. NaF, KCI, KO
623: C
622: C
621: A
619:A
617: D
618:A
Đúng 1
Bình luận (0)
Mô tả sự tạo thành liên kết trong phân tử F2, HBr, HCl, C2H4, CO2, N2 theo quan điểm hình thành các cặp electron dùng chung
Quan sát Hình 6.6 và cho biết khi nguyên tử O liên kết với hai nguyên tử H theo cách dùng chung electron thì lớp vỏ của nguyên tử oxygen giống lớp vỏ của nguyên tử khí hiếm nào?
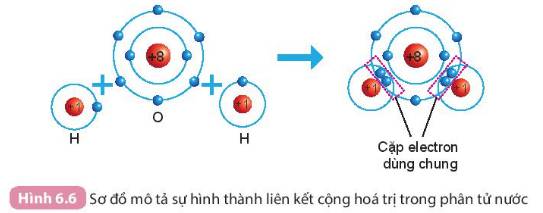
Nguyên tử `O` liên kết với nguyên tử `H` theo cách dùng chung electron, vỏ nguyên tử lớp oxygen giống lớp vỏ của nguyên tử khí hiếm `Ne`.
Đúng 2
Bình luận (0)
Chọn câu đúng nhất về liên kết cộng hóa trị. Liên kết cộng hóa trị là liên kết A. Giữa các phi kim với nhau. B. Trong đó cặp electron chung bị lệch về một nguyên tử. C. Được hình thành do sự dùng chung electron của 2 nguyên tử khác nhau. D. Được tạo nên giữa 2 nguyên tử bằng một hay nhiều cặp electron chung.
Đọc tiếp
Chọn câu đúng nhất về liên kết cộng hóa trị.
Liên kết cộng hóa trị là liên kết
A. Giữa các phi kim với nhau.
B. Trong đó cặp electron chung bị lệch về một nguyên tử.
C. Được hình thành do sự dùng chung electron của 2 nguyên tử khác nhau.
D. Được tạo nên giữa 2 nguyên tử bằng một hay nhiều cặp electron chung.
Tại sao vỏ nguyên tử khí hiếm lại đặc biệt?A. Vì vỏ nguyên tử khí hiếm có 8 electron ở lớp ngoài cùng ( trừ helium là 2 electron ).B. Vì vỏ nguyên tử khí hiếm không liên kết được.C. Vì mỗi vỏ nguyên tử của các nguyên tử có tối đa 8 electron ở lớp ngoài cùng ( trừ lớp ngoài cùng của các nguyên tử thuộc chu kì 1 trong bảng tuần hoàn có tối đa 2 electron ).D. Tất cả đều đúng.
Đọc tiếp
Tại sao vỏ nguyên tử khí hiếm lại đặc biệt?
A. Vì vỏ nguyên tử khí hiếm có 8 electron ở lớp ngoài cùng ( trừ helium là 2 electron ).
B. Vì vỏ nguyên tử khí hiếm không liên kết được.
C. Vì mỗi vỏ nguyên tử của các nguyên tử có tối đa 8 electron ở lớp ngoài cùng ( trừ lớp ngoài cùng của các nguyên tử thuộc chu kì 1 trong bảng tuần hoàn có tối đa 2 electron ).
D. Tất cả đều đúng.
D. Tất cả đều đúng.
Vỏ nguyên tử khí hiếm đặc biệt vì chúng có 8 electron ở lớp ngoài cùng (trừ helium là 2 electron), điều này làm cho chúng có cấu trúc electron ổn định và ít có xu hướng tạo liên kết hóa học với các nguyên tử khác. Mỗi vỏ nguyên tử của các nguyên tử có tối đa 8 electron ở lớp ngoài cùng (trừ lớp ngoài cùng của các nguyên tử thuộc chu kì 1 trong bảng tuần hoàn có tối đa 2 electron).
Vỏ nguyên tử khí hiếm đặc biệt vì chúng có 8 electron ở lớp ngoài cùng (trừ helium là 2 electron), điều này làm cho chúng có cấu trúc electron ổn định và ít có xu hướng tạo liên kết hóa học với các nguyên tử khác. Mỗi vỏ nguyên tử của các nguyên tử có tối đa 8 electron ở lớp ngoài cùng (trừ lớp ngoài cùng của các nguyên tử thuộc chu kì 1 trong bảng tuần hoàn có tối đa 2 electron).
Đúng 1
Bình luận (0)
Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
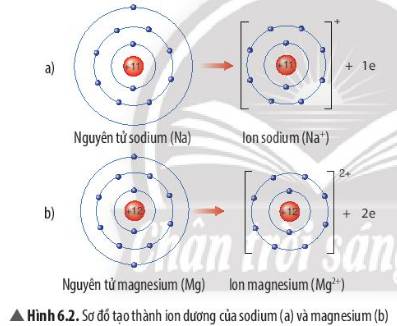
- Sự tạo thành ion sodium: Nguyên tử sodium (Na) cho đi 1 electron lớp ngoài cùng để tạo thành ion dương Na+
- Sự tạo thành ion magnesium: Nguyên tử magnesium (Mg) cho đi 2 electron lớp ngoài cùng để tạo thành ion dương Mg2+
=> Sau khi nhường electron, ion sodium và ion magnesium đều có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
Đúng 0
Bình luận (0)
Quan sát Hình 6.3, em hãy mô tả sự tạo thành ion chloride, ion oxide. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
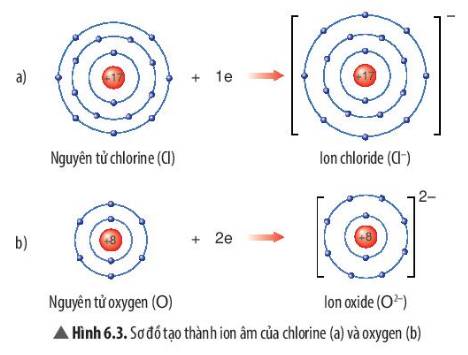
- Sự tạo thành ion chloride: Nguyên tử chlorine (Cl) nhận thêm 1 electron ở lớp ngoài cùng để tạo thành ion âm Cl-
- Sự tạo thành ion oxide: Nguyên tử oxygen (O) nhận thêm 2 electron ở lớp ngoài cùng để tạo thành ion âm O2-
- Sau khi nhận electron, ion chloride có 3 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
- Sau khi nhận electron, ion oxide có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử Argon (Ar)
Đúng 0
Bình luận (0)
Quan sát hình 6.1, hãy so sánh hóa trị của nguyên tố và số electron mà nguyên tử của nguyên tố đã góp chung để tạo ra liên kết
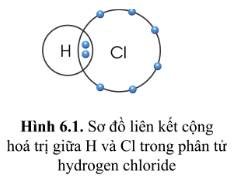
Hóa trị của H và Cl đều là I, bằng với số electron mà nguyên tử H và Cl góp chung để tạo ra liên kết.
Đúng 0
Bình luận (0)
Cho các phân tử sau: KCl, H 2 O , N 2 và N a 2 O .
Biết số hiệu nguyên tử của các nguyên tố lần lượt là: H = 1, N = 7, O = 8, Na = 11, Cl = 17, K = 19.
Viết công thức electron và công thức cấu tạo của các phân tử chứa liên kết cộng hoá trị.
Viết CT electron và công thức cấu tạo của phân tử chứa liên kết cộng hoá trị: N 2 và H 2 O (1,0 điểm)

Đúng 0
Bình luận (0)
Mô tả sự hình thành phân tử N2 từ hai nguyên tử N. Phân tử N2 có bao nhiêu cặp electron dùng chung? Viết công thức Lewis của N2.
- Cấu hình electron của N (Z = 7): 1s22s22p3
- Để đạt cấu hình của khí hiếm gần nhất, mỗi nguyên tử N đều cần thêm 3 electron. Vì vậy mỗi nguyên tử N cùng góp 3 electron để tạo nên 3 cặp electron chung cho 2 nguyên tử N.
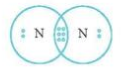
⟹ Số cặp electron dùng chung là 3.
⟹ Công thức Lewis của N2:
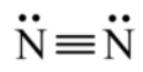
Đúng 0
Bình luận (0)






















