Khi làm thí nghiệm, làm thế nào để biết một phản ứng là tỏa nhiệt hay thu nhiệt?

Những câu hỏi liên quan
Trong các phản ứng hóa học ở thí nghiệm 2 và thí nghiệm 3, phản ứng nào tỏa nhiệt, phản ứng nào thu nhiệt?

Thí nghiệm 2: Thu nhiệt
Thí nghiệm 3: Toả nhiệt
Đúng 0
Bình luận (0)
Phản ứng tỏa nhiệt là thí nghiệm 2, phản ứng thu nhiệt là thí nghiệm 3
Đúng 0
Bình luận (0)
Thí nghiệm dưới đây mô tả quá trình của phản ứng nhiệt nhôm Cho các phát biểu sau: (1) X là Al2O3 nóng chảy và Y là Fe nóng chảy. (2) Phần khói trắng bay ra là Al2O3. (3) Dải Mg khi đốt được dùng để khơi mào phản ứng nhiệt nhôm. (4) Phản ứng nhiệt nhôm là phản ứng tỏa nhiệt. (5) Phản ứng nhiệt nhôm được sử dụng để điều chế một lượng nhỏ sắt khi hàn đường ray. Số phát biểu đúng là A. 4 B. 5 C. 2 D. 3
Đọc tiếp
Thí nghiệm dưới đây mô tả quá trình của phản ứng nhiệt nhôm
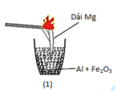
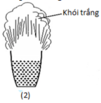

Cho các phát biểu sau:
(1) X là Al2O3 nóng chảy và Y là Fe nóng chảy.
(2) Phần khói trắng bay ra là Al2O3.
(3) Dải Mg khi đốt được dùng để khơi mào phản ứng nhiệt nhôm.
(4) Phản ứng nhiệt nhôm là phản ứng tỏa nhiệt.
(5) Phản ứng nhiệt nhôm được sử dụng để điều chế một lượng nhỏ sắt khi hàn đường ray.
Số phát biểu đúng là
A. 4
B. 5
C. 2
D. 3
Chọn C
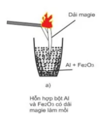
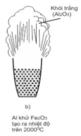
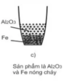
Người ta dùng phản ứng này để hàn đường ray xe lửa
Đúng 0
Bình luận (0)
C1. Trong thí nghiệm trên, yếu tố nào ở hai cốc được giữ giống nhau, yếu tố nào được thay đồi ? Tại sao phải làm như thế ? Hãy tìm số thích hợp cho các ô trống ở hai cột cuối bảng 24.1. Biết nhiệt lượng ngọn lửa đèn cồn truyền cho nước tỉ lệ với thời gian đun.
C2. Từ thí nghiệm trên có thể kết luận gì về mỗi quan hệ giữa nhiệt lượng vật cần thu vào để nóng lên và khối lượng của vật?
C3. Trong thí nghiệm này phải giữ không đổi những yếu tố nào? Muốn vậy phải làm thế nào?
C4. Trong thí nghiệm n...
Đọc tiếp
C1. Trong thí nghiệm trên, yếu tố nào ở hai cốc được giữ giống nhau, yếu tố nào được thay đồi ? Tại sao phải làm như thế ? Hãy tìm số thích hợp cho các ô trống ở hai cột cuối bảng 24.1. Biết nhiệt lượng ngọn lửa đèn cồn truyền cho nước tỉ lệ với thời gian đun.
C2. Từ thí nghiệm trên có thể kết luận gì về mỗi quan hệ giữa nhiệt lượng vật cần thu vào để nóng lên và khối lượng của vật?
C3. Trong thí nghiệm này phải giữ không đổi những yếu tố nào? Muốn vậy phải làm thế nào?
C4. Trong thí nghiệm này phải thay đổi yếu tố nào ? Muốn vậy phải làm thế nào?
C5. Từ thí nghiệm trên có thể rút ra kết luận gì về mỗi quan hệ giữa nhiệt lượng vật thu vào để nóng lên và độ tăng nhiệt độ?
C6. Trong thí nghiệm này những yếu tố nào thay đổi, không thay đổi ?
C1. Trong thí nghiệm trên, yếu tố nào ở hai cốc được giữ giống nhau, yếu tố nào được thay đồi ? Tại sao phải làm như thế ? Hãy tìm số thích hợp cho các ô trống ở hai cột cuối bảng 24.1. Biết nhiệt lượng ngọn lửa đèn cồn truyền cho nước tỉ lệ với thời gian đun.
Bài giải:
Độ tăng nhiệt độ và chất làm vật được giữ giống nhau; khối lượng khác nhau. Để tìm hiểu mỗi quan hệ giữa nhiệt lượng và khối lượng.
C2. Từ thí nghiệm trên có thể kết luận gì về mỗi quan hệ giữa nhiệt lượng vật cần thu vào để nóng lên và khối lượng của vật ?
Bài giải:
Khối lượng càng lớn thì nhiệt lượng vật thu vào càng lớn.
C3. Trong thí nghiệm này phải giữ không đổi những yếu tố nào ? Muốn vậy phải làm thế nào ?
Bài giải:
Phải giữ khối lượng và chất làm vật giống nhau. Muốn vậy hai cốc phải đựng cùng một lượng nước.
C4. Trong thí nghiệm này phải thay đổi yếu tố nào ? Muốn vậy phải làm thế nào ?
Sau đây là bảng kết quả thí nghiệm làm với hai cốc, mỗi cốc đựng 50 g nước, được lần lượt đun nóng bằng đền cồn trong 5 phút, 10 phút (H.24.2). Hãy tìm số thích hợp cho các ô trống ở hai cột cuối bảng 24.2.
Bài giải:
Phải cho độ tăng nhiệt độ khác nhau. Muốn vậy phải để cho nhiệt độ cuối của 2 cốc khác nhau bằng cách cho thời gian đun khác nhau.
C5. Từ thí nghiệm trên có thể rút ra kết luận gì về mỗi quan hệ giữa nhiệt lượng vật thu vào để nóng lên và độ tăng nhiệt độ ?
Bài giải:
Độ tăng nhiệt độ càng lớn thì nhiệt lượng vật thu vào càng lớn.
C6. Trong thí nghiệm này những yếu tố nào thay đổi, không thay đổi ?
Bài giải:
Khối lượng không đổi, độ tăng nhiệt độ giống nhau, chất làm vật khác nhau.
Đúng 0
Bình luận (0)
Trong thí nghiệm (câu hỏi 1), để tìm mối quan hệ giữa nhiệt lượng vật cần thu vào để nóng lên và độ tăng nhiệt độ cần phải thay đổi yếu tố nào? Muốn vậy phải làm thế nào? Trong thí nghiệm như hình 24.2, thí nghiệm làm với 2 cốc, mỗi cốc đựng 50 g nước, được lần lượt đun nóng bằng đèn cồn trong 5 phút, 10 phút. Kết quả ghi ở bảng 24.2
Đọc tiếp
Trong thí nghiệm (câu hỏi 1), để tìm mối quan hệ giữa nhiệt lượng vật cần thu vào để nóng lên và độ tăng nhiệt độ cần phải thay đổi yếu tố nào? Muốn vậy phải làm thế nào?
Trong thí nghiệm như hình 24.2, thí nghiệm làm với 2 cốc, mỗi cốc đựng 50 g nước, được lần lượt đun nóng bằng đèn cồn trong 5 phút, 10 phút.
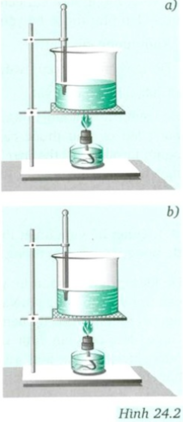
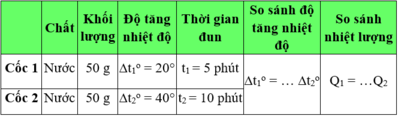
Kết quả ghi ở bảng 24.2
* Cần phải thay đổi độ tăng nhiệt độ của hai cốc khác nhau. Muốn vậy thời gian đun hai cốc phải khác nhau.
* Kết quả ghi ở bảng 24.2
Ta có: Δt1o = 1/2 .Δt2o và Q2 = 1/2 .Q1
Đúng 0
Bình luận (0)
Không được làm việc nào sau đây khi làm thí nghiệm kiểm tra xem tốc độ bay hơi của một chất lỏng có phụ thuộc vào nhiệt độ hay không? A. Dùng hai đĩa giống nhau. B. Đặt hai đĩa đựng cùng một lượng chất lỏng vào cùng một nơi. C. Dùng hai đĩa đựng hai chất lỏng khác nhau. D. Chỉ làm nóng một đĩa.
Đọc tiếp
Không được làm việc nào sau đây khi làm thí nghiệm kiểm tra xem tốc độ bay hơi của một chất lỏng có phụ thuộc vào nhiệt độ hay không?
A. Dùng hai đĩa giống nhau.
B. Đặt hai đĩa đựng cùng một lượng chất lỏng vào cùng một nơi.
C. Dùng hai đĩa đựng hai chất lỏng khác nhau.
D. Chỉ làm nóng một đĩa.
Để kiểm tra tốc độ bay hơi của một chất lỏng phụ thuộc vào các yếu tố: nhiệt độ, gió, mặt thoáng thì phải làm với cùng một chất lỏng nhưng thực hiện ở các điều kiện nhiệt độ, gió, mặt thoáng khác nhau
⇒ Đáp án C
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm cần dùng 28 bình chứa khí oxi để làm thí nghiệm, mỗi bình có dung tích là 100ml. Tính khối lượng thuốc tím (KMnO4) cần dùng để khi nhiệt phân thu đc đủ lượng khí oxi trên, biết khi thu lượng khí oxi bị hao hụt mất 20%
Giúp mik vs ạ mik cám ơn trc :33
\(V_{O_2\left(thu.được\right)}=28=0,1=2,8\left(l\right)\)
=> \(V_{O_2\left(sinh.ra\right)}=\dfrac{2,8.100}{80}=3,5\left(l\right)\)
=> \(n_{O_2\left(sinh.ra\right)}=\dfrac{3,5}{22,4}=0,15625\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3125<------------------------0,15625
=> mKMnO4 = 0,3125.158 = 49,375 (g)
Đúng 2
Bình luận (0)
Biến thiên entanpi của phản ứng (kí hiệu là Delta H) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì Delta H có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì Delta H có dấu dương. Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và các liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính Delta H của phản ứng, người ta dựa vào năng lượng các liên kết left(E_{lk}right). E_{lk} là năng lượng cần cung cấp...
Đọc tiếp
Biến thiên entanpi của phản ứng (kí hiệu là \(\Delta H\)) có thể hiểu đơn giản là nhiệt tỏa ra hoặc thu vào khi phản ứng hóa học xảy ra. Nếu phản ứng tỏa nhiệt thì \(\Delta H\) có dấu âm và ngược lại, nếu phản ứng thu nhiệt thì \(\Delta H\) có dấu dương. Khi một phản ứng hóa học xảy ra, các liên kết trong chất phản ứng bị cắt đứt và các liên kết mới được hình thành, tạo nên chất sản phẩm. Để tính \(\Delta H\) của phản ứng, người ta dựa vào năng lượng các liên kết \(\left(E_{lk}\right)\). \(E_{lk}\) là năng lượng cần cung cấp để cắt đứt một liên kết thành các nguyên tử ở thể khí. Năng lượng tỏa ra khi hình thành liên kết đó từ các nguyên tử ở thể khí cũng có giá trị bằng giá trị của \(E_{lk}\) nhưng có dấu ngược lại.
\(E_{lk}\) của một số liên kết được cho trong bảng sau:
| Liên kết | C\(\equiv\)C\(\) | C-C | C-H | H-H |
| \(E_{lk}\left(kJ/mol\right)\) | 839,0 | 343,3 | 418,4 | 432,0 |
Xét phản ứng: \(C_2H_2+2H_2\rightarrow C_2H_6\left(1\right)\)
Dựa vào bảng số liệu trên hãy:
a. Tính năng lượng cần cung cấp để phá vỡ liên kết của các chất tham gia trong phản ứng (1) (Lưu ý hệ số của các chất trong phương trình phản ứng).
b. Tính năng lượng tỏa ra khi hình thành các liên kết trong chất sản phẩm của phản ứng (1)
c. Từ các kết quả trên, xác định \(\Delta H\) của phản ứng (1) và cho biết phản ứng (1) tỏa nhiệt hay thu nhiệt.
\(a.E_r=839,0+2\cdot418,4+2\cdot432,0=2539,8kJ\\ b.E_p=343,3+6\cdot418,4=2853,7kJ\\ c.\Delta_rH^{^{ }0}=2539,8-3197=-313,9kJ\cdot mol^{-1}\\ \Delta H< 0:pư.thu.nhiệt\)
Đúng 1
Bình luận (1)
\(a.E_{reactants}=839,0+2\cdot432,0=1703kJ\\ b.E_{products}=343,3+6\cdot432,0=2935,3kJ\\ c.\Delta_rH^{^o}_{298}=E_r-E_p=1703-2935,3=1232,3kJ\cdot mol^{^{ }-1}.\)
\(\Delta H< 0\) => Phản ứng (1) thu nhiệt
Đúng 0
Bình luận (3)
Các bạn chỉ mình ví dụ như đề cho chưa rõ nhiệt lượng thu và , nghiệt lượng tỏa thì làm như thế nào để nhận biết được ạ
Biện pháp nào làm tăng hiệu suất tổng hợp SO3 từ SO2 và O2 trong công nghiệp ? Biết phản ứng tỏa nhiệt. (a) Thay O2 không khí bằng O2 tinh khiết. (b) Tăng áp suất bằng cách nén hỗn hợp. (c) Thêm xúc tác V2O5. (d) Tăng nhiệt độ để tốc độ phản ứng A. (b), (c). B. (a), (b). C. (a). D. (a), (b), (c), (d).
Đọc tiếp
Biện pháp nào làm tăng hiệu suất tổng hợp SO3 từ SO2 và O2 trong công nghiệp ? Biết phản ứng tỏa nhiệt.
(a) Thay O2 không khí bằng O2 tinh khiết.
(b) Tăng áp suất bằng cách nén hỗn hợp.
(c) Thêm xúc tác V2O5.
(d) Tăng nhiệt độ để tốc độ phản ứng
A. (b), (c).
B. (a), (b).
C. (a).
D. (a), (b), (c), (d).
Chọn B
Thay O2 không khí bằng O2 tinh khiết là làm tăng nồng độ của O2. Trường hợp này cân bằng chuyển dịch theo chiều thuận, do đó làm tăng hiệu suất của phản ứng.
Tăng áp suất thì cân bằng hóa học sẽ chuyển dịch theo chiều làm giảm số phân tử khí, tức là chiều thuận, do đó cũng làm tăng hiệu suất tổng hợp SO3.
Chất xúc tác không làm ảnh hưởng đến sự chuyển dịch cân bằng, nó chỉ giúp cho cân bằng nhanh chóng được thiết lập.
Tăng nhiệt độ thì cân bằng sẽ chuyển dịch theo chiều thu nhiệt, tức là chiều nghịch, do đó làm giảm hiệu suất phản ứng.
Vậy các biện pháp (a) và (b) là tăng hiệu suất phản ứng
Đúng 0
Bình luận (0)























