base là gì

Những câu hỏi liên quan
Tìm hiểu khái niệm baseBảng 9.1. Tên một số base thông dụng, công thức hoá học và dạng tồn tại của base trong dung dịchQuan sát Bảng 9.1 và thực hiện các yêu cầu:1. Công thức hoá học của các base có đặc điểm gì giống nhau?2. Các dung dịch base có đặc điểm gì chung?3. Thảo luận nhóm và đề xuất khái niệm về base.4. Em hãy nhận xét về cách gọi tên base và đọc tên base Ca(OH)2.
Đọc tiếp
Tìm hiểu khái niệm base
Bảng 9.1. Tên một số base thông dụng, công thức hoá học và dạng tồn tại của base trong dung dịch
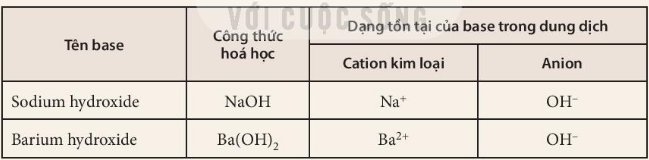
Quan sát Bảng 9.1 và thực hiện các yêu cầu:
1. Công thức hoá học của các base có đặc điểm gì giống nhau?
2. Các dung dịch base có đặc điểm gì chung?
3. Thảo luận nhóm và đề xuất khái niệm về base.
4. Em hãy nhận xét về cách gọi tên base và đọc tên base Ca(OH)2.
1. Có một hay nhiều nhóm OH-
2. Các dung dịch base gồm 1 cation kim loại và anion OH-
3. Base là những hợp chất trong phân tử có nguyên tử kim loại liên kết với nhóm hydroxide. Khi tan trong nước, base tạo ra ion OH-
4. Quy tắc gọi tên các base: Tên kim loại (kèm hoá trị đối với kim loại có nhiều hoá trị) + hydroxide.
Tên base Ca(OH)2: Calcium hydroxide.
Đúng 0
Bình luận (0)
Dựa vào bảng tính tan dưới đây, hãy cho biết những base nào là base không tan và những base nào là base kiềm? Viết công thức hoá học và đọc tên các base có trong bảng.
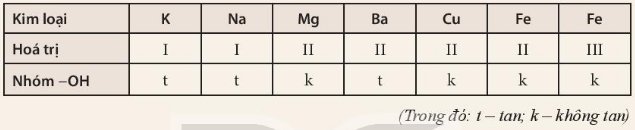
Base không tan:
Mg(OH)2: magnesium hydroxide.
Cu(OH)2: copper(II) hydroxide.
Fe(OH)3: iron(III) hydroxide.
Fe(OH)2: iron(II) hydroxide.
Base kiềm
KOH: potassium hydroxide.
Ba(OH)2:barium hydroxide
NaoOH:sodium hydroxide
Đúng 2
Bình luận (0)
Cho các chất: NaOH, KCl, HCl, HNO3, Cu(OH)2, Fe(OH)3, MgSO4, H2SO4, KOH, Ba(OH)2, C2H5OH, Mg(OH)2. (a) Cho biết trong các chất trên, chất nào là base tan? Chất nào là base không tan? (b) Gọi tên các base trên.
Cần lưu ý nhé: HCl, HNO3 và H2SO4 là axit chứ không phải là bazơ, KCl mang tính trung tính vì là chất này được tạo từ cả bazơ mạnh lẫn axit mạnh. C2H5OH là chất điện li nên cũng không phải là bazơ
a)
- Những chất là bazơ tan:
+ NaOH
+ KOH
+ Ba (OH)2
- Những chất là bazơ không tan:
+ Cu(OH)2
+ Fe(OH)3
+ Mg(OH)2
b)
NaOH: Natri Hidroxide
KCl: Kali Clohidric
HCl: Axit Clohidric
HNO3: Axit Nitric
Cu (OH)2: Đồng (II) Hidroxide
Fe(OH)3: Sắt (III) Hidroxide
MgSO4: Magiê Surfuric
H2SO4: Axit Surfuric
KOH: Kali Hidroxide
Ba(OH)2: Bari Hidroxide
C2H5OH: Ancol Etylic
Mg(OH)2: Magiê Hidroxide
#HT
Đúng 1
Bình luận (0)
Cho 15,5 gam Na2O tác dụng với nước, thu được 0,5 lit dung dịch Base.
1. Tính nồng độ mol của dung dịch Base thu được.
2. Tính thể tích dung dịch H2SO4 20%, có khối lượng riêng là 1,14g/ml cần dùng để trung hòa dung dịch Base nói trên
1. \(n_{Na_2O}=\dfrac{15,5}{62}=0,25\left(mol\right)\)
PTHH: Na2O + H2O → 2NaOH
Mol: 0,25 0,5
\(C_{M_{ddNaOH}}=\dfrac{0,5}{0,5}=1M\)
2.
PTHH: 2NaOH + H2SO4 → Na2SO4 + 2H2O
Mol: 0,5 0,25
\(m_{ddH_2SO_4}=\dfrac{0,25.98.100}{20}=122,5\left(g\right)\)
\(V_{ddH_2SO_4}=\dfrac{122,5}{1,14}=107,456\left(ml\right)\)
Đúng 1
Bình luận (0)
\(n_{Na2O}=\dfrac{m_{Na2O}}{M_{Na2O}}=0,25\left(mol\right)\)
\(Na_2O+H_2O\rightarrow2NaOH\)
0,25 mol - 0,25 mol - 0,5 mol
a) \(C_{M_{NaOH}}=\dfrac{n_{NaOH}}{V_{NaOH}}=1\left(M\right)\)
b) \(H_2SO_4+2NaOH\rightarrow Na_2SO4+2H_2O\)
0,25 mol - 0,5 mol - 0,25 mol - 0,5 mol
\(m_{ctH2SO4}=n_{H2SO4}.M_{H2SO4}=24,5\left(g\right)\)
\(C_{\%_{H2SO4}}=\dfrac{m_{ctH2SO4}}{m_{ddH2SO4}}.100\%\)
\(\Rightarrow m_{ddH2SO4}=\dfrac{m_{ctH2SO4}.100\%}{C_{\%_{H2SO4}}}=122,5\left(g\right)\)
\(D_{H2SO4}=\dfrac{m_{ddH2SO4}}{V_{H2SO4}}\Rightarrow V_{H2SO4}=\dfrac{m_{ddH2SO4}}{D_{H2SO4}}\approx107,46\left(ml\right)\)
Đúng 1
Bình luận (0)
Trên sân bóng chày dành cho nam, các vị trí gôn Nhà (Home plate), gôn 1 (First base), gôn 2 (Second base), gôn 3 (Third base) là bốn đỉnh của một hình vuông có cạnh dài 27,4 m. Vị trí đứng ném bóng (Pitcher’s mound) nằm trên đường nối gôn Nhà với gôn 2, và cách gôn Nhà 18,44 m. Tính các khoảng cách từ vị trí đứng ném bóng tới các gôn 1 và gôn 3.
Đọc tiếp
Trên sân bóng chày dành cho nam, các vị trí gôn Nhà (Home plate), gôn 1 (First base), gôn 2 (Second base), gôn 3 (Third base) là bốn đỉnh của một hình vuông có cạnh dài 27,4 m. Vị trí đứng ném bóng (Pitcher’s mound) nằm trên đường nối gôn Nhà với gôn 2, và cách gôn Nhà 18,44 m. Tính các khoảng cách từ vị trí đứng ném bóng tới các gôn 1 và gôn 3.

Tham khảo:
Kí hiệu gôn Nhà, gôn 1, gôn 2, gôn 3 và vị trí ném bóng lần lượt là các điểm A, B, C, D, O như hình vẽ.
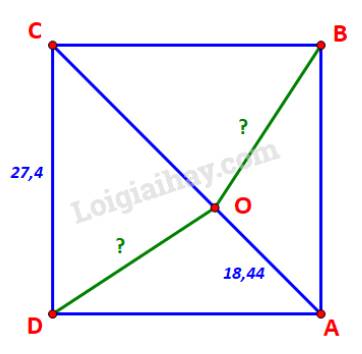
Ta có: \(CD = 27,4 \Rightarrow AC = CD.\sqrt 2 = 27,4.\sqrt 2 \approx 38,75\)
\( \Rightarrow OC = AC - OA \approx 38,75 - 18,44 = 20,31\)
Xét tam giác OCD ta có:
Định lí cos: \(O{D^2} = C{D^2} + C{O^2} - 2.CD.CO.\cos C\)
Trong đó \(\left\{ \begin{array}{l}CD = 27,4\\CO = 20,31\\\widehat C = {45^o}\end{array} \right.\)
\(\begin{array}{l} \Rightarrow O{D^2} = 27,{4^2} + 20,{31^2} - 2.27,4.20,31.\cos {45^o}\\ \Leftrightarrow O{D^2} \approx 376,255\\ \Leftrightarrow OD \approx 19,4\;(m)\end{array}\)
Dễ thấy \(\Delta \,COB = \Delta \,COD\)(c.g.c) \( \Rightarrow OB = OD = 19,4\;(m)\)
Đúng 0
Bình luận (0)
Cách nhận biết đâu là oxide base
Đâu là oxide acid
oxide base: kim loại + oxi
oxide acid: phi kim + oxi
Đúng 2
Bình luận (0)
Chứng minh NaOH là base theo thuyết bronsted
\(NaOH\rightarrow Na^++OH^-\)
OH- có khả năng nhận proton H+ nên NaOH là base
Đúng 1
Bình luận (0)
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giú...
Đọc tiếp
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giúp với ạ các bạn........
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giả...
Đọc tiếp
9. Sự điện ly của nước? Chỉ số pH và pOH? Tính chất acid-base của môi trường? Biểu diễn tính chất acidbase của môi trường qua pH?
10. Định nghĩa acid, base theo lý thuyết acid-base của Arrhenius; thuyết proton về acid, base của BronstedLowry; thuyết electron về acid, base của Lewis?
11. Thuyết proton về acid, base của Bronsted-Lowry: Cặp acid/base liên hợp; Tính chất acid-base của một chất trong dung môi nước; Phản ứng acid-base? Quan hệ giữa Ka và Kb của một cặp acid/base liên hợp HA/A−?
giải giúp mình vơi ạ






















