Nêu hiện tượng quan sát được khi thực hiện thí nghiệm sau và giải thích?
Ngâm dây Aluminium trong dung dịch giấm ăn?
hãy mô tả hiện tượng và viết phương trình phản ứng khi thực hiện thí nghiệm thí sau: a. cho một ít bộ sát vào ống nghiệm chứa dung dịch HCL. b. ngâm sợi dây đồng cho dung dịch bạc nitrot AgNO3
a) Sắt tan dần, xuất hiện bọt khí không màu không mùi
$Fe +2 HCl \to FeCl_2 + H_2$
b) Dung dịch chuyển dần sang màu xanh lam, có chất rắn màu trắng bạc bám trên dây đồng
$Cu + 2AgNO_3 \to Cu(NO_3)_2 + 2Ag$
a) Bột sắt tan dần, có khí thoát ra
Fe + 2HCl --> FeCl2 + H2
b) Một phần dây đồng tan vào dd, xuất hiện chất rắn màu xám, dd dần chuyển màu xanh
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
a) Bột sắt tan dần, có khí thoát ra
Fe + 2HCl --> FeCl2 + H2
b) Một phần dây đồng tan vào dd, xuất hiện chất rắn màu xám, dd dần chuyển màu xanh
Cu+2AgNO3→Cu(NO3)2+2Ag
Thực hiện các thí nghiệm sau:
(a). Đốt bột nhôm nguyên chất trong không khí
(b). Ngâm thanh thép vào dung dịch giấm ăn.
(c). Ngâm thanh đồng nguyên chất vào dung dịch FeCl3.
(d). Cho lá kẽm nguyên chất vào dung dịch chứa H2SO4 và CuSO4.
Các thí nghiệm không xảy ra ăn mòn điện hóa là
A. (a),(b).
B. (c),(d).
C. (b),(d).
D. (a),(c).
Chọn đáp án D
Điều kiện xảy ra ăn mòn điện hóa:
Phải có hai điện cực khác nhau về bản chất.
Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn và phải cùng tiếp xúc với một dung dịch điện li.
Xét các thí nghiệm:
(a) Không xảy ra ăn mòn điện hóa vì không có hai điện cực khác nhau về bản chất và không có dung dịch điện li.
(b) Xảy ra ăn mòn điện hóa. Hai điện cực Fe và C tiếp xúc với nhau và cùng tiếp xúc với dung dịch giấm ăn.
(c) Không xảy ra ăn mòn điện hóa vì không có hai điện cực khác nhau về bản chất.
Tính khử của Cu yếu hơn Fe nên không khử được Fe3+ về Fe.
![]()
Xảy ra ăn mòn điện hóa. Khi cho Zn vào dung dịch chứa H2SO4 và CuSO4 thì xảy ra phản ứng sau:
![]() .
.
Kim loại Cu sinh ra bám vào thanh Zn, tạo thành điện cực thứ hai tiếp xúc với điện cực Zn và cùng tiếp xúc với dung dịch điện li. Hai thí nghiệm không xảy ra ăn mòn điện hóa là (a) và (c).
Thực hiện các thí nghiệm sau:
(a). Đốt bột nhôm nguyên chất trong không khí.
(b). Ngâm thanh thép vào dung dịch giấm ăn.
(c). Ngâm thanh đồng nguyên chất vào dung dịch FeCl3.
(d). Cho lá kẽm nguyên chất vào dung dịch chứa H2SO4 và CuSO4.
Các thí nghiệm không xảy ra ăn mòn điện hóa là
A. (a),(b).
B. (c),(d).
C. (b),(d).
D. (a),(c).
Tiến hành Thí nghiệm 3, nêu hiện tượng quan sát được và giải thích kết quả thí nghiệm.

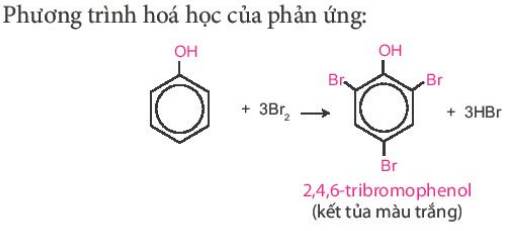
Tham khảo:
- Hiện tượng: Nước bromine mất màu và xuất hiện kết tủa trắng.
- Giải thích: Phenol phản ứng bromine, làm nước bromine mất màu, tạo kết tủa trắng 2,4,6-tribromophenol.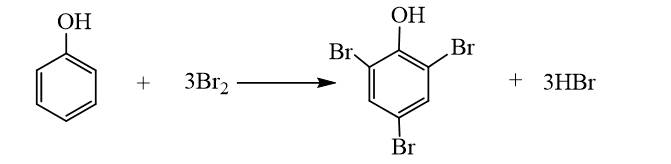
Hiện tượng:
-Nước brom mất màu
-Xuất hiện kết tủa trắng
Giải thích: Khi phenol phản ứng với brom thì sẽ làm mất màu nước brom và sẽ tạo ra kết tủa trắng 2,4,6-tribromophenol
nêu hiện tượng và viết phương trình hóa học xảy ra trong thí nghiệm sau:
- Nhỏ vài giọt dung dịch đồng sunfat vào ống nghiệm đựng dung dịch natri hidroxit
- Nhỏ vài giọt dung dịch H2SO4 vào ống nghiệm đụng Cu(OH)2
-Ngâm 1 đoạn dây đồng vào dung dịch AgNO3
- Nhỏ vài giọt dung dịch Bariclorua vào ống nghiệm đựng dung dịch natrisunfat
- Nhỏ vài giọt dung dịch đồng sunfat vào ống nghiệm đựng dung dịch natri hidroxit
Hiện tượng: xuất hiện chất không tan màu xanh
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
- Nhỏ vài giọt dung dịch H2SO4 vào ống nghiệm đụng Cu(OH)2
Hiện tượng:Chất rắn màu xanh lam tan dần, tạo thành dung dịch màu xanh lam.
\(Cu\left(OH\right)_2+H_2SO_4\rightarrow CuSO_4+2H_2O\)
-Ngâm 1 đoạn dây đồng vào dung dịch AgNO3
Hiện tượng:Có kim loại màu xác bám ngoài dây đồng. Dung dịch ban đầu không màu chuyển dần sang màu xanh. Đồng đã đẩy bạc ra khỏi dung dịch Bạc Nitrat và một phần đồng bị hoà tan tạo ra dung dịch Đồng Nitrat màu xanh lam
\(Cu+2AgNO_3\rightarrow2Ag+Cu\left(NO_3\right)_2\)
- Nhỏ vài giọt dung dịch Bariclorua vào ống nghiệm đựng dung dịch natrisunfat
Hiện tượng:Xuất hiện kết tủa trắng bari sunfat trong dung dịch.\(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\)( Có tham khảo trên mạng :< )
Nêu hiện tượng quan sát được, giải thích và viết phương trình hóa học của các phản ứng xảy ra trong ba thí nghiệm trên
Thí nghiệm 1
- Hiện tượng
Miếng Na tan dần.
Có khí thoát ra.
Miếng giấy lọc có tẩm phenolphtalein đổi thành màu đỏ.
- Phương trình hóa học: 2Na + H2O → 2NaOH + H2.
- Giải thích: Do Na phản ứng rất mạnh với nước tạo dung dịch bazo làm phenol chuyển hồng, phản ứng giải phóng khí H2.
Thí nghiệm 2
- Hiện tượng: Mẩu vôi nhão ra và tan dần
Phản ứng tỏa nhiều nhiệt.
Dung dịch đổi quỳ tím thành màu xanh (nếu dùng phenolphtalein thì đổi thành màu đỏ)
- Phương trình hóa học: CaO + H2O → Ca(OH)2.
- Giải thích: CaO tan trong nước tạo dung dịch Ca(OH)2 có tính bazo làm quỳ tím chuyển xanh (phenolphtalein chuyển hồng), phản ứng tỏa nhiệt.
Thí nghiệm 3
- Hiện tượng: Photpho cháy sáng.
Có khói màu trắng tạo thành.
Sau khi lắc khói màu trắng tan hết.
Dung dịch làm quỳ tím chuyển thành màu đỏ.
4P + 5O2 → 2P2O5
P2O5 + 3H2O → 2H3PO4.
- Giải thích:
Photpho đỏ phản ứng mạnh với khí Oxi tạo khói trắng là P2O5. P2O5 là oxit axit, tan trong nước tạo dung dịch axit H3PO4 là quỳ tím chuyển đỏ.
Tiến hành Thí nghiệm 1, quan sát khả năng hoàn tan của phenol trong nước. Nêu hiện tượng và giải thích kết quả thí nghiệm.


Tham khảo:
- Phenol ít tan trong nước lạnh.
- Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt.
- Giải thích: Phenol phản ứng với dung dịch sodium hydroxide tạo thành dung dịch muối tan trong suốt sodium phenolate (C6H5ONa).
C6H5OH + NaOH → C6H5ONa + H2O
Hiện tượng: Dung dịch ở dạng huyền phù, màu trắng đục tan thành dung dịch trong suốt
Giải thích: Phenol khi tác dụng với NaOH sẽ cho ra dung dịch muối tan trong suốt là C6H5ONa
*Thí nghiệm 1:
+) Hiện tượng: Xuất hiện chất rắn màu đỏ, dd màu xanh nhạt dần
+) PTHH: \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
*Thí nghiệm 2
+) Hiện tượng: Xuất hiện kết tủa trắng
+) PTHH: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\downarrow\)
*Thí nghiệm 3
a) Hiện tượng: Xuất hiện kết tủa trắng
PTHH: \(AgNO_3+HCl\rightarrow HNO_3+AgCl\downarrow\)
b) Hiện tượng: Chất rắn tan dần, sủi bọt khí
PTHH: \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
*Thí nghiệm 4: Xem lại đề
*Thí nghiệm 5
+) Hiện tượng: Chất rắn tan dần, dd chuyển sang màu xanh lá cây
+) PTHH: \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
*Thí nghiệm 6
+) Hiện tượng: Kẽm tan dần, xuất hiện khí
+) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
*Thí nghiệm 7
+) Hiện tượng: Nhôm tan dần, xuất hiện khí
+) PTHH: \(Al+NaOH+H_2O\underrightarrow{t^o}NaAlO_2+\dfrac{3}{2}H_2\uparrow\)
Tìm hiểu khả năng dẫn điện của vật liệu
Hãy quan sát hiện tượng khi thực hiện thí nghiệm và điền kết quả quan sát được theo mẫu sau:

Vật liệu | Bóng đèn sáng hay không sáng | Vật liệu dẫn điện hay không dẫn điện |
Kim loại | Sáng | Dân điện |
Nhựa | Không sáng | Không dẫn điện |
Gỗ | Không sáng | Không dẫn điện |
Cao su | Không sáng | Không dẫn điện |
Thủy tinh | Không sáng | Không dẫn điện |
Gốm | Không sáng | Không dẫn điện |