Hãy viết các phương trình hoá học để chứng minh các aldehyde vừa có tính oxi hoá, vừa có tính khử.

Những câu hỏi liên quan
Viết PTHH chứng minh : a, tính oxi hoá của các halogen giảm dần từ F2 đến I2 b, HCL vừa có tính khử , vừa có tính oxi hoá c, HF có khả năng ăn mòn thuỷ tinh
a)
- F2 tác dụng với H2 ở nhiệt độ thấp, trong bóng tối
\(H_2+F_2\underrightarrow{-252^oC}2HF\)
- Cl2 tác dụng với H2 ở nhiệt độ thường, có ánh sáng
\(H_2+Cl_2\underrightarrow{as}2HCl\)
- Br2 tác dụng với H2 ở nhiệt độ cao
\(Br_2+H_2\underrightarrow{t^o}2HBr\)
- I2 tác dụng với H2 ở nhiệt độ cao, có xúc tác
\(I_2+H_2\xrightarrow[Pt]{350-500^oC}2HI\)
=> Tính oxh giảm dần từ F2 đến I2
b)
- HCl có tính khử: \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
- HCl có tính oxh: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
c)
- \(SiO_2+4HF\rightarrow SiF_4+2H_2O\)
Đúng 2
Bình luận (0)
Viết các phương trình hóa học để chứng tỏ rằng, anđehit vừa có tính oxi hóa vừa có tính khử.
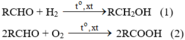
Trong (1), anđehit đóng vai trò là chất oxi hoá
Trong (2), anđehit đóng vai trò là chất khử.
Đúng 0
Bình luận (0)
Viết các phương trình phản ứng để chứng minh:
- Kim loại kiềm có tính khử mạnh, tính khử tăng dần khi đi từ Li đến Cs.
- Ion Fe2+ có cả tính oxi hoá, có cả tính khử.
- Ion Fe3+ có tính oxi hóa.
- Kim loại kiềm có tính khử mạnh, tính khử tăng dần khi đi từ Li đến Cs.
=> Xét pứ vs nước và phi kim em nhé
- Ion Fe2+ có cả tính oxi hoá, có cả tính khử.
=>Xét pứ Cu
Fe2++Cuo->Fe0+Cu+2
, Axit đặc
Fe2++H++NO3-2->Fe+3+NO+H2O
- Ion Fe3+ có tính oxi hóa.
=>Xét pứ td vs Fe
Fe+3+Fe0->Fe+2
Đúng 0
Bình luận (0)
Cho các chất và tính chất sau:
(1) S(r) (2) SO2 (k) (3) H2S (k) (4) H2SO4 (dd)
(a). Hợp chất có tính axit và tính oxi hoá mạnh (b). Hợp chất chỉ có tính khử. (c). Đơn chất vừa có tính khử vừa có tính oxi hoá. (d). Hợp chất vừa có tính oxi hoá vừa có tính khử
Hãy ghép cặp chất với tính chất phù hợp: A. (1)-d, (2)-a, (3)-b, (4)-c. B. (1)-c, (2)-a, (3)-b, (4)-d. C. (1)-c, (2)-b, (3)-a, (4)-c. D. (1)-c, (2)-d, (3)-b, (4)-a
Đọc tiếp
Cho các chất và tính chất sau:
| (1) S(r) (2) SO2 (k) (3) H2S (k) (4) H2SO4 (dd) |
(a). Hợp chất có tính axit và tính oxi hoá mạnh (b). Hợp chất chỉ có tính khử. (c). Đơn chất vừa có tính khử vừa có tính oxi hoá. (d). Hợp chất vừa có tính oxi hoá vừa có tính khử |
Hãy ghép cặp chất với tính chất phù hợp:
A. (1)-d, (2)-a, (3)-b, (4)-c.
B. (1)-c, (2)-a, (3)-b, (4)-d.
C. (1)-c, (2)-b, (3)-a, (4)-c.
D. (1)-c, (2)-d, (3)-b, (4)-a
Đáp án D
S là đơn chất vừa có tính khử vừa có tính oxi hoá => (1) – (c)
SO2 là hợp chất vừa có tính oxi hoá vừa có tính khử => (2) – (d)
H2S là hợp chất chỉ có tính khử => (3) – (b)
H2SO4 là hợp chất có tính axit và tính oxi hoá mạnh => (40) – (a)
Đúng 0
Bình luận (0)
Câu nào sau đây diễn tả đúng tính chất hoá học của lưu huỳnh ?
A. Lưu huỳnh chỉ có tính oxi hoá.
B. Lưu huỳnh chỉ có tính khử.
C. Lưu huỳnh vừa có tính oxi hoá, vừa có tính khử.
D. Lưu huỳnh không cố tính oxi hoá và không có tính khử.
Câu nào sau đây diễn tả đúng tính chất hoá học của lưu huỳnh ?
A. Lưu huỳnh chỉ có tính oxi hoá.
B. Lưu huỳnh chỉ có tính khử.
C. Lưu huỳnh vừa có tính oxi hoá, vừa có tính khử.
D. Lưu huỳnh không cố tính oxi hoá và không có tính khử.
Dãy gồm các chất vừa có tính khử vừa có tính oxi hoá là A. Fe, Fe3O4. B. FeO, FeCl2. C. Fe, Fe(OH)2. D. FeSO4, Fe2(SO4)3.
Đọc tiếp
Dãy gồm các chất vừa có tính khử vừa có tính oxi hoá là
A. Fe, Fe3O4.
B. FeO, FeCl2.
C. Fe, Fe(OH)2.
D. FeSO4, Fe2(SO4)3.
Đáp án B
Fe có số oxi hóa cao nhất là +3, thấp nhất là 0 => Các hợp chất sắt II vừa có tính khử vừa có tính oxi hoá
Vậy FeO và FeCl2 vừa có tính khử và tính oxi hóa.
Đúng 0
Bình luận (0)
Bài 2:1. Viết 2 phương trình phản ứng chứng minh Clo có tính oxi hoá mạnh hơn brom và iot?2. Hãy dẫn ra những phản ứng hóa học để chứng minh rằng:a) Oxi và ozon đều có tính chất oxi hóa.b) Ozon có tính chất oxi hóa mạnh hơn oxi.3. Viết phương trình phản ứng của các nguyên tố halogen khi tác dụng với nước (ghi rõ điềukiện, nếu có) ?4. Từ Clo viết phương trình phản ứng điều chế nước Giaven và Clorua vôi?5. Muối ăn không những có tầm quan trọng trong đời sống hàng ngày của con người mà còn lànguyên...
Đọc tiếp
Bài 2:
1. Viết 2 phương trình phản ứng chứng minh Clo có tính oxi hoá mạnh hơn brom và iot?
2. Hãy dẫn ra những phản ứng hóa học để chứng minh rằng:
a) Oxi và ozon đều có tính chất oxi hóa.
b) Ozon có tính chất oxi hóa mạnh hơn oxi.
3. Viết phương trình phản ứng của các nguyên tố halogen khi tác dụng với nước (ghi rõ điều
kiện, nếu có) ?
4. Từ Clo viết phương trình phản ứng điều chế nước Giaven và Clorua vôi?
5. Muối ăn không những có tầm quan trọng trong đời sống hàng ngày của con người mà còn là
nguyên liệu để sản xuất NaOH. Viết phương trình hóa học của phản ứng sản xuất NaOH từ muối
ăn
6. Viết phương trình phản ứng chứng minh HF có thể ăn mòn thuỷ tinh và phương trình của Flo
tác dụng với nước?
Cl2 + 2NaBr --> 2NaCl + Br2
Cl2 +2NaI --->2 NaCl + I2
Đúng 0
Bình luận (0)
3) Viết phương trình phản ứng chứng minh – giải thích: HCl có tính oxi hóa. Cl2 vừa có tính khử, vừa có tính oxi hóa (1 phương trình).
Mg + 2HCl -> MgCl2 + H2
Mg có số oxi hoá ban đầu là 0 sau phản ứng lên +2, H có số oxi hoá ban đầu là +1 sau phản ứng còn 0 nên HCl thể hiện tính oxi hoá ở phương trình này
Cl2 + 2NaOH -> NaCl + NaClO + H2O
Cl2 ban đầu có số oxi hoá là 0,sau phản ứng ở NaCl có số oxi hoá là -1 chứng tỏ có tính oxi hoá, ở NaClO có số oxi hoá là +1 chứng tỏ có tính khử
Đúng 16
Bình luận (0)
Viết 2 phương trình chứng minh SO2 vừa có tính khử vừa có tính oxi hóa
\(SO_2+Br_2+2H_2O\rightarrow2HBr+H_2SO_4\) ( tính khử )
\(SO_2+2Mg\rightarrow\left(t^o\right)2MgO+S\) ( tính oxi hóa )
Đúng 3
Bình luận (0)




















