Dựa vào phương trình hóa học của phản ứng điều chế khí oxygen từ KMnO4, em hãy cho biết phản ứng có xảy ra theo chiều ngược lại được không?

Những câu hỏi liên quan
Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
Khi đốt nến (làm bằng parafin), nến cháy trong không khí (tác dụng với oxygen) tạo ra khí carbon dioxide và hơi nước.Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
Đọc tiếp
Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
Khi đốt nến (làm bằng parafin), nến cháy trong không khí (tác dụng với oxygen) tạo ra khí carbon dioxide và hơi nước.Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
Câu 31. Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra trong các quá trình sau. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.(a) Cồn cháy trong không khí (tác dụng với oxygen) tạo thành nước và khí carbon dioxide.(b) Hòa tan bột copper (II) oxide vào dung dịch hydrochloric acid không màu thu được dung dịch copper (II) chloride có màu xanh. Biết rằng sản phẩm của phản ứng còn có nước.(c) Thả mảnh nhôm (aluminium) vào dung dịch sulfuric acid t...
Đọc tiếp
Câu 31. Chỉ ra dấu hiệu cho thấy đã có phản ứng hóa học xảy ra trong các quá trình sau. Hãy viết phương trình chữ của phản ứng và xác định chất phản ứng, sản phẩm của các phản ứng.
(a) Cồn cháy trong không khí (tác dụng với oxygen) tạo thành nước và khí carbon dioxide.
(b) Hòa tan bột copper (II) oxide vào dung dịch hydrochloric acid không màu thu được dung dịch copper (II) chloride có màu xanh. Biết rằng sản phẩm của phản ứng còn có nước.
(c) Thả mảnh nhôm (aluminium) vào dung dịch sulfuric acid thu được dung dịch aluminium sulfate và thấy có sủi bọt khí (hydrogen).
(d) Nhỏ vài giọt barium chloride vào dung dịch sulfuric acid thấy xuất hiện chất kết tủa màu trắng (barium sulfate). Biết rằng sản phẩm của phản ứng còn có hydrochloric acid.
`#3107.101107`
Dấu hiệu:
(a): Có sự tỏa nhiệt, ánh sáng
(b): Có sự thay đổi về màu sắc
(c): Có sự tạo thành chất khí (sủi bọt khí)
(d): Tạo ra chất kết tủa (các chất không tan)
__________
(a):
PT chữ: Ethanol + Oxygen \(\underrightarrow{\text{ }\text{ }\text{ t}^0\text{ }\text{ }\text{ }}\) Carbon dioxide + Nước
Chất tham gia (chất pứ): Ethanol, Oxygen
Chất sản phẩm: Carbon dioxide, nước
(b):
PT chữ: Copper (II) Oxide + Hydrochloric acid \(\longrightarrow\) Copper (II) chloride + Nước
Chất tham gia: Copper (II) Oxide, hydrochloric acid
Chất sản phẩm: Copper (II) chloride, nước
(c):
PT chữ: Aluminium + Sulfuric acid \(\longrightarrow\) Aluminium sulfate + Hydrogen
Chất tham gia: Aluminium, sulfuric acid
Chất sản phẩm: Aluminium sulfate, hydrogen
(d):
PT chữ: Barium chloride + sulfuric acid \(\longrightarrow\) Barium sulfate + hydrochloric acid
Chất tham gia: Barium chloride, sulfuric acid
Chất sản phẩm: Barium sulfate, hydrochloric acid.
Đúng 2
Bình luận (0)
Từ các nguyên liệu có sẵn: quặng pyrit (FeS2), nước, không khí, dung dịch axit sunfuric loãng, em hãy viết các phương trình hóa học của phản ứng xảy ra để điều chế 2 sản phẩm muối sắt (II) sunfat và sắt (III) sunfat
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
$2H_2O \xrightarrow{đp} 2H_2 + O_2$
$2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3$
$SO_3 + H_2O \to H_2SO_4$
$Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O$
$Fe_2O_3 + 3H_2 \to 2Fe + 3H_2O$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,4g Sulfur trong không khí thu được 12,8g khí Sulfur dioxide
a) Viết phương trình hóa học phản ứng xảy ra
b) Cho biết tỉ lệ số nguyên tử , phân tử giữa các chất trong phản ứng
c) Áp dụng DLBTKL , hãy tính khối lượng khí Oxygen đã phản ứng
\(a.S+O_2\xrightarrow[]{t^0}SO_2 \)
b. Tỉ lệ 1 : 1 : 1
\(c:BTKL:m_S+m_{O_2}=m_{SO_2}\\ \Rightarrow m_{O_2}=m_{SO_2}-m_S\\ =12,8-6,4\\ =6,4g\)
Đúng 2
Bình luận (0)
Mn giúp em vớiCâu 1. Khi lò than cháy đã xảy ra phản ứng hóa học giữa cacbon và khí oxi trong không khí tạo ra khícacbonic.a) Viết phương trình chữ của phản ứng hóa học xảy ra.b) Điều kiện đế xảy ra phản ứng trên là gì?c) Dấu hiệu nào chứng tỏ có phản ứng hóa học xảy ra?d) Đề xuất phương án đế than cháy nhanh và hiệu quả hơn.Câu 2. Viết và đọc phương trình chữ của phản ứng hóa học xảy ra trong các quá trình sau:a) Thối hơi thở (chứa khí cacbonic) vào nước vôi trong (chứa canxi hiđroxit) thấy dun...
Đọc tiếp
Mn giúp em với
Câu 1. Khi lò than cháy đã xảy ra phản ứng hóa học giữa cacbon và khí oxi trong không khí tạo ra khí
cacbonic.
a) Viết phương trình chữ của phản ứng hóa học xảy ra.
b) Điều kiện đế xảy ra phản ứng trên là gì?
c) Dấu hiệu nào chứng tỏ có phản ứng hóa học xảy ra?
d) Đề xuất phương án đế than cháy nhanh và hiệu quả hơn.
Câu 2. Viết và đọc phương trình chữ của phản ứng hóa học xảy ra trong các quá trình sau:
a) Thối hơi thở (chứa khí cacbonic) vào nước vôi trong (chứa canxi hiđroxit) thấy dung dịch vấn đục
do tạo thành canxi cacbonat và nước.
b) Nước oxi già (hiđro peoxit) bị phân hủy thành nước và khí oxi.
c) Nung đá vôi (thành phần chính là canxi cacbonat) tạo thành vôi sống (thành phần chính là canxi
oxit) và khí cacbonic.
Đốt cháy hết 1,24 gam P trong không khí thu được doan pentoxide theo sơ đồ phản ứng: P + O, — » P,Os 1º Lập phương trình hóa học của phản ứng và tính: a. Khối lượng diphosphorus pentoxide tạo ra. b. Thể tích khí oxygen tham gia phản ứng ở điều kiện chuẩn.
PTHH: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
a) \(n_P=\dfrac{1,24}{31}=0,04\left(mol\right)\)
Theo PTHH: \(n_{P_2O_5}=\dfrac{0,04\cdot2}{4}=0,02\left(mol\right)\)
\(\Rightarrow m_{P_2O_5}=n_{P_2O_5}\cdot M_{P_2O_5}=0,02\cdot142=2,84\left(g\right)\)
b) Theo PTHH: \(n_{O_2}=\dfrac{0,04\cdot5}{4}=0,05\left(mol\right)\)
\(\Rightarrow V_{O_2\left(dkc\right)}=n_{O_2}\cdot24,79=0,05\cdot24,79=1,2395\left(l\right)\)
Đúng 3
Bình luận (0)
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điệ...
Đọc tiếp
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:
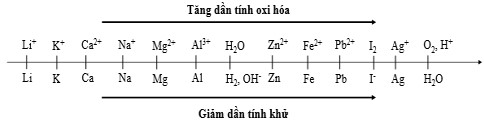
Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời P b N O 3 2 và M g N O 3 2 bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm, hãy cho biết
Bán phản ứng nào xảy ra ở catot
A. P b 2 + + 2 e → P b
B. M g 2 + + 2 e → M g
C. O 2 + 4 H + + 4 e → 2 H 2 O
D. H 2 O + 2 e → H 2 + 2 O H -
Nung thuốc tím (KMnO4) sau một thời gian người ta thu được chất rắn màu xanh tan được trong nước, chất rắn màu đen không tan và khí oxygen. Để khẳng định có phản ứng hóa học xảy ra, ta dựa vào dấu hiệu:
A. có sự thay đổi nhiệt độ.
B. có sự thay đổi màu sắc.
C. có chất khí sinh ra.
D. cả 2 dấu hiệu là thay đổi màu sắc và có chất khí sinh ra.
Oxi hóa không hoàn toàn etilen (có xúc tác) để điều chế anđehit axetic thu được hỗn hợp X. Dẫn 2,24 lít khí X (quy về đktc) vào một lượng dư dung dịch bạc nitrat trong NH3 đến khi phản ứng hoàn toàn thấy có 16,2 gam bạc kết tủa.
Viết phương trình hóa học của các phản ứng xảy ra
Phương trình phản ứng:
2CH2=CH2 + O2 → 2CH3CHO (1)
Hỗn hợp X gồm: CH2=CH2 và CH3CHO
CH3CHO + H2O + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag↓ + 2NH4NO3 (2)
Đúng 0
Bình luận (0)



















