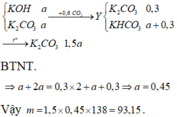Hấp thụ hết 2,688 lit CO2 (đktc) vào cốc đựng 150 gam dung dịch KOH a% thu được 11,4 gam muối. Tính a và nồng độ % các chất trong dung dịch thu được sau phản ứng.

Những câu hỏi liên quan
: Hấp thụ hết 2,464 lit CO2 (đktc) vào cốc đựng dung dịch KOH 1,5M. Tính V và nồng độ mol các chất trong dung dịch thu được sau phản ứng khi:
a) Tính thể tích dd KOH tối thiểu cần dùng để hấp thụ hết lượng CO2 trên
b) Tính thể tích dd KOH tối đa cần dùng để hấp thụ hết lượng CO2 trên.
c) Tính thể tích dd KOH để thu được 13,85 gam muối.
nCO2= 2,464/22,4= 0,11(mol)
a) PTHH: KOH + CO2 -> KHCO3
nKHCO3=nKOH= nCO2 = 0,11(mol) => VddKOH(min)= 0,11/1,5=11/150(l)\(\approx\)0,073(l)
b) 2 KOH + CO2 -> K2CO3 + H2O
nKOH=2.nCO2= 0,22(mol)
=> VddKOH(max)= 0,22/1.5= 11/75(l)\(\approx\) 0,147(l)
c) 2 KOH + CO2 -> K2CO3 + H2O
x__________0,5x__0,5x(mol)
KOH + CO2 -> KHCO3
y___y___________y(mol)
Ta có:
nCO2(tổng)=0,11 <=> 0,5x+y=0,11 (a)
Mặt khác: m(muối)= 13,85
<=> mK2CO3+mKHCO3=13,85
<=> 138.0,5x+100.y=13,85
<=> 79x+100y=13,85 (b)
Từ (a), (b), ta được hpt:
\(\left\{{}\begin{matrix}0,5x+y=0,11\\79x+100y=13,85\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=\frac{57}{580}\\y=\frac{353}{5800}\end{matrix}\right.\)
=> \(V_{ddKOH}=\frac{\frac{57}{580}+\frac{353}{5800}}{1,5}\approx0,106\left(l\right)\)
Hấp thụ hết 2,296 lit Co2(đktc)vào cốc đựng 100gam dung dịch NAOHa% hu được 9,435 gam muối. Tính a và nồng dô % các chất trong dung dịch sau phan ứng
Muối có thể có NaHCO3, hoặc Na2CO3 hoặc cả hai
Đặt số mol NaHCO3, Na2CO3 lần lượt là x,y(mol)
Theo đề ta có hệ phương trình:
\(\left\{{}\begin{matrix}x+y=0,1025\\84x+106y=9,435\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,065\left(mol\right)\\y=0,0375\left(mol\right)\end{matrix}\right.\)
BT Na: \(\dfrac{100.a\%}{40.100\%}=0,065+0,0375.2\Rightarrow a=5,6\)
\(C\%_{NaHCO_3}=\dfrac{0,065.84}{100}.100\%=5,46\%\)
\(C\%_{Na_2CO_3}=\dfrac{106.0,0375}{100}.100\%=3,975\%\)
Đúng 1
Bình luận (0)
HOÁ --- bài 2: Hấp thụ hết 3,36 lít CO2 (đktc) vào cốc đựng V ml dd NaOH 1,2M thu được 26,85 gam muối . Tính V và nồng độ mol các chất trong dd sau phản ứng
nCO2=0,15mol
nNa2CO3=0,25mol
PTHH: CO2+2NaOH=>Na2CO3 + H2O
0,15: 0,25 =>nNa2CO3 dư
p/ư: 0,15----0,3---------->0,15
=>V=0,3:1,2=0.25lit
=> CM(Na2CO3)=0,15:0,25=0,6M
Đúng 0
Bình luận (0)
hấp thụ hết 6,72 lit CO2 vào 500 ml dung dịch NaOH 1M thu được dung dịch X. Cho X vào dung dịch BaCl2 dư thu được m gam kết tủa. Tính nồng độ mol các chất trong X và m
Ta có:
nCO2=6,72\22,4=0,3 mol
;nNaOH=0,5.1=0,5
Ta có:
nNaOHnCO2=0,5\0,3=1,67
Nên phản ứng tạo ra 2 muối
2NaOH+CO2→Na2CO3+H2O
NaOH+CO2→NaHCO3
Ta có:
nNa2CO3=nNaOH−nCO2=0,5−0,3=0,2 mol;
nNaHCO3=0,3−0,2=0,1 mol
→CM Na2CO3=0,20,5=0,4M;CM NaHCO3=0,10,5=0,2M
BaCl2+Na2CO3→BaCO3+2NaCl
→nBaCO3=nNa2CO3=0,2 mol
→m=mBaCO3=0,2.197=39,4 gam
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn V lit CO2(ở đktc) vào bình đựng 200ml dung dịch NaOH -1M và Na2CO3 -0,5M .Cô cạn dung dịch sau phản ứng thu được 19,9 gam chất rắn khan. Giá trị V là A. 1,12 B. 4,48 C. 2,24 D. 3,36
Đọc tiếp
Hấp thụ hoàn toàn V lit CO2(ở đktc) vào bình đựng 200ml dung dịch NaOH -1M và Na2CO3 -0,5M .Cô cạn dung dịch sau phản ứng thu được 19,9 gam chất rắn khan. Giá trị V là
A. 1,12
B. 4,48
C. 2,24
D. 3,36
Hấp thụ hết 13,44 lít CO2 (đktc) vào 1 lít dung dịch chứa KOH aM và K2CO3 aM thu được dung dịch Y. Cho Y tác dụng hết với dung dịch BaCl2 dư thu được 59,1 gam kết tủa. Đun sôi đến cạn dung dịch Y thu được m gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là A. 116,4 B. 161,4 C. 93,15 D. 114,6
Đọc tiếp
Hấp thụ hết 13,44 lít CO2 (đktc) vào 1 lít dung dịch chứa KOH aM và K2CO3 aM thu được dung dịch Y. Cho Y tác dụng hết với dung dịch BaCl2 dư thu được 59,1 gam kết tủa. Đun sôi đến cạn dung dịch Y thu được m gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 116,4
B. 161,4
C. 93,15
D. 114,6
Hấp thụ hết 2,24 lit CO2 vào cốc đựng 200 ml dung dịch Ba(OH)2 aM thu được 5,94 gam kết tủa và dung dịch A. Lọc kết tủa, đun nóng dung dịch A lại thu thêm được m gam kết tủa nữa. Tìm a và m.
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{BaCO_3}=\dfrac{5,91}{197}=0,03\left(mol\right)\)
Đun nóng dung dịch A lại thu được kết tủa, chứng tỏ A có \(Ba\left(HCO_3\right)_2\)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\\ Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
Ta có:
\(n_{BaCO_3}+2n_{Ba\left(HCO_3\right)_2}=n_{CO_2}\\ \Rightarrow n_{Ba\left(HCO_3\right)_2}=\dfrac{0,1-0,03}{2}=0,035\left(mol\right)\\ n_{Ba\left(OH\right)_2}=n_{BaCO_3}+n_{Ba\left(HCO_3\right)_2}=0,035+0,03=0,065\left(mol\right)\\ \Rightarrow a=\dfrac{0,065}{2}=0,325M\)
\(Ba\left(HCO_3\right)_2\rightarrow BaCO_3+CO_2+H_2O\)
\(n_{BaCO_3}=n_{Ba\left(HCO_3\right)_2}=0,035\left(mol\right)\\ \Rightarrow m=0,035\cdot197=6,895\left(g\right)\)
Đúng 6
Bình luận (0)
. Hấp thụ hoàn toàn 0,896 lit khí CO2 ở đktc qua 500 ml dung dịch Ca(OH)2 nồng độ xM, sau phản ứng thu được 3 gam kết tủa và dung dịch A. Tìm giá trị của X
. Hấp thụ hoàn toàn 0,896 lit khí CO2 ở đktc qua 500 ml dung dịch Ca(OH)2 nồng độ xM, sau phản ứng thu được 3 gam kết tủa và dung dịch A. Tìm giá trị của X
Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\\n_{CaCO_3}=\dfrac{3}{100}=0,03\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo 2 muối
PTHH: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\) (1)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\) (2)
Theo PTHH: \(n_{Ca\left(OH\right)_2\left(1\right)}=n_{CaCO_3}=0,03\left(mol\right)=n_{CO_2\left(1\right)}\)
\(\Rightarrow n_{CO_2\left(2\right)}=0,04-0,03=0,01\left(mol\right)\) \(\Rightarrow n_{Ca\left(OH\right)_2\left(2\right)}=0,005\left(mol\right)\)
\(\Rightarrow\Sigma n_{Ca\left(OH\right)_2}=0,03+0,005=0,035\left(mol\right)\) \(\Rightarrow x=C_{M_{Ca\left(OH\right)_2}}=\dfrac{0,035}{0,5}=0,07\left(M\right)\)
Đúng 2
Bình luận (0)
Ta có: \(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{3}{100}=0,03\left(mol\right)\)
PTHH: CO2 + Ca(OH)2 ---> CaCO3↓ + H2O
Ta thấy: \(\dfrac{0,04}{1}>\dfrac{0,03}{1}\)
Vậy CO2 dư.
Theo PT: \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}=0,03\left(mol\right)\)
Đổi 500ml = 0,5 lít.
=> \(C_{M_{Ca\left(OH\right)_2}}=x=\dfrac{0,03}{0,5}=0,06M\)
Đúng 0
Bình luận (3)