Hoà tan hoàn toàn một kim loại R trong dung dịch HCl 7,3 % sau phản ứng thì thu được dung dịch muối có nồng độ là 12,79 % . Xác định R ?

Những câu hỏi liên quan
Hòa tan 14,4 gam kim loại R hóa trị II trong dung dịch HCl 29,2%. Sau khi phản ứng hoàn toàn thu được dung dịch mới có nồng độ HCl 5,456% và nồng độ muối clorua là 28,401%. Xác định kim loại R.
Hoà tan hoàn toàn 6,5g một kim loại chưa rõ hoá trị bằng dung dịch HCl 7,3% vừa đủ thu
được dung dịch muối và 2,24 lít khí (đktc).
a. Xác định kim loại.
b. Tính khối lượng dung dịch HCl đã dùng.
c. Xác định nồng độ % của dung dịch muối thu được.
a) $2R + 2nHCl \to 2RCl_n + nH_2$
Theo PTHH :
$n_R = \dfrac{2}{n}.n_{H_2} = \dfrac{0,2}{n}(mol)$
$\Rightarrow \dfrac{0,2}{n}.R = 6,5 \Rightarrow R= \dfrac{65}{2}n$
Với n = 2 thì R = 65(Zn)
Vậy kim loại cần tìm là Zn
b)
$n_{HCl} = 2n_{H_2} = 0,2(mol)$
$m_{dd\ HCl} = \dfrac{0,2.36,5}{7,3\%} = 100(gam)$
c)
Sau phản ứng :
$m_{dd} = 6,5 + 100 - 0,1.2 = 106,3(gam)$
$C\%_{ZnCl_2} = \dfrac{0,1.136}{106,3}.100\% = 12,8\%$
Đúng 3
Bình luận (0)
hoà tan hoàn toàn 4,8 g một kim loại R( có hoá trị I ,II,III ) cần dùng vừa đủ một lượng dung dịch HCl 10% . phản ứng kết thúc thấy khối lượng dung dịch tăng 4,4g
a)xác định R
b) tính nồng độ % muối thu đc
a, Giả sử R có hóa trị n.
PT: \(2R+2nHCl\rightarrow2RCl_n+nH_2\)
Ta có: \(n_R=\dfrac{4,8}{M_R}\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{n}{2}n_R=\dfrac{2,4n}{M_R}\left(mol\right)\)
Mà: m dd tăng = mR - mH2 \(\Rightarrow4,4=4,8-\dfrac{2,4n}{M_R}.2\Rightarrow M_R=12n\left(g/mol\right)\)
Với n = 2, MR = 24 (g/mol) là thỏa mãn.
Vậy: R là Mg.
b, Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
_____0,2_____0,4____0,2_____0,2 (mol)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\Rightarrow m_{ddHCl}=\dfrac{14,6}{10\%}=146\left(g\right)\)
Có: m dd sau pư = 4,8 + 146 - 0,2.2 = 150,4 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{0,2.136}{150,4}.100\%\approx18,085\%\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn một hiđroxit của kim loại R bằng dung dịch HCl 14,6% (vừa đủ), sau phản ứng thu được dung dịch chứa muối clorua có nồng độ 17,03%. Công thức hiđroxit của kim loại R là A. Mg(O
H
)
2
B. Cu(O
H
)
2
C. Zn(O
H
)
2
D. Fe(O
H
)
3
Đọc tiếp
Hòa tan hoàn toàn một hiđroxit của kim loại R bằng dung dịch HCl 14,6% (vừa đủ), sau phản ứng thu được dung dịch chứa muối clorua có nồng độ 17,03%. Công thức hiđroxit của kim loại R là
A. Mg(O H ) 2
B. Cu(O H ) 2
C. Zn(O H ) 2
D. Fe(O H ) 3
Chọn A

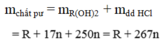
Vì phản ứng không sinh ra chất khí hay kết tủa
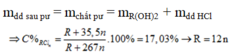
Vậy n = 2, R = 24 g/mol thỏa mãn, chất cần tìm là M g O H 2 .
Đúng 0
Bình luận (0)
Hoà tan 0.54 gam kim loại R (có hoá trị III trong hợp chất) bằng 50ml dung dịch HCl 2M. Sau phản ứng thu được 0.672 lít khí (ở đktc) a. Xác định kim loại R b. Tính nồng độ mol của dung dịch thu được sau phản ứng.
mik sửa lại cái dưới bị lỗi latex
\(a.n_{HCl}=0,05.2=0,1\left(mol\right);n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ 2R+6HCl\rightarrow2RCl_3+3H_2\\ \Rightarrow\dfrac{0,1}{6}>\dfrac{0,03}{3}\Rightarrow HCl.dư,R.pư.hết\\ n_R=0,03.2:3=0,02\left(mol\right)\\ M_R=\dfrac{0,54}{0,02}=27\left(g/mol\right)\\ \Rightarrow R=27\left(Al,nhôm\right)\\ b.C_{M_{AlCl_3}}=\dfrac{0,3.2:3}{0,05}=0,4M\\ C_{M_{HCl\left(dư\right)}}=\dfrac{0,1-\left(0,3.6:3\right)}{0,05}=0,8M\)
Đúng 3
Bình luận (2)
\(a.n_{HCl}=0,05.2=0,1\left(mol\right)\\ n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ 2R+6HCl\rightarrow2RCl_3+3H_2\\ \Rightarrow\dfrac{0,1}{6}>\dfrac{0,03}{3}\Rightarrow HCl.dư,R.pư.hết\\ n_R=0,03.2:3=0,02\left(mol\right)\\ M_R=\dfrac{0,54}{0,02}=27\left(g/mol\right)\\ \Rightarrow R=27\left(Al,nhôm\right)\\ b.n_{AlCl_3}=n_{Al}=0,02mol\\ C_{M_{AlCl_3}}=\dfrac{0,02}{0,05}=0,4M\\ C_M_{HCl\left(dư\right)}=\dfrac{0,1-\left(0,03.2\right)}{0,05}=0,8M\)
Đúng 0
Bình luận (0)
\(2R+6HCl\rightarrow2RCl_3+3H_2\)
TPT: 2 6 2 3 (mol)
TĐB: 0,02 0,1 0,02 0,03 (mol)
PƯ: 0,02 0,06 0,02 0,03 (mol)
Dư: 0 0,04 0 0 (mol)
50ml = 0,05 lít
\(n_{HCl}=C_M.V_{dd}=2.0,05=0,1\left(mol\right)\)
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Tỉ lệ: \(\dfrac{n_{HCl}}{6}=\dfrac{0,1}{6}>\dfrac{n_{H_2}}{3}=\dfrac{0,03}{3}\)\(\Rightarrow n_{HCl}\) dư
\(m_R=n.M\)
\(\Leftrightarrow0,54=0,02R\)
\(\Leftrightarrow R=27\)
Vậy kim loại R là Al (III)
\(RCl_3\) là \(AlCl_3\)
Sau phản ứng còn \(AlCl_3\) và 0,04 mol \(HCl\)
\(C_{M_{HCl\left(dư\right)}}=\dfrac{n}{V_{dd}}=\dfrac{0,04}{0,05}=0,8\left(M\right)\)
\(C_{M_{AlCl_3}}=\dfrac{n}{V_{dd}}=\dfrac{0,02}{0,05}=0,4\left(M\right)\)
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn 4,8 gam một kim loại R có hóa trị II vào 100 ml dung dịch HCl 5M. Sau phản ứng thu được 4,48 lít khí (đktc) và dung dịch A. Xác định R và tính nồng độ mol/lít các chất có trong dung dịch A.
PTHH: R + 2HCl ---> RCl2 + H2 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{100}{1000}.5=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
Vậy HCl dư.
Theo PT(1): \(n_R=n_{H_2}=0,2\left(mol\right)\)
=> \(M_R=\dfrac{4,8}{0,2}=24\left(g\right)\)
Vậy R là magie (Mg)
PT: Mg + 2HCl ---> MgCl2 + H2 (2)
Ta có: \(m_{dd_{MgCl_2}}=4,8+\dfrac{100}{1000}-0,2.2=4,5\left(lít\right)\)
Theo PT(2): \(n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,2}{4,5}=\dfrac{2}{45}M\)
Đúng 0
Bình luận (0)
Cho 51,75g kim loại R (hóa trị II) vào 200g dung dịch CuSO4 16%, sau khi phản ứng xảy ra hoàn toàn thì thu được dung dịch X và 51,55g hỗn hợp kim loại. Xác định kim loại R và tính nồng độ phần trăm của chất tan có trong X
Xem chi tiết
PTHH: \(R+CuSO_4\rightarrow RSO_4+Cu\)
Ta có: \(n_{CuSO_4}=\dfrac{200\cdot16\%}{160}=0,2\left(mol\right)=n_{Cu}=n_R\)
\(\Rightarrow m_{Cu}=0,2\cdot64=12,8\left(g\right)\)
Theo bài ra, ta có: mhỗn hợp = mR ban đầu - mR pư + mCu
\(\Rightarrow51,75-m_{R\left(pư\right)}+12,8=51,55\left(g\right)\)
\(\Rightarrow m_{R\left(pư\right)}=13\left(g\right)\) \(\Rightarrow M_R=\dfrac{13}{0,2}=65\) \(\Rightarrow\) R là Kẽm
Mặt khác: \(m_{dd}=m_{R\left(bđ\right)}+m_{ddCuSO_4}-m_{Cu}-m_{Zn\left(dư\right)}=225,95\left(g\right)\)
\(\Rightarrow C\%_{ZnSO_4}=\dfrac{0,2\cdot161}{225,95}\cdot100\%\approx14,25\%\)
Đúng 1
Bình luận (0)
hoà tan oxit ro và dung dịch hcl 14,6% vừa đủ, thu được dung dịch muối có nồng độ 17,592%. xác định kim loại r
PT: \(RO+2HCl\rightarrow RCl_2+H_2O\)
Gọi: mRO = a (g)
\(\Rightarrow n_{RO}=\dfrac{a}{M_R+16}\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{HCl}=2n_{RO}=\dfrac{2a}{M_R+16}\left(mol\right)\\n_{RCl_2}=n_{RO}=\dfrac{a}{M_R+16}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{HCl}=\dfrac{2a}{M_R+16}.36,5=\dfrac{73a}{M_R+16}\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{\dfrac{73a}{M_R+16}}{14,6\%}=\dfrac{500a}{M_R+16}\left(g\right)\)
⇒ m dd sau pư = \(a+\dfrac{500a}{M_R+16}\left(g\right)\)
Mà: \(m_{RCl_2}=\dfrac{a}{M_R+16}.\left(M_R+71\right)\left(g\right)\)
\(\Rightarrow\dfrac{\dfrac{a}{M_R+16}.\left(M_R+71\right)}{a+\dfrac{500a}{M_R+16}}=0,17592\)
\(\Rightarrow M_R=24\left(g/mol\right)\)
→ R là Mg.
Đúng 1
Bình luận (0)
hoà tan một muối cacbonat của kim loại R ( chưa biết hoá trị ) trong một lượng vừa đủ dung dịch H2SO4 12,25% thu được dung dịch muối sunfat của kim loại R có nồng độ 17,431%. Xác định kim loại R
tham khảo
Coi mdd H2SO4=100(gam)mdd H2SO4=100(gam)
nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)
Sau phản ứng ,
mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)
Đúng 0
Bình luận (0)

























