cho 37,6g hh gồm các oxide gồm CuO , CaO , Fe2O3 tác dụng vừa đủ với 0,6 lít dd HCL 2M , cô cạn dung dịch sau phản ứng thì số gam muối khan thu được là ?
Cho 37,6 gam hỗn hợp gồm CaO, CuO và Fe2O3 tác dụng vừa đủ với 0,6 lít dung dịch HCl 2M, rồi cô cạn dung dịch sau phản ứng thì số gam muối khan thu được là
A. 70,6
B. 61,0
C. 80,2
D. 49,3
Đáp án A
nHCl = 1,2 (mol)
Oxit + 2HCl →Muối + H2O
1,2 → 0,6 (mol)
Bảo toàn khối lượng:
moxit + m HCl = m muối + m nước
37,6 + 1,2.36,5 = m muối + 0,6.18
mmuối = 70,6 (g)
Cho 37,6 gam hỗn hợp gồm CaO, CuO và Fe2O3 tác dụng vừa đủ với 0,6 lít dung dịch HCl 2M, rồi cô cạn dung dịch sau phản ứng thì số gam muối khan thu được là
A. 80,2.
B. 70,6.
C. 49,3
D. 61,0
Cho 37,6g hh gồm CaO, CuO và Fe2O3 tác dụng vừa đủ vs 0,6 lít dd HCl 2M, rồi cô cạn dd sau phản ứng thì số gam muối khan thu đc là
\(n_{HCl}=C_{MHCl}.m_{ddHCl}=2.0,6=1,2\left(mol\right)\)
-> \(m_{HCl}=n_{HCl}.M_{HCl}=1,2.\left(1+35,5\right)=43,8\left(g\right)\)
Mà \(n_{\left(H\right)}=n_{HCl}\)
-> \(n_{\left(H\right)}=1,2\left(mol\right)\)
-> \(n_{H_2O}=\frac{1}{2}n_{\left(H\right)}=\frac{1}{2}.1,2=0,6\left(mol\right)\)
-> \(m_{H_2O}=n_{H_2O}.M_{H_2O}=0,6.18=10,8\left(g\right)\)
- Áp dụng định luật bảo toàn khối lượng :
\(m_{hh}+m_{HCl}=m_{H_2O}+\) mMuối
=> mMuối = \(m_{hh}+m_{HCl}-m_{H_2O}\)
=> mMuối = 37,6 + 43,8 - 10,8 = 70,6 ( g )
Vậy lượng muối khan sau khi cô cạn dung dịch là 70,6 gam .
nHCl=2.0,6=1,2(mol)
-> mHCl=1,2.(1+35,5)=43,8(g)
Mà n(H)=nHCl
> n(H)=1,2(mol)=1\2.1,2=0,6(mol)
-> mH2O=0,6.18=10,8(g)
- Áp dụng định luật bảo toàn khối lượng :
mhh+mHCl=mH2O+mhh+mHCl=mH2O+ mMuối
> mMuối = mhh+mHCl−mH2O
> mMuối = 37,6 + 43,8 - 10,8 = 70,6 ( g )
Vậy lượng muối khan sau khi cô cạn dung dịch là 70,6 gam .
cho 37,6 g hỗn hợp gồm CaO,CuO,Fe2O3 tác dụng vừa đủ với 0,6 lít dung dịch HCl 2M, rồi cô cạn dung dịch sau phản ứng thì số gam muối khan thu được là ?
hh (CaO,CuO,Fe2O3)+2HCl->muoi+H2O
co so mol HCl=1,2mol->so mol H2O=0,6mol->m H2O=10,8
Bao toan khoi luong : m muoi khan=37,6 +1,2.36,5-10,8=70,6g
\(n_{HCl}=1,2\left(mol\right)\)
\(Oxit+2HCl\rightarrow Muoi+H_2O\)
__________1,2 _________0,6 ________(mol)
Bảo toàn khối lượng:
\(m_{oxit}+m_{HCl}=m_{muoi}+m_{nuoc}\)
\(=37,6+1,2.36,5=m_{muoi}+0,6.18\)
\(\Rightarrow m_{muoi}=70,6\left(g\right)\)
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm , Fe 2 O 3 , FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí H 2 và dung dịch Y.
Cho toàn bộ H 2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. Nếu cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan ?
n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
Cho 3,425 gam hỗn hợp gồm 5 oxit FeO; CuO; Al2O3; ZnO; Fe2O3 tác dụng vừa đủ với 300 ml dung dịch HCl 0,1M. Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Tính m
\(n_{HCl}=0,1.0,3=0,03\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{0,03}{2}=0,015\left(mol\right)\)
Theo ĐLBTKL: \(m_{oxit}+m_{HCl}=m_{muối}+m_{H_2O}\)
=> mmuối = 3,425 + 0,03.36,5 - 0,015.18 = 4,25(g)
Cho m gam hỗn hợp các oxit CuO, F e 2 O 3 , ZnO tác dụng vừa đủ với 50 ml dd HCl 2M. Cô cạn dung dịch sau phản ứng thu được 3,071 g muối clorua. Giá trị của m là:
A. 0,123g
B. 0,16g
C. 2,1g
D. 0,321g
Tương tự bài 1 và bài 4, ta có:
m 3 o x i t + m H C l = m m u o i + m H 2 O s a n p h a m
⇔ m 3 o x i t = m m u o i + m H 2 O s a n p h a m - m H C l
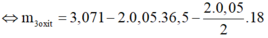
⇔ m 3 o x i t = 0,321g
⇒ Chọn D.
Cho 24 gam hh gồm CuO và Fe2O3 tác dụng vừa đủ với 400ml dd HCl 2M.
a. Cô cạn thì thu được bao nhiêu gam muối (làm theo 2 cách).
b. Tính khối lượng từng oxit
\(n_{HCl}=0,4.2=0,8\left(mol\right)\\ Đặt:n_{CuO}=a\left(mol\right);n_{Fe_2O_3}=b\left(mol\right)\left(a,b>0\right)\\CuO+2HCl\rightarrow CuCl_2+H_2O\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O \\ \Rightarrow\left\{{}\begin{matrix}80a+160b=24\\2a+6b=0,8\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ C1:m_{muối}=135a+2.162,5b=135.0,1+325.0,1=46\left(g\right)\\ C2:n_{H_2O}=\dfrac{n_{HCl}}{2}=0,4\left(mol\right)=n_{O\left(trongH_2O\right)}=n_{O\left(trong.oxit\right)}\\ \Rightarrow m_{muối}=m_{CuO,Fe_2O_3}-m_{O\left(trong.oxit\right)}+m_{Cl^-}=24-0,4.16+0,8.35,5=46\left(g\right)\\ b,m_{CuO}=80a=8\left(g\right);m_{Fe_2O_3}=160b=16\left(g\right)\)
Làm vài bài rồi ra sân bay check in đây
CuO+2HCl->CuCl2+H2O
x--------2x
Fe2O3+6HCl->2FeCl3+3H2O
y--------------6y
Ta có :
\(\left\{{}\begin{matrix}56x+160y=24\\2x+6y=0,8\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
=>m CuO=0,1.56=5,6g
=>m Fe2O3=0,1.160=16g
-> m muối =0,1.135+0,2.162,5=46g
C2:n H2O=0,4 mol
=>m muối =24-0,4.16+0,8.35,5=46g
Cho x gam hỗn hợp gồm MgO, F e 2 O 3 , ZnO, CuO tác dụng vừa đủ với 50g dd H 2 S O 4 11,76%. Cô cạn dd sau phản ứng thu được 8,41 g muối khan. Giá trị của m là:
A. 3,2g
B. 3,5g
C. 3,61g
D. 4,2g
Tương tự bài 1, ta có:
m 4 o x i t = m m u o i - m H 2 S O 4 + m H 2 O s a n p h a m
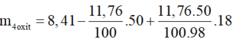
m 4 o x i t = 3,61g
⇒ Chọn C.