Dùng V (lít) khí hiđro (ở đktc)khử 8 gam sắt (|||) oxit a) viết phương trình hóa học b) tính thể tích khí hiđro thu được (ở đktc) c) tính khối lượng axit Clohiđric (HCl) đã dùng

Những câu hỏi liên quan
Dùng hiđro (H2) để khử 7,2 gam sắt (II) oxit (FeO)
a) Viết phương trình hóa học của phản ứng xảy ra ?
b) Tính khối lượng đồng (Cu) thu được?
c) Tính thể tích khí hiđro đã dùng (ở đktc)?
hình như bn ghi sai r đó phải là:đồng oxit mới phải chứ![]()
Đúng 0
Bình luận (0)
a) PTHH: H2 + CuO --t0--> Cu + H2O
b) nCuO = \(\dfrac{m}{M}\) = \(\dfrac{7,2}{80}\) = 0,09 (mol)
nCu = nCuO = 0,09 (mol)
⇒ mCu = n x M = 0,09 x 64 = 5,76 (g)
c) nH2 = nCuO = 0,09 (mol)
⇒ VH2 = n x 22,4 = 0,09 x 22,4 = 2,016 (l)
Đúng 0
Bình luận (0)
Dùng hiđro (H2) để khử 7,2 gam sắt (II) oxit (CuO)
a) Viết phương trình hóa học của phản ứng xảy ra ?
b) Tính khối lượng đồng (Cu) thu được?
c) Tính thể tích khí hiđro đã dùng (ở đktc)?
CuO+H2-to>Cu+H2O
0,09----0,09---0,09
n CuO=\(\dfrac{7,2}{80}\)=0,09 mol
=>m Cu=0,09.64=5,76g
=>VH2=0,09.22,4=2,016l
Đúng 5
Bình luận (0)
\(n_{CuO}=\dfrac{7,2}{80}=0,09mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,09 0,09 0,09 ( mol )
\(m_{Cu}=0,09.64=5,76g\)
\(V_{H_2}=0,09.22,4=2,016l\)
Đúng 2
Bình luận (0)
:Trong phòng thí nghiệm người ta dùng khí hiđro để khử sắt(III) oxit và thu được 11,2 gam Fe. a) Viết phương trình hóa học của phản ứng đã xảy ra.
b) Tính khối lượng sắt(III) oxit đã phản ứng.
c) Tính thể tích khí hiđro đã tiêu thụ (ở đktc).
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 1
Bình luận (0)
Trong phòng thí nghiệm ,người ta dùng hiđro để khử sắt(III)oxit(Fe2O3) thu được 24 gam sắt. a. Viết phương trình hóa học của phản ứng xảy ra b.tính số gam sắt(III)oxit đã phản ứng c. tính thể tích khí hiđro dùng để khử(ở đktc)
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{24}{56}=\dfrac{3}{7}\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=\dfrac{3}{14}\left(mol\right)\Rightarrow m_{Fe_2O_3}=\dfrac{3}{14}.160=\dfrac{240}{7}\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=\dfrac{9}{14}\left(mol\right)\Rightarrow V_{H_2}=\dfrac{9}{14}.22,4=14,4\left(l\right)\)
Đúng 2
Bình luận (0)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{24}{56}\approx0,43\left(mol\right)\\ a.PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
2 3 2 3
0,43 0,645 0,45 0,645
\(b.m_{Fe_2O_3}=n.M=0,43.\left(56.2+16.3\right)=68,8\left(g\right)\\ c.V_{H_2}=n.24,79=0,645.24,79=15,98955\left(l\right).\)
Đúng 1
Bình luận (0)
a)\(PTHH:Fe_3O_4+4H_2\xrightarrow[]{}3Fe+4H_2O\)
b)\(m_{Fe}=\dfrac{24}{56}=0,4\left(m\right)\)
\(PTHH:Fe_3O_4+4H_2\xrightarrow[]{}3Fe+4H_2O\)
tỉ lệ :1 4 3 4
số mol :0,13 0,53 0,4 0,53
\(m_{Fe_3O_4}=0,13.232=30,16\left(g\right)\)
c)\(V_{H_2}=0,53.22,4=11,872\left(l\right)\)
Đúng 1
Bình luận (2)
Cho 11,2 gam sắt vào một lượng dư axit hcl a Tính thể tích khí hiđro ở đktc b Tính khối lượng axit hcl đã phản ứng c Dùng lượng khí hiđro trên khử CuO ở nhiệt độ cao. Tính khối lượng Cu thu đc
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{H_2}=n_{Fe}=0.2\left(mol\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(n_{HCl}=2n_{Fe}=0.2\cdot2=0.4\left(mol\right)\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)
\(n_{Cu}=n_{H_2}=0.2\left(mol\right)\)
\(m_{Cu}=0.2\cdot64=12.8\left(g\right)\)
Đúng 1
Bình luận (0)
Trong phòng thí nghiệm người ta dùng khí hiđro để khử sắt(II) oxit và thu được 11,2 g Fe.
a) Viết phương trình hóa học của phản ứng đã xảy ra.
b) Tính khối lượng sắt (III) oxit đã phản ứng.
c) Tính thể tích khí hiđro đã tiêu thụ (đktc).
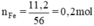
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.
Đúng 0
Bình luận (0)
Khử 16 gam sắt (III) oxit bằng khí hiđro. a. Viết phương trình phản ứng b. Tính khối lượng kim loại thu được? c. Tính thể tích khí hiđro (đktc) cần dùng
Fe2O3+3H2-to>2Fe+3H2O
0,1-----0,3-------0,2-----0,3 mol
n Fe2O3 =0,1 mol
m Fe=0,2.56=11,2g
VH2=0,3.22,4=6,72l
#yT
Đúng 1
Bình luận (0)
Cho 5,6 gam sắt tác dụng với dung dịch HCl,sau phản ứng thu được muối sắt (II) colorua FeCl2 và khí hiđro sinh ra ở đktc.( Cho Fe=56;Cl=35,5;H=1) a)Viết phương trình hoá học b)tính khối lượng axit đã dùng c) tính thể tích hiđro sinh ra (ở đktc)
Fe+2HCl->FeCl2+H2
0,1----0,2-------------0,1 mol
n Fe=5,6\56=0,1 mol
=>m HCl=0,2.36,5=7,3g
=>VH2=0,1.22,4=2,24l
Đúng 1
Bình luận (0)
cho 2,8 gam sắt tác dụng với dung dịch axit clohiđric (HCL) thu được sắt (II) clorua và khí hiđro
a) tính thể tích khí hidro thu được ở đktc
b) tính khối lượng axit clohiđric cần dùng
c) dẫn khí hiđro sinh ra ở phản ứng đi qua bột CuO nung nóng, tính khối lượng đồng tạo thành sau phản ứng
a.b.
\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,05 0,1 0,05 ( mol )
\(V_{H_2}=0,05.22,4=1,12l\)
\(m_{HCl}=0,1.36,5=3,65g\)
c.
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,05 0,05 ( mol )
\(m_{Cu}=0,05.64=3,2g\)
Đúng 2
Bình luận (0)





















