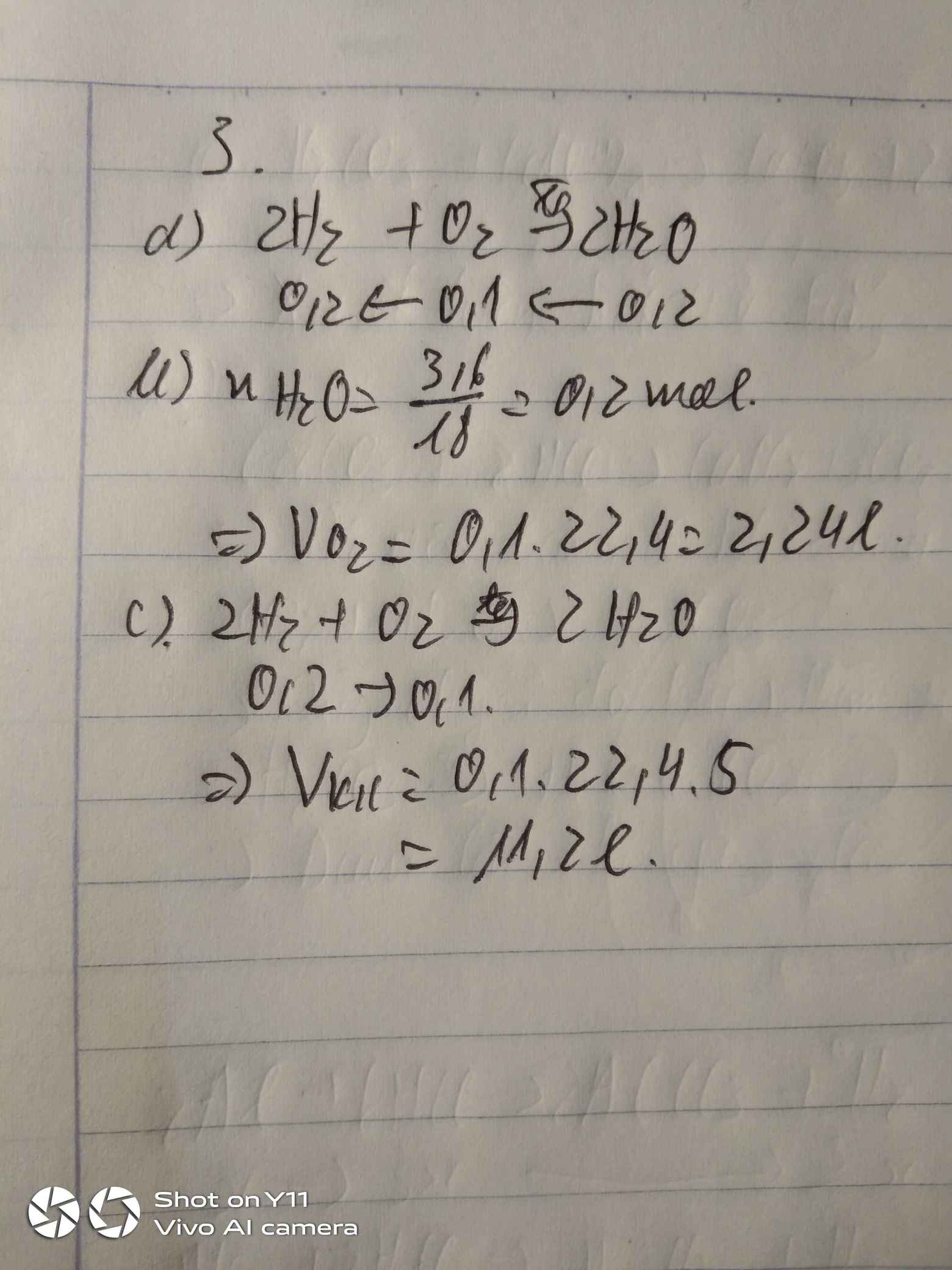Đốt cháy phốt pho theo sơ đồ P+O2 --->P2O5 a)lập phương trình phản ứng b) cần bao nhiêu lít O2 để đốt cháy hoàn toàn 15,5g P c) để tạo ra 28,4g P2O5 thì cần bao nhiêu lít không khí (biết oxi chiếm 1/5 thể tích không khí)

Những câu hỏi liên quan
Đốt cháy photpho theo sơ đồ:
P + O2 -> P2O5
a, hãy lập phương trình phản ứng
b, cần bao nhiêu lít oxi để đốt cháy hoàn toàn 15,5g photpho
c, để tạo ra 28,4g P2O5 thì cần bao nhiêu lít không khí ( biết oxi chiếm 1/5 thể tích không khí) đktc
a) Phương trình phản ứng :
4P + 5O2 ----->2P2O5 (1)
b)
np = \(\dfrac{m}{M}\)= \(\dfrac{15,5}{31}\)= 0,5 ( mol)
(1)=> nO = np . \(\dfrac{5}{4}\)= 0,5 . \(\dfrac{5}{4}\)= 0,625 ( mol )
VO = n . 22,4 = 0,625 . 22,4 = 14 (l)
Vậy cần 14l oxi để đốt chát hoàn toàn 15,5g P
c) Làm tương tự như câu b nha
Đúng 0
Bình luận (0)
nP = \(\dfrac{15,5}{31}\) = 0,5 mol
4P + 5O2 -> 2P2O5 (1)
0,5->0,625
b) VO2 = 0,625 . 22,4 = 14 (l)
c) nP2O5 = \(\dfrac{28,4}{142}\) = 0,2 mol
theo pt (1) nO2 = \(\dfrac{5}{2}\)nP2O5 = 0,5 mol
=>Vkk = 0,5. 22,4.5 = 56 (l)
Đúng 0
Bình luận (0)
pt 4P+5O2-->2P2O5
ta có nP=15,5/31=0,5 mol
theo pt nO2=5/4 nP=0,625 mol
suy ra vO2=0,625*22,4=14 l
nP2O5=0,2 mol
theo pt nO2=5/2 nP2O5=0,5 MOL
SUY RA vO2=11,2 L suy ra v kk=56 l
Đúng 0
Bình luận (0)
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
1. Đốt cháy 6,2 g Phốt pho(P) trong không khí tạo ra Đi phốt pho penta oxit (P2O5)
a. Viết phương trình hóa học của phản ứng.
b. Tính thể tích khí O2 đã tham gia phản ứng ở (đktc).
c. Tính khối lượng Đi phốt pho penta oxit (P2O5)
2. Cho 6,5 g Kẽm (Zn) tác dụng với dung dịch axit clo hiđric (HCl) tạo ra muối kẽm clorua (ZnCl2) và khí hiđro (H2).
a. Viết PTPƯ xảy ra.
b. Tính khối lượng muối kẽm clorua (ZnCl2) tạo thành?
c. Tính thể tích khí hiđro sinh ra ở (đktc)?
Đọc tiếp
1. Đốt cháy 6,2 g Phốt pho(P) trong không khí tạo ra Đi phốt pho penta oxit (P2O5) a. Viết phương trình hóa học của phản ứng. b. Tính thể tích khí O2 đã tham gia phản ứng ở (đktc). c. Tính khối lượng Đi phốt pho penta oxit (P2O5) 2. Cho 6,5 g Kẽm (Zn) tác dụng với dung dịch axit clo hiđric (HCl) tạo ra muối kẽm clorua (ZnCl2) và khí hiđro (H2). a. Viết PTPƯ xảy ra. b. Tính khối lượng muối kẽm clorua (ZnCl2) tạo thành? c. Tính thể tích khí hiđro sinh ra ở (đktc)?
Hidoro tác dụng với oxi theo sơ đồ sau H2 + o2 ----> h2o A. Hãy cân bằng phản ứng trên B.Để thủ được 3,6 gam nước thì thể tích oxi (đktc) càn dùng là bao nhiêu lít ? C.tính thể tích không khí cần dùng để đốt cháy hoàn toàn 0,2 mol khí h2 , biết thể tích các khí đó ở đktc và oxi chiếm 20% thể tích không khí
Đề Bài: Đốt chảy Photpho trong Oxi, theo sơ đồ phản ứng:
P + O2 --> P2O5
Nếu thu được 7,1g P2O5 thì cần dùng bao nhiêu lít oxi ở đktc ?
4P + 5O2 -->2 P2O5
0,1----0,125-------0,05
n P2O5=7,1\142=0,05 mol
=>VO2=0,125.22,4=2,8l
Đúng 0
Bình luận (0)
13/Để đốt cháy hoàn toàn 11,2 lít khí CH4 cần phải dùng: a)bbao nhiêu lít khí O2 b) bao nhiêu lít không khí, biết O2 chiếm 1/5 thể tích không khí (viết thể tích các khí đó ở đktc)
a) \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,5--->1
=> VO2 = 1.22,4 = 22,4 (l)
b) Vkk = 22,4.5 = 112 (l)
Đúng 1
Bình luận (0)
Đốt cháy photpho trong bình chứa 16g khí oxi theo sơ đồ phản ứng P+O2->P2O5
a.Viết phương trình phản ứng
b.Tính khối lượng chất rắn P2O5 tạo thành
c.Tính khối lượng photpho cần dùng
a) 4P + 5O2 --to--> 2P2O5
b) \(n_{O_2}=\dfrac{16}{32}=0,5\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,4<--0,5------->0,2
=> mP2O5 = 0,2.142 = 28,4 (g)
c_ mP = 0,4.31 = 12,4 (g)
Đúng 2
Bình luận (0)
\(n_{O_2}=\dfrac{16}{32}=0,5\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,4 0,5 0,2
\(\rightarrow\left\{{}\begin{matrix}m_{P_2O_5}=0,2.142=28,4\left(g\right)\\m_P=0,4.31=12,4\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
1. Photpho cháy trong khí oxi theo phản ứng sau: P + O2 - P2O5Có bao nhiêu gam P2O5 thu được nếu đốt cháy hoàn toàn 124 gam Photpho?
Đọc tiếp
1. Photpho cháy trong khí oxi theo phản ứng sau: P + O2 -> P2O5
Có bao nhiêu gam P2O5 thu được nếu đốt cháy hoàn toàn 124 gam Photpho?
Đốt cháy hoàn toàn m(g) P (photpho) trong oxi thu được 5,6 lít khí là P2O5 ở đktc
A) viết PTHH phản ứng sảy ra ?
B) tính khối lương P2O5 thu được ?
C) tính thể tích không khí cần dùng? biết ràng oxi chiếm 20% thể tích không khí.
\(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\a, 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\\b,n_{P_2O_5}=\dfrac{2}{5}.0,25=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=142.0,1=14,2\left(g\right)\\c,V_{kk\left(đktc\right)}=4.5,6=28\left(lít\right) \)
Đúng 2
Bình luận (1)