Cho m(g) Cu tác dụng hoàn toàn vs dd H2SO4 đặc nóng thu được 6,72 (l).Khí SO2 điều kiện tiêu chuẩn,sản phẩm khử duy nhất tính m ??

Những câu hỏi liên quan
Cho m gam Fe tác dụng hoàn toàn với
H
2
SO
4
đặc, nóng (dư) thu được 6,72 lít khí
SO
2
(sản phẩm khử duy nhất ở đktc). Giá trị m là A. 16,8. B. 1,68. C. 1,12. D. 11,2.
Đọc tiếp
Cho m gam Fe tác dụng hoàn toàn với H 2 SO 4 đặc, nóng (dư) thu được 6,72 lít khí SO 2 (sản phẩm khử duy nhất ở đktc). Giá trị m là
A. 16,8.
B. 1,68.
C. 1,12.
D. 11,2.
Đáp án D
Số mol thu được là: n SO 2 = 6 , 72 22 , 4 = 0 , 3 mol
Sơ đồ phản ứng: Fe 0 ⏟ m gam + H 2 S + 6 O 4 ( đặc , dư ) → t 0 Fe + 3 2 ( SO 4 ) 3 + SO 2 + 4 ⏟ 0 , 3 mol ↑ + H 2 O
Các quá trình nhường, nhận electron:
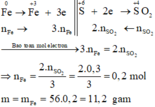
Đúng 0
Bình luận (0)
Đốt cháy 11,2 gam Fe ngoài không khí một thời gian thu được 15,04 gam hỗn hợp X gồm Fe FeO Fe304 Fe2O3 cho toàn bộ X tác dụng với H2SO4 đặc nóng thu được V lít (điều kiện tiêu chuẩn )khí SO2 (sản phẩm khử duy nhất) .Tính V
\(m_{O_2}=15.04-11.2=3.85\left(g\right)\)
\(n_{O_2}=\dfrac{3.85}{32}=0.1203125\left(mol\right)\)
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
Bảo toàn e :
\(n_{SO_2}=\dfrac{3\cdot0.2-0.1203125\cdot4}{2}=0.059375\left(mol\right)\)
\(V_{SO_2}=1.33\left(l\right)\)
Đúng 1
Bình luận (2)
Hỗn hợp a gồm 2 kim loại Fe và Cu có khối lượng m gam. cho A tác dụng với dung dịch HCl dư thu được 2,24 l khí H2 điều kiện tiêu chuẩn. nếu cho A tác dụng với dung dịch H2 SO4 đặc nóng dư thì thu được 4,48 lít khí SO2 sản phẩm khử duy nhất biết các phản ứng xảy ra hoàn toàn.
a. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b. Tính thể tích dung dịch HCL 1 m đã dùng biết HCl dùng dư 10% so với lượng cần phản ứng.
C. điện lượng khí SO2 ở trên qua dung dịch brom dư Sau đó nhỏ tiế...
Đọc tiếp
Hỗn hợp a gồm 2 kim loại Fe và Cu có khối lượng m gam. cho A tác dụng với dung dịch HCl dư thu được 2,24 l khí H2 điều kiện tiêu chuẩn. nếu cho A tác dụng với dung dịch H2 SO4 đặc nóng dư thì thu được 4,48 lít khí SO2 sản phẩm khử duy nhất biết các phản ứng xảy ra hoàn toàn. a. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu. b. Tính thể tích dung dịch HCL 1 m đã dùng biết HCl dùng dư 10% so với lượng cần phản ứng. C. điện lượng khí SO2 ở trên qua dung dịch brom dư Sau đó nhỏ tiếp BaCl2 đến dư vào dung dịch tính khối lượng kết tủa thu được.
Cho hỗn hợp X gồm Al và Mg tác dụng với 1 lít dung dịch gồm AgNO3 a mol/lít và Cu(NO3)2 2a mol/lít, thu được 45,2 gam chất rắn Y. Cho Y tác dụng với dung dịch H2SO4 đặc nóng dư, thu được 7,84 lít khí SO2 (ở điều kiện tiêu chuẩn, là sản phẩm khử duy nhất). Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là: A. 0,25 B. 0,15 C. 0,20 D. 0,30
Đọc tiếp
Cho hỗn hợp X gồm Al và Mg tác dụng với 1 lít dung dịch gồm AgNO3 a mol/lít và Cu(NO3)2 2a mol/lít, thu được 45,2 gam chất rắn Y. Cho Y tác dụng với dung dịch H2SO4 đặc nóng dư, thu được 7,84 lít khí SO2 (ở điều kiện tiêu chuẩn, là sản phẩm khử duy nhất). Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là:
A. 0,25
B. 0,15
C. 0,20
D. 0,30
Đáp án D
Áp dụng bảo toàn electron có: ![]()
Trường hợp 1: Chất rắn chỉ có Ag
⇒ n Ag = 0 , 7 mol ⇒ m Ag = 75 , 6 gam > 45 , 2 => Loại
Trường hợp 2: Chất rắn có a mol Ag và 2a mol Cu
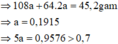
=> Loại =>Ag+ phản ứng hết, Cu2+ phản ứng còn dư
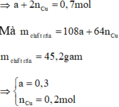
Đúng 0
Bình luận (0)
Cho m gam hh gồm Cu và CuO tác dụng vừa đủ vs dd H2SO4 đặc nóng thu đc 4,48 lít khí SO2 là sản phẩm khử duy nhất ,dd thu đc có chứa 48g chất tan duy nhất.Tính m?
\(n_{SO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ n_{CuSO_4}=\dfrac{48}{160}=0,3\left(mol\right)\)
PTHH:
Cu + 2H2SO4 ---> CuSO4 + SO2 + 2H2O
0,2 0,2 0,2
CuO + H2SO4 ---> CuSO4 + H2O
0,1 0,1
\(m=0,2.64+0,1.80=20,8\left(g\right)\)
Đúng 1
Bình luận (1)
Hòa tan m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO, Fe3O4 trong H2SO4 đặc nóng, dư, thu được 3,36 lít SO2 (đktc, sản phẩm khử duy nhất). Mặt khác, nung m gam X với khí CO dư, thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn thu được 35 gam kết tủa. Hòa tan Y trong dung dịch HNO3 đặc nóng, due thu được V lít khí NO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). Giá trị của V là: A.33,6. B. 11,2. C. 44,8. D. 22,4.
Đọc tiếp
Hòa tan m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO, Fe3O4 trong H2SO4 đặc nóng, dư, thu được 3,36 lít SO2 (đktc, sản phẩm khử duy nhất). Mặt khác, nung m gam X với khí CO dư, thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn thu được 35 gam kết tủa. Hòa tan Y trong dung dịch HNO3 đặc nóng, due thu được V lít khí NO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). Giá trị của V là:
A.33,6.
B. 11,2.
C. 44,8.
D. 22,4.
Cho 17,2 gam hỗn hợp kim loại gồm Fe cà Cu tác dụng vừa đủ với dd H2SO4 đặc nóng dư thu được 6,72 lít khí SO2 (đktc) là sản phẩm khử duy nhất. Tính khối lượng mỗi muối và khối lượng dung dịch H2SO4 80% phản ứng
`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Đúng 4
Bình luận (0)
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 17,6g hh cu và Fe vào dd h2so4 đặc nóng dư thu đc 8,96 l khí SO2 là sản phẩm khử duy nhất .Tính % theo khối lượng mỗi kim loại
Gọi số mol Cu, Fe là a, b (mol)
=> 64a + 56b = 17,6 (1)
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
b-------------------------------->1,5b
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
a--------------------------->a
=> a + 1,5b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,1.64}{17,6}.100\%=36,36\%\\\%m_{Fe}=\dfrac{0,2.56}{17,6}.100\%=63,64\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 10,8 gam sắt (II) oxit tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng tạo thành một khí duy nhất là khí SO2. Tính thể tích khí thu được ở điều kiện tiêu chuẩn?
A. 2,24 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 5,6 lít.
\(2FeO+4H_2SO_4 \buildrel{{t^o}}\over\longrightarrow Fe_2(SO_4)_3+SO_2+4H_2O\\ n_{Fe}=\frac{10,8}{72}=0,15(mol)\\ n_{SO_2}=\frac{1}{2}.n_{FeO}=\frac{1}{2}.0,15=0,075(mol)\\ V_{SO_2}=0,075.22,4=1,68(l)\)
Đúng 3
Bình luận (2)
Cho 10,8 gam sắt (II) oxit tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng tạo thành một khí duy nhất là khí SO2. Tính thể tích khí thu được ở điều kiện tiêu chuẩn?
A. 2,24 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 5,6 lít.
2FeO + 4H2SO4 → 4H2O + Fe2(SO4)3 + SO2
\(n_{SO_2}=\dfrac{1}{2}n_{FeO}=0,075\left(mol\right)\)
=> VSO2= 0,075 .22,4= 1,68 (lít)
Đúng 2
Bình luận (0)






















