Các đại lượng để lập bảng trong toán phần trăm là gì vậy mn

Những câu hỏi liên quan
hãy tính toán và điền giá trị chưa biết vào ô trong bảng sau ;đại lượng mct mdd vdd c phần trăm cm dd nacl 58,5g 400g
Anh có thấy bảng nào đâu ta?
Đúng 2
Bình luận (0)
Trong các bài toán về cấp số cộng, ta thường gặp năm đại lượng u_1,d,n,u_n,S_n
a) Hãy viết các hệ thức liên hệ giữa các đại lượng đó. Cần phải biết ít nhất mấy đại lượng để có thể tìm được các đại lượng còn lại ?
b) Lập bảng theo mẫu sau và điền số thích hợp vào ô trống ?
Đọc tiếp
Trong các bài toán về cấp số cộng, ta thường gặp năm đại lượng \(u_1,d,n,u_n,S_n\)
a) Hãy viết các hệ thức liên hệ giữa các đại lượng đó. Cần phải biết ít nhất mấy đại lượng để có thể tìm được các đại lượng còn lại ?
b) Lập bảng theo mẫu sau và điền số thích hợp vào ô trống ?

a) Cần biết ít nhật ba trong năm đại lượng u1, n, d, un, Sn thì có thể tính được hai đại lượng còn lại.
b) Thực chất đây là năm bài tập nhỏ, mỗi bài ứng với các dữ liệu ở một dòng. Học sinh phải giải từng bài nhỏ rồi mới điền kết quả.
b1) Biết u1 = -2, un = 55, n = 20. Tìm d, Sn
Áp dụng công thức d = 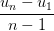 , Sn =
, Sn = 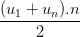
Đáp số: d = 3, S20 = 530.
b2) Biết d = -4, n = 15, Sn = 120. Tìm u1, un
Áp dụng công thức un = u1 + (n - 1)d và Sn = 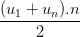 ,
,
ta có: 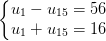
Giải hệ trên, ta được u1 = 36, u15 = - 20.
Tuy nhiên, nếu sử dụng công thức 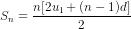
thì S15 = 120 = 15u1 + 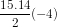 .
.
Từ đó ta có u1 = 36 và tìm được u15 = - 20.
b3) Áp dụng công thức un = u1 + (n - 1)d, từ đây ta tìm được n; tiếp theo áp dụng công thức 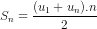 . Đáp số: n = 28, Sn = 140.
. Đáp số: n = 28, Sn = 140.
b4) Áp dụng công thức 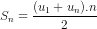 , từ đây tìm được n, tiếp theo áp dụng công thức un = u1 + (n - 1)d. Đáp số: u1 = -5, d= 2.
, từ đây tìm được n, tiếp theo áp dụng công thức un = u1 + (n - 1)d. Đáp số: u1 = -5, d= 2.
b5) Áp dụng công thức 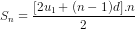 , từ đây tìm được n, tiếp theo áp dụng công thức un = u1 + (n - 1)d. Đáp số: n = 10, un = -43
, từ đây tìm được n, tiếp theo áp dụng công thức un = u1 + (n - 1)d. Đáp số: n = 10, un = -43
Đúng 0
Bình luận (0)
Lượng nước trong hạt tươi là 16%. Người ta lấy 200 kg hạt tươi đem phơi khô thì thấy khối lượng giảm đi 20kg.
Vậy tỉ số phần trăm lượng nước trong hạt phơi khô là bao nhiêu ?
(Làm tròn đến một chữ số phần thập phân)
Toán Violympic đó các bạn ! Giải giúp mình nhé các cao thủ Toán INTERNET !
luong nuoc trong qua kho la;
200x16% - 20 = 12kg
ty so % la;
(12 / 180)x100% = 6,7%
Đúng 0
Bình luận (0)
Lượng nước trong 200 kg hạt tươi là: 200 x 16% = 32 kg
Lượng thuần hạt là: 200 - 32 = 168 kg
Lượng nước còn lại trong hạt đã phơi khô là: 32 - 20 = 12 kg
Tỉ số % nước trong hạt đã phoi khô là: 12 : (168+12) =6,6666666666667%
6,666666666666667% = 6,7%
Đúng 0
Bình luận (0)
Trong các bài toán về cấp số cộng, ta thường gặp năm đại lượng
u
1
,
d
,
n
,
u
n
,
S
n
.a.Hãy viết các hệ thức liên hệ giữa các đại lượng đó. Cần phải biết ít nhất mấy đại lượng để có thể tìm được các đại lượng còn lại?b.Lập bảng theo mẫu sau và điền vào số thích hợp vào ô trống:
Đọc tiếp
Trong các bài toán về cấp số cộng, ta thường gặp năm đại lượng u 1 , d , n , u n , S n .
a.Hãy viết các hệ thức liên hệ giữa các đại lượng đó. Cần phải biết ít nhất mấy đại lượng để có thể tìm được các đại lượng còn lại?
b.Lập bảng theo mẫu sau và điền vào số thích hợp vào ô trống:
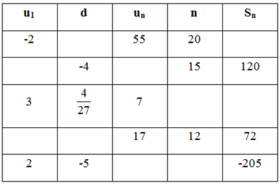
a. Mối liên hệ giữa các công thức:
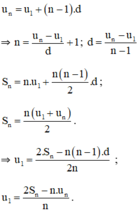
Dựa vào các công thức trên thấy cần phải biết ít nhất 3 đại lượng để tìm được các đại lượng còn lại.
b. Ta có bảng:
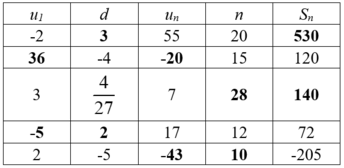
Giải thích:
+ Với u1 = -2; un = 55; n = 20
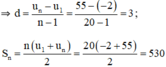
+ Với d = -4 ; n = 15 ; Sn = 120
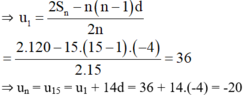
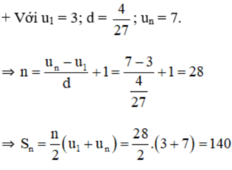
+ Với un = 17; n = 12; Sn = 72
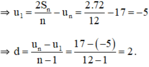
+ Với u1 = 2; d = -5; Sn = -205.
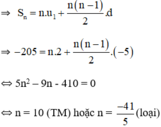
⇒ un = u10 = u1 + 9d = -43.
Đúng 0
Bình luận (0)
Cho biết các nguyên tố trong hình 5.2 thuộc nhóm nguyên tố đại lượng hay vi lượng. Tổng tỉ lệ phần trăm của các nguyên tố C, H, O, N là bao nhiêu và tỉ lệ này có ý nghĩa gì?
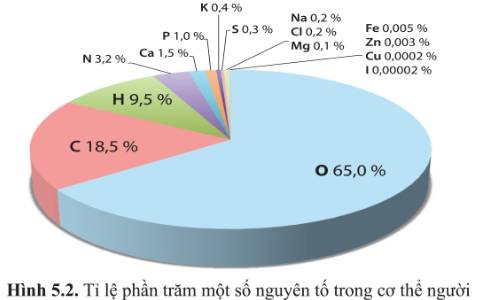
- Nguyên tố đại lượng chiếm lượng lớn trong cơ thể còn các nguyên tố vi lượng chiếm lượng rất nhỏ (thường nhỏ hơn 0,01% khối lượng cơ thể). Dựa vào đó, ta có thể phân loại các nguyên tố trong hình 5.2:
+ C, H, O, N, Ca, P, K, S, Na, Cl, Mg chiếm tỉ lệ lớn hơn 0,01% nên thuộc nhóm các nguyên tố đại lượng.
+ Zn, Fe, Cu, I chiếm tỉ lệ nhỏ hơn 0,01% nên thuộc nhóm các nguyên tố vi lượng.
- Tổng tỉ lệ phần trăm của các nguyên tố C, H, O, N là 96,2%. Tỉ lệ này cho thấy C, H, O, N là thành phần chủ yếu cấu tạo nên các hợp chất chính trong tế bào như nước, carbohydrate, lipid, protein và nucleic acid.
Đúng 1
Bình luận (0)
Điểm bài kiểm tra môn Toán học kỳ I của học sinh lớp 7A được ghi trong bảng sau:10910999899109101078108989981088979109a) Dấu hiệu ở đây là gì? Số các giá trị là bao nhiêu?b) Lập bảng “tần số”.
Đọc tiếp
Điểm bài kiểm tra môn Toán học kỳ I của học sinh lớp 7A được ghi trong bảng sau:
10 | 9 | 10 | 9 | 9 | 9 | 8 | 9 | 9 | 10 |
9 | 10 | 10 | 7 | 8 | 10 | 8 | 9 | 8 | 9 |
9 | 8 | 10 | 8 | 8 | 9 | 7 | 9 | 10 | 9 |
a) Dấu hiệu ở đây là gì? Số các giá trị là bao nhiêu?
b) Lập bảng “tần số”.
a:
Dấu hiệu là :điểm kiểm tra học kì I của lớp 7A.
Số các giá trị là 30.
b:
| Giá trị | 10 | 9 | 8 | 7 |
| Tần số | 8 | 13 | 7 | 2 |
Đúng 2
Bình luận (0)
a) -Dấu hiệu: Điểm kiểm tra môn toán học kì I của mỗi học sinh lớp 7A.
- Số các giá trị: 30
b) Bảng ''tần số":
| Số điểm(x) | 7 | 8 | 9 | 10 | |
| Tần số(n) | 2 | 7 | 13 | 8 | N= 30 |
*Ghi giá trị (x) theo thứ tự từ nhỏ--> lớn nha!
➜Bạn có thể tham khảo nhé!
Đúng 2
Bình luận (0)
Điểm kiểm tra Toán của lớp 7A được ghi lại trong bảng sau:38410697967761065888687104888986851099799769a, dấu hiệu ở đây là gì?b, Tính số học sinh là bài kiểm trac, số các giá trị khác nhau của dấu hiệu là gì ? d, Lập bảng tần số và tính số trung bình cộnge, tìm mốt của dấu hiệuf, Số điểm giỏi (9 đến 10) chiếm tỉ lệ bao nhiêu
Đọc tiếp
Điểm kiểm tra Toán của lớp 7A được ghi lại trong bảng sau:
| 3 | 8 | 4 | 10 | 6 | 9 | 7 | 9 |
| 6 | 7 | 7 | 6 | 10 | 6 | 5 | 8 |
| 8 | 8 | 6 | 8 | 7 | 10 | 4 | 8 |
| 8 | 8 | 9 | 8 | 6 | 8 | 5 | 10 |
| 9 | 9 | 7 | 9 | 9 | 7 | 6 | 9 |
a, dấu hiệu ở đây là gì?
b, Tính số học sinh là bài kiểm tra
c, số các giá trị khác nhau của dấu hiệu là gì ?
d, Lập bảng tần số và tính số trung bình cộng
e, tìm mốt của dấu hiệu
f, Số điểm giỏi (9 đến 10) chiếm tỉ lệ bao nhiêu
Dấu hiệu là điểm Ktra toán
Có 40hs làm bài
Có 8GT khác nhau
Đúng 5
Bình luận (0)
a)Dấu hiệu ở đây là " Điểm kiểm tra toán của lớp 7A"
b)Có tổng 40 hs của lớp 7A
c)có 8 gtrị khác nhau
d,e,f chịu thua
Đúng 0
Bình luận (1)
a, dấu hiệu là điểm kiểm tra toán của lớp 7A
b, Có 40 học sinh tham gia làm bài kiểm tra
c, Số các giá trị của dấu hiệu là 32
d, Bảng ts :
Giá trị (x) 2 4 5 6 7 8 9 10
Tần số (n) 2 4 8 6 4 5 2 1 N = 32
e, Mốt của dấu hiệu (Mo) = 8
Đúng 1
Bình luận (0)
a. Giải bài toán lập CTHH bằng phương pháp đại số.Thí dụ: Đốt cháy một hỗn hợp 300ml hiđrocacbon và amoniac trong oxi có dư. Sau khi cháy hoàn toàn, thể tích khí thu được là 1250ml. Sau khi làm ngưng tụ hơi nước, thể tích giảm còn 550ml. Sau khi cho tác dụng với dung dịch kiềm còn 250ml trong đó có 100ml nitơ. Thể tích của tất cả các khí đo trong điều kiện như nhau. Lập công thức của hiđrocacbonb. Giải bài toán tìm thành phần của hỗn hợp bằng phương pháp đại số.Thí dụ: Hoà tan trong nước 0,325g...
Đọc tiếp
a. Giải bài toán lập CTHH bằng phương pháp đại số.
Thí dụ: Đốt cháy một hỗn hợp 300ml hiđrocacbon và amoniac trong oxi có dư. Sau khi cháy hoàn toàn, thể tích khí thu được là 1250ml. Sau khi làm ngưng tụ hơi nước, thể tích giảm còn 550ml. Sau khi cho tác dụng với dung dịch kiềm còn 250ml trong đó có 100ml nitơ. Thể tích của tất cả các khí đo trong điều kiện như nhau. Lập công thức của hiđrocacbon
b. Giải bài toán tìm thành phần của hỗn hợp bằng phương pháp đại số.
Thí dụ: Hoà tan trong nước 0,325g một hỗn hợp gồm 2 muối Natriclorua và Kaliclorua. Thêm vào dung dịch này một dung dịch bạc Nitrat lấy dư - Kết tủa bạc clorua thu được có khối lượng là 0,717g. Tính thành phần phần trăm của mỗi chất trong hỗn hợp.
Help me !
a. Giải bài toán lập CTHH bằng phương pháp đại số.
Thí dụ: Đốt cháy một hỗn hợp 300ml hiđrocacbon và amoniac trong oxi có dư. Sau khi cháy hoàn toàn, thể tích khí thu được là 1250ml. Sau khi làm ngưng tụ hơi nước, thể tích giảm còn 550ml. Sau khi cho tác dụng với dung dịch kiềm còn 250ml trong đó có 100ml nitơ. Thể tích của tất cả các khí đo trong điều kiện như nhau. Lập công thức của hiđrocacbon
Bài giải
Khi đốt cháy hỗn hợp hiđrocacbon và amoniac trong oxi phản ứng xảy ra theo phương trình sau:
4NH3 + 3O2 -> 2N2 + 6H2O (1)
CxHy + (x + y/4) O2 -> xCO2 + y/2 H2O (2)
Theo dữ kiện bài toán, sau khi đốt cháy amoniac thì tạo thành 100ml nitơ. Theo PTHH (1) sau khi đốt cháy hoàn toàn amoniac ta thu được thể tích nitơ nhỏ hơn 2 lần thể tích amoniac trong hỗn hợp ban đầu, vậy thể tích amonac khi chưa có phản ứng là 100. 2 = 200ml. Do đó thể tích hiđro cácbon khi chưa có phản ứng là 300 - 200 = 100ml. Sau khi đốt cháy hỗn hợp tạo thành (550 - 250) = 300ml, cacbonnic và (1250 - 550 - 300) = 400ml hơi nước.
Từ đó ta có sơ đồ phản ứng:
CxHy + (x + y/4) O2 -> xCO2 + y/2 H2O
100ml 300ml 400ml
Theo định luật Avogađro, có thể thay thế tỉ lệ thể tích các chất khí tham gia và tạo thành trong phản ứng bằng tỉ lệ số phân tử hay số mol của chúng.
CxHy + 5O2 -> 3CO2 + 4 H2O
=> x = 3; y = 8
Vậy CTHH của hydrocacbon là C3H8
b. Giải bài toán tìm thành phần của hỗn hợp bằng phương pháp đại số.
Thí dụ: Hoà tan trong nước 0,325g một hỗn hợp gồm 2 muối Natriclorua và Kaliclorua. Thêm vào dung dịch này một dung dịch bạc Nitrat lấy dư - Kết tủa bạc clorua thu được có khối lượng là 0,717g. Tính thành phần phần trăm của mỗi chất trong hỗn hợp.
Bài giải
Gọi MNaCl là x và mKCl là y ta có phương trình đại số:
x + y = 0,35 (1)
PTHH: NaCl + AgNO3 -> AgCl ↓ + NaNO3
KCl + AgNO3 -> AgCl ↓ + KNO3
Dựa vào 2 PTHH ta tìm được khối lượng của AgCl trong mỗi phản ứng:
m'AgCl = x . MAgCl/MNaCl = x . 143/58,5 = x . 2,444
mAgCl = y . MAgCl/MKCl = y . 143/74,5 = y . 1,919
=> mAgCl = 2,444x + 1,919y = 0,717 (2)
Từ (1) và (2) => hệ phương trình
Giải hệ phương trình ta được: x = 0,178
y = 0,147
=> % NaCl = .100% = 54,76%
% KCl = 100% - % NaCl = 100% - 54,76% = 45,24%.
Vậy trong hỗn hợp: NaCl chiếm 54,76%, KCl chiếm 45,24%
------------ Chúc bn học tốt ----------------
Đúng 0
Bình luận (0)
a)Khi đốt cháy hồn hợp hiđrocacbon và amoniac trong oxi phản ứng xảy ra theo phương trình sau
\(4NH3+3O_2\rightarrow2N_2+6H_2O\left(1\right)\)
\(CxHy+\left(x+\frac{y}{4}\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\left(2\right)\)
Theo dữ kiện bài, sau khi đốt cháy amoniac thì tạo thành 10ml nitơ
Theo PTHH (1) sau khi đốt cháy hoàn toàn amoniac ta thu được thể tích nitơ nhỏ hơn 2 lần thể tích amoniac trong hồn hợp ban đầu, vậy thể tích amonac khi chưa có phản ứng là:\(100\cdot2=200ml\)
Do đó thể tích hiđro cácbon khi chưa có phản ứng là:\(300-200=100ml\).Sau khi đốt cháy hỗn hợp tạo thành (550-250)=30ml, cácbonnic và (1250-550-300)=400ml hơi nước
Từ đó ta có sơ đồ phản ứng:
\(CxHy+\left(x+\frac{y}{4}\right)O_2\rightarrow xCO_2+\frac{y}{2}H_2O\)
100ml 300ml 400ml
Theo định luật Avogađro, có thể thay tỉ lệ thể tích các chất khí tham gia và tạo thành trong phản ứng bằng tỉ lệ phần tử hay số mol của chúng
\(C_xH_y+5O_2\rightarrow3CO_2+4H_2O\)
\(\Rightarrow x=3;y=8\)
Vậy CTHH của hidrocacbon là C3H8
Đúng 0
Bình luận (0)
Hòa tan 8g CuSO4 trong 100ml H2O tính nồng độ phần trăm và nồng độ mol của dung dịch thu được để tính CM của dung dịch ta phải tính các đại lượng nào nêu biểu thức để tính C% của dung dịch ta còn thiếu đại lượng nêu cách tính
\(n_{CuSO_4}=\dfrac{8}{160}=0,05\left(mol\right)\\ V_{ddCuSO_4}=V_{H_2O}=100\left(ml\right)=0,1\left(l\right)\\ C_{MddCuSO_4}=\dfrac{0,05}{0,1}=0,5\left(M\right)\\ m_{H_2O}=100.1=100\left(g\right)\\ m_{ddCuSO_4}=100+8=108\left(g\right)\\ C\%_{ddCuSO_4}=\dfrac{8}{108}.100\approx7,407\%\)
Đúng 0
Bình luận (0)
Câu 1 (2,0 điểm): Điểm kiểm tra 45 phút môn Toán của học sinh lớp 7A được ghi lại trong bảng sau:65358779581658995107102678424689a) Dấu hiệu ở đây là gì? Số các giá trị là bao nhiêu?b) Lập bảng tần số?c) Tính số trung bình cộng?
Đọc tiếp
Câu 1 (2,0 điểm): Điểm kiểm tra 45 phút môn Toán của học sinh lớp 7A được ghi lại trong bảng sau:
6 | 5 | 3 | 5 | 8 | 7 |
7 | 9 | 5 | 8 | 1 | 6 |
5 | 8 | 9 | 9 | 5 | 10 |
7 | 10 | 2 | 6 | 7 | 8 |
4 | 2 | 4 | 6 | 8 | 9 |
a) Dấu hiệu ở đây là gì? Số các giá trị là bao nhiêu?
b) Lập bảng tần số?
c) Tính số trung bình cộng?
a, Dấu hiệu: Điểm kiểm tra 45 phút môn Toán của học sinh lớp 7A
Số các giá trị: 30
b, Bảng tần số:
| giá trị(x) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
| tần số(n) | 1 | 2 | 1 | 2 | 5 | 4 | 4 | 5 | 4 | 2 | N=30 |
c, Tổng các tích x.n là:
1.1+2.2+3.1+4.2+5.5+6.4+7.4+8.5+9.4+10.2
=1+4+3+8+25+24+28+40+36+20
=189
Số trung bình cộng là \(\overline{X}\)= \(\dfrac{189}{30}\)=6,3
Đúng 0
Bình luận (0)





























