đốt cháy hoàn toàn 10 kg than đá chứa 10% tạp chất khác ko cháy được , còn lại là cacbon . tính thể tích khí co2 tạo thàn ở đktc

Những câu hỏi liên quan
BÀI 1: đốt cháy hoàn toàn 14 kg than đá có chứa 96%C, 2,56%S còn lại là tạp chất không cháy. Tính thể tích CO2 và SO2 tạo thành?
BÀI 2: tính thể tích khí oxi cần thiết để đốt cháy hoàn toàn khí Etan (C4H8) có trong 1,8m3 khí chứa 2% tạp chất không cháy. Các thể tích đo được ở điều kiện tiêu chuẩn?
B1:
\(n_C=\dfrac{96\%.14.1000}{12}=1120\left(mol\right)\\ n_S=\dfrac{2,56\%.14.1000}{32}=11,2\left(mol\right)\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ n_{SO_2}=n_S=11,2\left(mol\right)\\ n_{CO_2}=n_C=1120\left(mol\right)\\ V_{CO_2\left(đktc\right)}=1120.22,4=25088\left(l\right)\\ n_{SO_2\left(đktc\right)}=11,2.22,4=250,88\left(l\right)\)
Đúng 1
Bình luận (0)
B2:
\(n_{C_2H_6}=\dfrac{1,8.\left(100\%-2\%\right).1000}{22,4}=78,75\left(mol\right)\\ C_2H_6+\dfrac{7}{2}O_2\rightarrow\left(t^o\right)2CO_2+3H_2O\\ n_{O_2\left(đktc\right)}=\dfrac{7}{2}.78,75=275,625\left(mol\right)\\ V_{O_2\left(đktc\right)}=275,625.22,4=6174\left(l\right)=6,174\left(m^3\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 24 kg than đá có chứa 0,5% tạp chất lưu huỳnh và bà và 1,5% tạp chất khác không cháy được chấm. Tính thể tích khí CO2 và SO2 tạo thành (ở điều kiện tiêu chuẩn)
\(m_S=0,5\%.24=0,12\left(kg\right)=120\left(g\right)\\ \Rightarrow n_S=\dfrac{120}{32}=3,75\left(mol\right)\\ m_C=1,5\%.24=0,36\left(kg\right)=360\left(g\right)\\ \Rightarrow n_C=\dfrac{360}{12}=30\left(mol\right)\\ S+O_2\rightarrow\left(t^o\right)SO_2\\ C+O_2\rightarrow\left(t^o\right)CO_2\\ n_{SO_2}=n_S=3,75\left(mol\right)\\ \Rightarrow V_{SO_2\left(đktc\right)}=3,75.22,4=84\left(l\right)\\ n_{CO_2}=n_C=30\left(mol\right)\\ \Rightarrow V_{CO_2\left(đktc\right)}=22,4.30=672\left(l\right)\)
(Chắc đề là 1,5% C)
Đúng 1
Bình luận (6)
24kg = 24000g
\(m_S=24000.0,5\%=120\left(g\right)\\ n_S=\dfrac{120}{32}=3,75\left(mol\right)\\ \%C=100\%-0,5\%-1,5\%=98\%\\ m_C=24000.98\%=23520\left(g\right)\\ n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
PTHH:
S + O2 → (to) SO2
3,75 3,75 3,75
C + O2 → (to) CO2
1960 1960 1960
\(V_{SO_2}=22,4.3,75=84\left(l\right)\\ V_{CO_2}=22,4.1960=43904\left(l\right)\)
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn 24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích CO2 và SO2 tạo thành (ở đktc)
$m_S = 24.0,5\% = 0,12(kg)$
$m_C = 24.(100\% - 0,5\% - 1,5\%) = 23,52(kg)$
$\Rightarrow n_S = 0,00375(kmol) = 3,75(mol)$
$n_C = 1,96(kmol) = 1960(mol)$
$C + O_2 \xrightarrow{t^o} CO_2$
$S + O_2 \xrightarrow{t^o} SO_2$
Theo PTHH :
$n_{CO_2} = n_C = 1960(mol) ; n_{SO_2} = n_S = 3,75(mol)$
$\Rightarrow V_{CO_2} = 1960.22,4 = 43904(lít)$
$\Rightarrow V_{SO_2} = 3,75.22,4 = 84(lít)$
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích khí CO2 và SO2 tạo thành (ở điều kiện tiêu chuẩn).
Đổi: 24kg = 24000g
24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được

⇒ nS = 120 / 32 = 3,75 mol
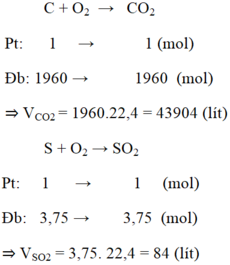
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 2 kg than đá (chứa 96,6 phần trăm cacbon:, 0,6 phần trăm lưu huỳnh : còn lại là tạp chất trơ ko cháy) bằng oxi không khí
a) tính thể tích không khí dùng ở điều kiện tiêu chuẩn. Cho không khí chứa 80 phần trăm nitơ :20 phần trăm oxi và thể tích
b) khi đốt cháy than đá trong điều kiện nào sẽ tạo ra CO. Viết phương trình phản ứng
Đốt hoàn toàn 1,5 kg than chứa 90℅ cacbon còn lại là tạp chất ko cháy. Tính thể tích oxi và không khí cần dùng để đốt hết 1,5 kg than biết oxi chiếm 1/5 thể tích không khí và các khí đi ở điều kiện tiêu chuẩn
Ta có: \(m_C=1,5.1000.90\%=1350\left(g\right)\)
\(n_C=\dfrac{1350}{12}=112,5\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_{O_2}=n_C=112,5\left(mol\right)\)
\(\Rightarrow V_{O_2}=112,5.22,4=2520\left(l\right)\)
\(V_{kk}=V_{O_2}.5=12600\left(l\right)\)
Đúng 1
Bình luận (0)
Tính thể tích không khí (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than tổ ong chứa 60% cacbon, 0,8% lưu huỳnh và phần còn lại là tạp chất không cháy. Biết oxi chiếm 1/5 thể tích không khí.
PTHH:
C + O2 ---to----> CO2
50.....50.......................................(mol)
S + O2 ----to---> SO2
0,25...0,25 ............................................(mol)
→ (cần dùng) = (50 + 0,25) . 22,4 = 1125,6 (l)
=>Vkk=1125.6.5=5628l
Đúng 0
Bình luận (0)
Bài 1: Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than đá chứa 96% cacbon và 4% tạp chất không cháy.Bài 2: Cho những chất sau: Ccacbon, hiđro, magie, metan, cacbon oxit. Cho biết sự oxi hóa chất nào sẽ tạo ra:A. Oxit ở thể rắn.B. Oxit ờ thể lỏng.C. Oxit ở thể khíBài 3: Một bình chứa 44,8 lít khí oxi, vs lượng khí oxi này có thể đốt cháy đc:A. Bao nhiêu mol cacbon, mol photpho, mol lưu huỳnh.B. Bao nhiêu gam bột sắt, bột nhôm.C. Bao nhiêu mol CO, C_2H_60?
Đọc tiếp
Bài 1: Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than đá chứa 96% cacbon và 4% tạp chất không cháy.
Bài 2: Cho những chất sau: Ccacbon, hiđro, magie, metan, cacbon oxit. Cho biết sự oxi hóa chất nào sẽ tạo ra:
A. Oxit ở thể rắn.
B. Oxit ờ thể lỏng.
C. Oxit ở thể khí
Bài 3: Một bình chứa 44,8 lít khí oxi, vs lượng khí oxi này có thể đốt cháy đc:
A. Bao nhiêu mol cacbon, mol photpho, mol lưu huỳnh.
B. Bao nhiêu gam bột sắt, bột nhôm.
C. Bao nhiêu mol CO, C\(_2\)H\(_6\)0?
Bài 1: Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1 kg than đá chứa 96% cacbon và 4% tạp chất không cháy.
Theo gt ta có: $n_{C}=800(mol)$
$C+O_2\rightarrow CO_2$
Suy ra $n_{O_2}=800(mol)\Rightarrow V_{O_2}=17920(l)$
Bài 2: Cho những chất sau: Ccacbon, hiđro, magie, metan, cacbon oxit. Cho biết sự oxi hóa chất nào sẽ tạo ra:
A. Oxit ở thể rắn: Mg
B. Oxit ờ thể lỏng: $H_2$
C. Oxit ở thể khí: $C;CH_4;CO$
Đúng 3
Bình luận (1)
khối lượng C trong 1kg than: mc= = 0,96 (kg)= 960g
nc= = 80 (mol)
C + O2 CO2
80 80 (mol)
VO2= n. 22,4= 80. 22,4 = 1792 (l)
2 c
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Bài 5 (SGK trang 84): Đốt cháy hoàn toàn 24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được. Tính thể tích khí CO2 và SO2 ( ở điều kiện tiêu chuẩn ).
PT: \(C+O_2\underrightarrow{t^o}CO_2\) (1)
\(S+O_2\underrightarrow{t^o}SO_2\) (2)
Ta có: mS = 24.0,5% = 0,12 (kg) = 120 (g) ⇒ nS = 120/32 = 3,75 (mol)
Theo PT (2): \(n_{SO_2}=n_S=3,75\left(mol\right)\)
\(\Rightarrow V_{SO_2}=3,75.22,4=84\left(l\right)\)
Ta có: mC = 24 - 0,12 - 24.1,5% = 23,52 (kg) = 23520 (g)
\(\Rightarrow n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
Theo PT (1): \(n_{CO_2}=n_C=1960\left(mol\right)\)
\(\Rightarrow V_{CO_2}=1960.22,4=43904\left(l\right)\)
Đúng 1
Bình luận (0)























