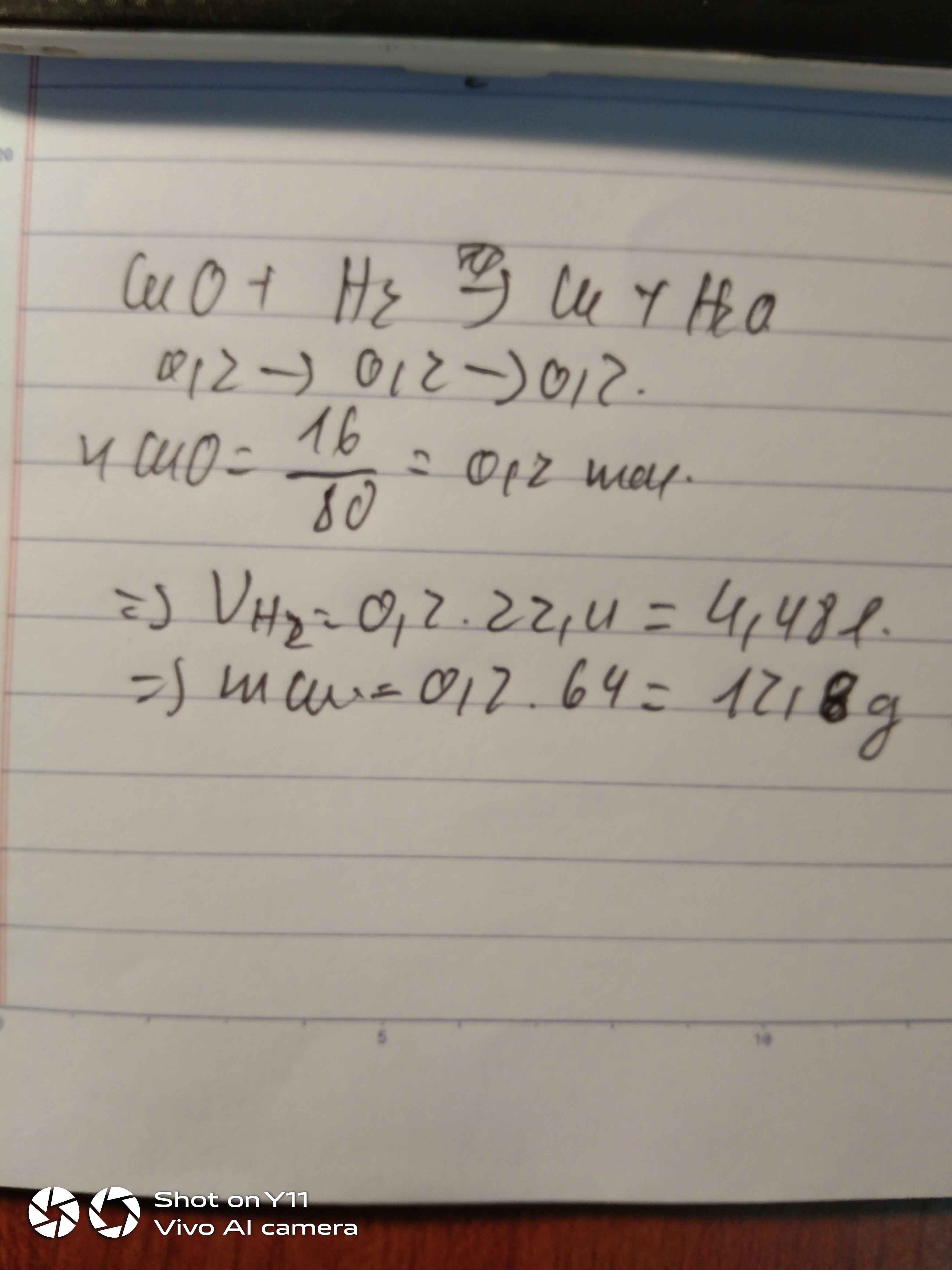khử 160g đồng ii oxit ( Cuo ) bằng khí h2 a)tính thể tích khí h2 tham gia phản ứng b) khối lượng cu sinh ra bao nhiêu gam c) tính khối lượng nước thu được

Những câu hỏi liên quan
Dùng hiđro (H2) để khử 7,2 gam sắt (II) oxit (CuO)
a) Viết phương trình hóa học của phản ứng xảy ra ?
b) Tính khối lượng đồng (Cu) thu được?
c) Tính thể tích khí hiđro đã dùng (ở đktc)?
CuO+H2-to>Cu+H2O
0,09----0,09---0,09
n CuO=\(\dfrac{7,2}{80}\)=0,09 mol
=>m Cu=0,09.64=5,76g
=>VH2=0,09.22,4=2,016l
Đúng 5
Bình luận (0)
\(n_{CuO}=\dfrac{7,2}{80}=0,09mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,09 0,09 0,09 ( mol )
\(m_{Cu}=0,09.64=5,76g\)
\(V_{H_2}=0,09.22,4=2,016l\)
Đúng 2
Bình luận (0)
Dùng hiđro (H2) để khử 7,2 gam sắt (II) oxit (FeO)
a) Viết phương trình hóa học của phản ứng xảy ra ?
b) Tính khối lượng đồng (Cu) thu được?
c) Tính thể tích khí hiđro đã dùng (ở đktc)?
hình như bn ghi sai r đó phải là:đồng oxit mới phải chứ![]()
Đúng 0
Bình luận (0)
a) PTHH: H2 + CuO --t0--> Cu + H2O
b) nCuO = \(\dfrac{m}{M}\) = \(\dfrac{7,2}{80}\) = 0,09 (mol)
nCu = nCuO = 0,09 (mol)
⇒ mCu = n x M = 0,09 x 64 = 5,76 (g)
c) nH2 = nCuO = 0,09 (mol)
⇒ VH2 = n x 22,4 = 0,09 x 22,4 = 2,016 (l)
Đúng 0
Bình luận (0)
Đun nóng 80g CuO với khí H2 thu được kim loại Cu và nước a) tính khối lượng của kim loại thu được b) tính thể tích khí H2 tham gia phản ứng
\(n_{CuO}=\dfrac{80}{80}=1\left(mol\right)\)
Pt : \(CuO+H_2\underrightarrow{t^o}Cu+H_2O|\)
1 1 1 1
1 1 1
a) \(n_{Cu}=\dfrac{1.1}{1}=1\left(mol\right)\)
⇒ \(m_{Cu}=1.64=64\left(g\right)\)
b) \(n_{H2}=\dfrac{1.1}{1}=1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=1.22,4=22,4\left(l\right)\)
Chúc bạn học tốt
Đúng 3
Bình luận (0)
\(n_{CuO}=\dfrac{80}{80}=1\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(1...........1........1\)
\(m_{Cu}=1\cdot64=64\left(g\right)\)
\(V_{H_2}=1\cdot22.4=22.4\left(l\right)\)
Đúng 3
Bình luận (0)
Khử 16g Copper(II) oxide (CuO ) bằng khí hydrogen (H2 ) a.Tính thể tích khí hydrogen (H2 ) tham gia phản ứng? b. Tính khối lượng kim loại tạo thành? Fe= 56, O=16, Cu=64, H=1
Cho 7,2 gam sắt (II) oxit (FeO) khử bằng khí hidro (H2) thu được kim loại sắt (Fe) và nước (H2O)
a) Viết phương trình hóa học
b) Tính khối lượng sắt thu được sau phản ứng
c) Tính thể tích khí hidro tham gia ở dktc
a, \(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
b, \(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
\(n_{Fe}=n_{FeO}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
c, \(n_{H_2}=n_{FeO}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 2
Bình luận (0)
Khử hoàn toàn 12 gam CuO bằng khí H2. Hãy: a/ Viết phương trình hóa học. b/ Tính khối lượng Cu thu được sau phản ứng. c/ Tính thể tích khí H2 cần dùng ở đktc.Giúp mình với !!!
Đọc tiếp
Khử hoàn toàn 12 gam CuO bằng khí H2. Hãy:
a/ Viết phương trình hóa học.
b/ Tính khối lượng Cu thu được sau phản ứng.
c/ Tính thể tích khí H2 cần dùng ở đktc.
Giúp mình với !!!
\(n_{CuO}=\dfrac{m}{M}=\dfrac{12}{64+16}=0,15\left(mol\right)\)
\(a,PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(0,15:0,15:0,15\left(mol\right)\)
\(b,m_{Cu}=n.M=0,15.64=9,6\left(g\right)\)
\(c,V_{H_2}=n.22,4=0,15.22,4=3,36\left(l\right)\)
Đúng 2
Bình luận (1)
Trong phòng thí nghiệm , người ta dùng hidro (H2) để khử 8 gam đồng (II) oxit (cuo) A. Viết phương trình hóa học của phản ứng xảy ra B. Tính khối lượng đồng (cu) thu được C. Tính thể tích hiđro đã dùng (ở đktc)
A. \(H_2+CuO\rightarrow Cu+H_2O\)
B. \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Cu}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)
C. Theo PTHH: \(n_{H_2}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Cho kim loại nhôm phản ứng hoàn toàn với 9,8 gam H2 SO4
a )viết phương trình hóa học xảy ra
b )Tính khối lượng Al đã tham gia
c )Tính thể tích hình H2 (đktc) thu được
d) dùng hết dùng hết lượng khí trên để khử đồng (3) oxit ở nhiệt độ cao tính khối lượng Cu thu được
Cho 2,7g Al tác dụng hết với dung dịch axit clohidric HCL a) Tính thể tích khí H2 sinh ra (đktc). b) Nếu dùng toàn bộ lượng khí H2 từ phản ứng trên để khử 20g đồng (II) oxit CuO thì thu đc bao nhiêu gam sắt. Mong cao nhân nào đó giúp em ạ
a, \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
b, Có lẽ đề hỏi bao nhiêu gam đồng thay vì "bao nhiêu gam sắt" bạn nhỉ?
\(n_{CuO}=\dfrac{20}{80}=0,25\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,25}{1}>\dfrac{0,15}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Cu}=0,15.64=9,6\left(g\right)\)
Đúng 2
Bình luận (0)