Câu 12: Cho 23g Na vào trong 100g nước. Tính C% của dung dịch sau khi Na tan hết

Những câu hỏi liên quan
Tính nồng độ phần trăm của dung dịch thu được khi:a) Hòa tan 17,1 gam muối ăn vào 500g nướcb) Sục 2,24 lít khí HCl (đktc) vào 1 lít nước (D1)c) Trộn 100g dung dịch NaOH 20% với 200g dung dịch NaOH 15%d) 4,6g Na vào 100g nước (PTHH: Na + H2O NaOH + H2)e) 5g đá vôi (CaCO3) vào 200g dung dịch HCl 18,25%f) 100g dung dịch HCl 3,65% với 50g dung dịch NaOH 4%g) 100g dung dịch Na2SO4 14,2% với 50g dung dịch BaCl2 10,4%
Đọc tiếp
Tính nồng độ phần trăm của dung dịch thu được khi:
a) Hòa tan 17,1 gam muối ăn vào 500g nước
b) Sục 2,24 lít khí HCl (đktc) vào 1 lít nước (D=1)
c) Trộn 100g dung dịch NaOH 20% với 200g dung dịch NaOH 15%
d) 4,6g Na vào 100g nước (PTHH: Na + H2O NaOH + H2)
e) 5g đá vôi (CaCO3) vào 200g dung dịch HCl 18,25%
f) 100g dung dịch HCl 3,65% với 50g dung dịch NaOH 4%
g) 100g dung dịch Na2SO4 14,2% với 50g dung dịch BaCl2 10,4%
Cho 23g Na tác dụng với 100g nước. Nồng độ phần trăm của dung dịch thu được là:
A. 23,8 %
B. 30,8%
C. 32,8%
D. 29,8%
Giải thích:
nNa = 23: 23 = 1 (mol)
2Na + 2H2O → 2NaOH + H2↑
1 →1 → 0,5
mdd sau = mNa + mH2O – mH2 = 23 + 100- 0,5.2 = 122g
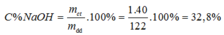
Đáp án C
Đúng 0
Bình luận (0)
a. Tính khối lượng dung dịch thu được khi hòa tan 15 gam NaCl vào 65 gam nước?
b. Ở nhiệt độ 18°C, khi hòa tan hết 53 gam Na₂CO₃ vào 250 gam nước thì được dung dịch bão hòa. Xác định độ tan của muối Na₂CO₃ ở nhiệt độ trên.
a) mdd =15+65=80g
b)
⇒SNa2CO3=\(\dfrac{53}{250}\).100=21,2g
Vậy độ tan của muối Natricacbonat ở 18 độ C là 21,2g
Đúng 1
Bình luận (0)
a. mdd = 15+65 = 80 (g)
b. Độ tan của muối Na2CO3 ở 18^oC là : S = (53 x 100)/250 = 21,2 (gam).
Đúng 1
Bình luận (0)
Hoà tan hết 2,3g Na kim loại vào 97,8g nước . Hãy tính nồng độ % của dung dịch thu được sau phản ứng
Câu 7: Cho 2,3 gam Na vào nước du a) Viết PTHH xảy ra? b) Tính khối lượng chất tan trong dung dịch sau phản ứng? c) Cho tất cả khi thu được ở trên đi qua ống thủy tinh chứa 10 gam CuO nung nóng. Tính khối lượng chất rắn thu được sau khi phản ứng kết thúc.
a) PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
b) Ta có: \(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)=n_{NaOH}\) \(\Rightarrow m_{NaOH}=0,1\cdot40=4\left(g\right)\)
c) PTHH: \(H_2+CuO\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=0,05\left(mol\right)\\n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) CuO còn dư, Hidro p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Cu}=0,05\left(mol\right)\\n_{CuO\left(dư\right)}=0,075\left(mol\right)\end{matrix}\right.\) \(\Rightarrow m_{rắn}=m_{Cu}+m_{CuO}=9,2\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 2,3g Na tan hết trong 47,8ml nước thu được dung dịch NaOH và có khí H2 thoát ra. Tính nồng độ C% của dung dịch NaOH?
mH2O = 47,8 . 1 = 47,8 (g)
nH2O = 47,8/18
nNa = 2,3/23 = 0,1 (mol)
PTHH: 2Na + 2H2O -> 2NaOH + H2
0,1 ---> 0,1 ---> 0,1 ---> 0,05
mNaOH = 0,1 . 40 = 4 (g)
mH2 = 0,05 . 2 = 0,1 (g)
mdd (sau p/ư) = 47,8 + 2,3 - 0,1 = 50 (g)
C%NaOH = 4/50 = 8%
Đúng 2
Bình luận (0)
ĐỀ hỏi nồng độ mol hay nồng độ chất tan vậy, nếu hỏi nồng độ chất tan thì đề lỗi
Đúng 1
Bình luận (0)
Câu 6: Tính nồng độ của các chất trong các trường hợp sau
a/ C% của dung dịch khi hòa tan 15g NaCl vào 185g nước
b/ Trộn 100g dung dịch HNO3 18,9% với 200g dung dịch HNO3 6,3%
c/ Hòa tan 5,85 g NaCl vào 100ml nước. Tính CM
d/ Trộn 200ml dung dịch KOH 2M với 200ml dung dịch KOH 0,2M
e/ Cho thêm 50g nước vào 150g dung dịch NaOH 16%.Tính C% ?
\(a,C\%_{NaCl}=\dfrac{15}{15+185}.100\%=7,5\%\\ b,m_{HNO_3}=\dfrac{18,9}{100}.100+\dfrac{6,3}{100}.200=31,5\left(g\right)\\ m_{ddHNO_3}=100+200=300\left(g\right)\\ C\%_{HNO_3}=\dfrac{31,5}{300}.100\%=10,5\%\)
\(c,n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\\ C_{M\left(NaCl\right)}=\dfrac{0,1}{0,1}=1M\\ d,n_{KOH}=2.0,2+0,2.0,2=0,44\left(mol\right)\\ V_{ddKOH}=0,2+0,2=0,4\left(l\right)\\ C_{M\left(KOH\right)}=\dfrac{0,44}{0,4}=1,1M\\ e,m_{NaOH}=\dfrac{150.16}{100}=24\left(g\right)\\ m_{ddNaOH}=50+150=200\left(g\right)\\ C\%_{NaOH}=\dfrac{24}{200}.100\%=12\%\)
Đúng 1
Bình luận (0)
Tính nồng độ % của các chất trong dung dịch thu được trong các thí nghiệm sau:
a/ Hòa tan hết 12,4 gam Na2O vào 50 gam nước.
b/ Hòa tan hết hỗn hợp gồm 16 gam NaOH và 4,6 gam Na vào 100 gam nước.
c/ Cho 9,2 gam Na vào 100 gam dung dịch HCl 7,3%.
a, \(n_{Na_2O}=\dfrac{12,4}{62}=0,2\left(mol\right)\)
PTHH: Na2O + H2O ---> 2NaOH
0,2------------------>0,4
\(\Rightarrow C\%_{NaOH}=\dfrac{0,4.40}{12,4+50}.100\%=25,64\%\)
b, \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O ---> 2NaOH + H2
0,2------------------->0,2------->0,1
\(\Rightarrow C\%_{NaOH}=\dfrac{0,2.40+16}{100+16+4,6-0,1.2}.100\%==20\%\)
c, \(n_{Na}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
\(n_{HCl}=\dfrac{100.7,3\%}{36,5}=0,2\left(mol\right)\)
PTHH:
2Na + 2HCl ---> 2NaCl + H2
0,2<-----0,2-----------0,2--->0,1
2Na + 2H2O ---> 2NaOH + H2
0,2------------------>0,2----->0,1
\(\Rightarrow m_{dd}=9,2+100-\left(0,1+0,1\right).2=108,8\left(g\right)\\ \Rightarrow\left\{{}\begin{matrix}C\%_{NaCl}=\dfrac{0,2.58,5}{108,8}.100\%=10,75\%\\C\%_{NaOH}=\dfrac{0,2.40}{108,8}.100\%=7,35\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Cho 1 mẩu Na cho vào nước (Dnước = 1g/ml) thấy có 1 khí bay ra và tạo 1 dung dịch có tính kiềm. Tính C% của dung dịch sau phản ứng. Biết rằng khối lượng của Na là 23g