dẫn từ từ 6,72 lít khí co2 qua 500ml dung dịch koh 1m,tính khối lượng muối thu được sau pứ

Những câu hỏi liên quan
Dẫn 6,72(l) khí CO2(đktc) qua 500ml dung dịch NaOH 1(M). Tính khối lượng muối thu được sau phản ứng?
nCO2=0,3(mol)
nNaOH=0,5(mol)
Vì: 1< nNaOH/nCO2=0,5/0,3=1,67<2
=> Sp thu được là hỗn hợp 2 muối
PTHH: 2 NaOH + CO2 -to-> Na2CO3 + H2O
2x____________x_________x(mol)
NaOH + CO2 -> NaHCO3
y_____y______y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}2x+y=0,5\\x+y=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
=> m(muối)= mNa2CO3 + mNaHCO3=0,2.106+0,1.84= 29,6(g)
Đúng 3
Bình luận (0)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(PTHH:CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
Mol: 0,3 0,3
\(\Rightarrow m_{Na_2CO_3}=0,3.106=31,8\left(g\right)\)
Đúng 0
Bình luận (1)
nCO2= \(\dfrac{V}{22,4}\)=\(\dfrac{6,72}{22,4}\)=0,3 (mol).
nNaOH= CM.V= 1 . 0,5= 0,5(mol).
\(\dfrac{n_{NaOH}}{n_{CO2}}\)=\(\dfrac{0,5}{0,3}\)= 1,67 mà 1<1,67<2 ⇒ tạo 2 muối (1) và (2).
CO2 + NaOH -> NaHCO3 (1)
CO2 + NaOH -> Na2CO3 + H2O (2)
Lập TLSS: \(\dfrac{0,3}{1}\) > \(\dfrac{0,5}{0,1}\)
⇒Tính theo NaOH.
mNaHCO3= 0,5 . 84 = 42g
mNa2CO3= 0,5 . 106= 53g
Đúng 0
Bình luận (2)
Dẫn từ từ 6,72 lít khí
C
O
2
ở đltc vào 300 ml dung dịch NaOH 1,2 M. Tính tổng khối lượng các muối trong dung dịch thu được và khối lượng kết tủa khi cho
B
a
C
l
2
dư vào dung dịch sau khi hấp thụ
C
O
2
A. 26,52 g; 10,15 g B. 20g; 11,82g C. 26,52 g; 11,82 g D. 11,82 g; 26,52 g
Đọc tiếp
Dẫn từ từ 6,72 lít khí C O 2 ở đltc vào 300 ml dung dịch NaOH 1,2 M. Tính tổng khối lượng các muối trong dung dịch thu được và khối lượng kết tủa khi cho B a C l 2 dư vào dung dịch sau khi hấp thụ C O 2
A. 26,52 g; 10,15 g
B. 20g; 11,82g
C. 26,52 g; 11,82 g
D. 11,82 g; 26,52 g
cho 6,72 lít khí co2 (đktc) vào cốc đựng 500ml dung dịch koh 1M. sau phản ứng thu thêm tiếp lượng dư cacl2 vào cốc thu được m gam kết tủa. tính m?
\(n_{KOH} = 0,5.1 = 0,5(mol)\\ n_{CO_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ n_{K_2CO_3} = a(mol) ; n_{KHCO_3} = b(mol)\\ 2KOH + CO_2 \to K_2CO_3 + H_2O\\ KOH + CO_2 \to KHCO_3\\ n_{KOH} = 2a + b = 0,5\\ n_{CO_2} = a + b = 0,3\\ \Rightarrow a = 0,2 ; b = 0,1\\ CaCl_2 + K_2CO_3 \to CaCO_3 + 2KCl\\ n_{CaCO_3} = n_{K_2CO_3} = 0,2(mol)\\ \Rightarrow m = 0,2.100 = 20(gam) \)
Đúng 2
Bình luận (0)
Dẫn 6,72 lít khí CO2 qua 200g dung dịch KOH 14%
a) Viết Pthh
b) Tính khối lượng muối tạo thành
c) Tính nồng độ % các chất trong dung dịch sau phản ứng
\(n_{CO_2}=0,3\left(mol\right);n_{KOH}=0,5\left(mol\right)\)
Lập tỉ lệ : \(\dfrac{n_{KOH}}{n_{CO_2}}=\dfrac{0,5}{0,3}=1,67\)=> Tạo 2 muối KHCO3 và K2CO3
\(CO_2+KOH\rightarrow KHCO_3\)
\(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
Gọi x,y lần lượt là số mol KHCO3 và K2CO3 ta có
\(\left\{{}\begin{matrix}x+y=0,3\\x+2y=0,5\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> \(m_{KHCO_3}=0,1.100=10\left(g\right);m_{K_2CO_3}=0,2.138=27,6\left(g\right)\)
c) \(C\%_{KHCO_3}=\dfrac{10}{0,3.44+200}.100=4,69\%\)
\(C\%_{K_2CO_3}=\dfrac{27,6}{0,3.44+200}.100=12,95\%\)
Đúng 3
Bình luận (0)
Xác định khối lượng kết tủa thu được khi dẫn từ từ 6,72 lít khí CO2 (đktc) vào 400ml dung dịch Ca(OH)2 1M?
A. 30 gam
B. 40 gam
C. 35 gam
D. 45 gam
Đáp án A
nCO2= 6,72/22,4= 0,3 mol;
nCa(OH)2= 0,4.1= 0,4 mol
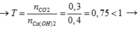
Sau phản ứng thu được muối trung hòa CaCO3
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có: 0,3 < 0,4 nên CO2 phản ứng hết, Ca(OH)2 còn dư
Ta có: nCaCO3= nCO2= 0,3 mol → mCaCO3= 0,3.100= 30,0 gam
Đúng 0
Bình luận (0)
Dẫn từ từ 0,84 lít khí CO2 (đktc) vào 200ml dung dịch KOH vừa đủ, sản phẩm thu được là K2CO3 và nước.
a) Xác định khối lượng muối thu được sau phản ứng.
b) Tính nồng độ mol/l của dung dịch KOH đem dùng?
Can u help me?!!!?
a, Ta có: \(n_{CO_2}=\dfrac{0,84}{22,4}=0,0375\left(mol\right)\)
PT: \(CO_2+2KOH\rightarrow K_2CO_3+H_2O\)
\(n_{K_2CO_3}=n_{CO_2}=0,0375\left(mol\right)\)
\(\Rightarrow m_{K_2CO_3}=0,0375.138=5,175\left(g\right)\)
b, \(n_{KOH}=2n_{CO_2}=0,075\left(mol\right)\)
\(\Rightarrow C_{M_{KOH}}=\dfrac{0,075}{0,2}=0,375\left(M\right)\)
Đúng 4
Bình luận (0)
Dẫn 4,48 (l) CO2 (đktc) qua 300 ml dung dịch KOH 1M. Tính khối lượng muối thu được sau phản ứng
Xem chi tiết
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\\ n_{KOH}=0,3.1=0,3mol\\ T=\dfrac{0,3}{0,2}=1,5\)
⇒1<T<2, tạo muối KHCO3, K2CO3
\(n_{K_2CO_3}=a;n_{KHCO_3}=b\\ 2KOH+CO_2\rightarrow K_2CO_3+H_2O\\ KOH+CO_2\rightarrow KHCO_3\\ \Rightarrow\left\{{}\begin{matrix}2a+b=0,3\\a+b=0,2\end{matrix}\right.\\ \Rightarrow a=b=0,1\\ m_{muối}=0,1\left(138+100\right)=23,8g\)
Đúng 2
Bình luận (0)
dẫn từ từ 6,72 lít khí CO2(đktc) vào 300g dung dịch KOH 16,8%. tính C% chất tan có trong dung dịch thu được
\(n_{CO_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(n_{KOH}=\dfrac{300\cdot16.8\%}{56}=0.9\left(mol\right)\)
\(T=\dfrac{0.9}{0.3}=3\)
=> Tạo ra K2CO3 , KOH dư
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
\(0.6...........0.3.............0.3\)
\(m_{dd}=0.3\cdot44+300=313.2\left(g\right)\)
\(C\%_{K_2CO_3}=\dfrac{0.3\cdot138}{313.2}\cdot100\%=13.22\%\)
\(C\%_{KOH\left(dư\right)}=\dfrac{\left(0.9-0.6\right)\cdot56}{313.2}\cdot100\%=5.36\%\)
Đúng 4
Bình luận (0)
dẫn từ từ 6,72 lít khí so2 (đktc) vào một dung dịch có hoà tan 44,8g KOH. a) Xác định các chất có trong dung dịch sau phản ứng. b)Hãy tính khối lượng các chất thu được sau phản ứng
a)
$n_{KOH} = \dfrac{44,8}{56} = 0,8(mol)$
$n_{SO_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
Ta thấy : $n_{KOH} : n_{SO_2} = 0,8 : 0,3 = 2,67 > 2$ nên dung dịch sau phản ứng có : $KOH$ dư ; $K_2SO_3$
b)
$n_{K_2SO_3} = n_{SO_2} = 0,3(mol)$
$\Rightarrow m_{K_2SO_3} = 0,3.158 = 47,4(gam)$
$n_{KOH\ dư} = 0,8 - 0,3.2 = 0,2(mol)$
$\Rightarrow m_{KOH\ dư} = 0,2.56 = 11,2(gam)$
Đúng 4
Bình luận (0)

























