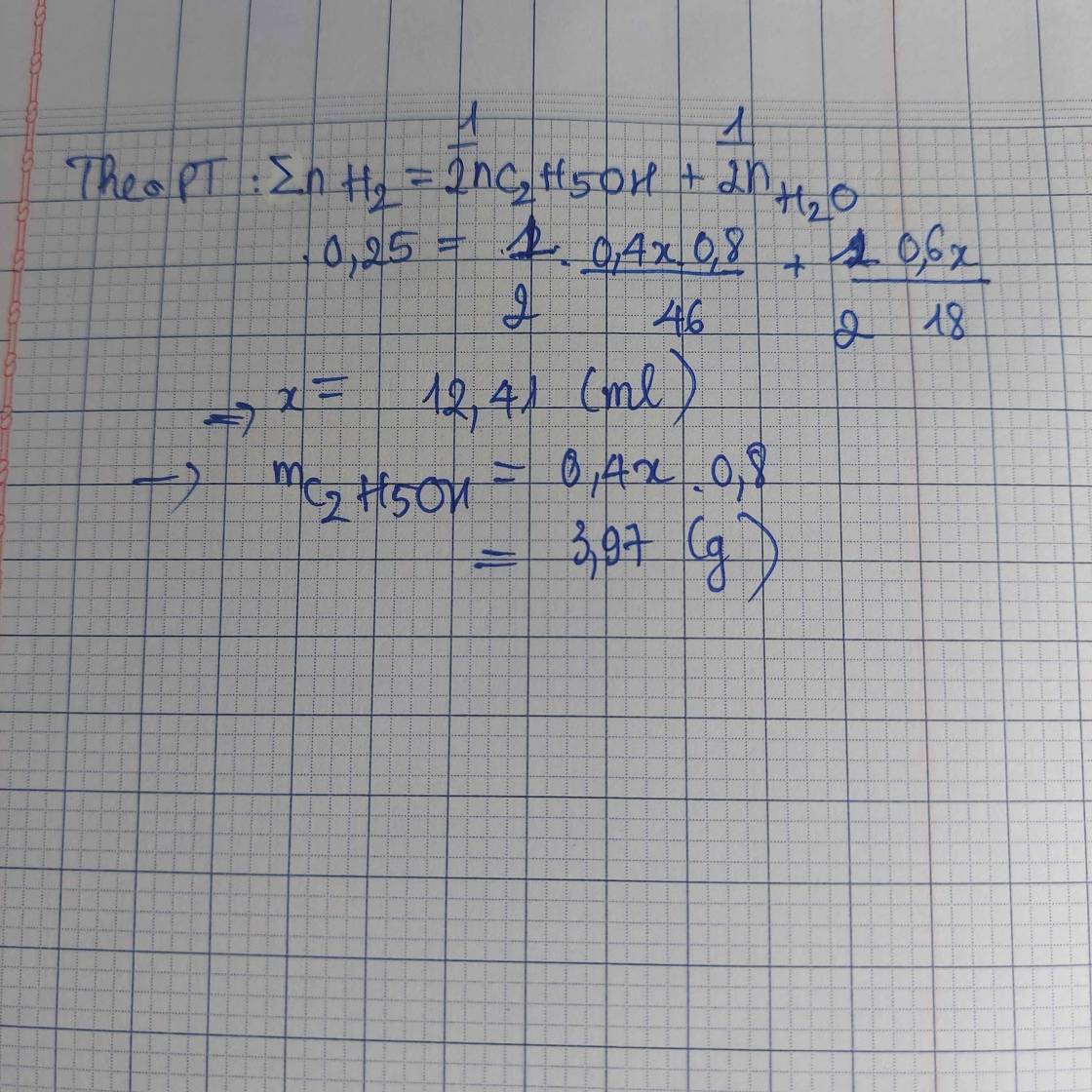cho 0,5 lít đ rượu etylic 30 độ pứ với na dư,sau pứ thu được bao nhiêu lít h2,cho biết d rượu=0,8,d nước =1

Những câu hỏi liên quan
Câu 9. Cho 0,5 lít dd rượu etylic 300 pư với Na dư, sau pư thu được bao nhiêu lít H2 (đktc), cho biết Drượu = 0,8 (g/ml). Dnước = 1 (g/ml).
\(m_{C_2H_5OH\left(nguyên.chất\right)}=\dfrac{0,5.30}{100}=0,15l=150ml\)
\(\rightarrow m_{H_2O}=500-150=350ml\)
\(m_{C_2H_5OH}=150.0,8=120g\)
\(m_{H_2O}=350.1=350g\)
\(\left\{{}\begin{matrix}n_{C_2H_5OH}=\dfrac{120}{46}=2,6mol\\n_{H_2O}=\dfrac{350}{18}=19,44mol\end{matrix}\right.\)
\(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\)
2,6 1,3 ( mol )
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
19,44 9,72 ( mol )
\(V_{H_2}=\left(1,3+9,72\right).22,4=246,848l\)
Đúng 1
Bình luận (0)
\(0,5lít=500ml\)
\(m_{C_2H_5OH}=500.0,8=400g\)
\(n_{C_2H_5OH}=\dfrac{400}{46}=8,69mol\)
\(n_{Na}=\dfrac{300}{23}=12,04mol\)
\(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\)
8,69 < 12,04 ( mol )
8,69 8,69 ( mol )
\(V_{H_2}=8,96.22,4=200,704l\)
Đúng 0
Bình luận (0)
từ 36g glucozo lên men rượu thì thu đc bao nhieu lít đ rượu 5,75 độ,biết hiệu suất pứ=80%,d rượu=0,8
\(n_{C_6H_{12}O_6}=\dfrac{36}{180}=0,2\left(mol\right)\)
PTHH: C6H12O6 \(\xrightarrow{ \text{men rượu} } \) 2CO2 + 2C2H5OH
0,2 ----------------------------> 0,4
\(\rightarrow m_{C_2H_5OH}=0,4.80\%.46=14,72\left(g\right)\\ \rightarrow V_{C_2H_5OH}=\dfrac{14,72}{0,8}=18,4\left(g\right)\\ \rightarrow V_{ddC_2H_5OH}=\dfrac{18,4}{5,75\%}=320\left(ml\right)\)
Đúng 2
Bình luận (0)
\(n_{C_6H_{12}O_6}=\dfrac{36}{180}=0,2mol\)
\(C_6H_{12}O_6\underrightarrow{lênmen}2C_5H_{12}OH+2CO_2\)
0,2 0,4
Thực tế: \(n_{C_5H_{12}OH}=0,4\cdot80\%=0,32mol\)
\(\Rightarrow m_{rượu}\)(nguyên chất)=\(0,32\cdot46=14,72g\)
\(V_{rượu}=\dfrac{m}{D}=\dfrac{14,72}{0,8}=18,4ml\)
Độ rượu: \(5,75^o=\dfrac{18,4}{V_{ddrượu}}\cdot100\%\Rightarrow V_{ddrượu}=320ml\)
Đúng 1
Bình luận (0)
Cho 10,1 gam dung dịch rượu etylic tác dụng với kim loại Na dư thu được 2,8 lít
H
2
(đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml và của nước là 1 g/ml. Xác định độ rượu đem tham gia phản ứng? A.
92
,
74
o
B.
96
o
C.
73
,
92
0
D.
97
,
24...
Đọc tiếp
Cho 10,1 gam dung dịch rượu etylic tác dụng với kim loại Na dư thu được 2,8 lít H 2 (đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml và của nước là 1 g/ml. Xác định độ rượu đem tham gia phản ứng?
A. 92 , 74 o
B. 96 o
C. 73 , 92 0
D. 97 , 24 o
Đáp án: A
Vì dung dịch rượu gồm rượu etylic và nước nên ta gọi:
n H 2 O = x m o l và n C 2 H 5 O H = y m o l
PTHH:
2 N a + 2 H 2 O → 2 N a O H + H 2 ↑ ( 1 )
x mol → 0,5.x mol
2 N a + 2 C 2 H 5 O H → 2 C 2 H 5 O N a + H 2 ↑
y mol → 0,5.y mol
Ta có hệ phương trình:
18 x + 46 y = 10 , 1 0 , 5 x + 0 , 5 y = 0 , 125 ⇒ x = 0 , 05 y = 0 , 2
V C 2 H 5 O H nguyên chất = m D = 0 , 2 . 46 0 , 8 = 11 , 5 m l
V H 2 O = m D = 10 , 1 - 9 , 2 1 = 0 , 9 m l
=> V d d r ư ợ u = V H 2 O + V C 2 H 5 O H = 0,9 + 11,5 = 12,4 ml
=> Độ rượu D 0 = V C 2 H 5 O H V d d r u o u . 100 = 11 , 5 12 , 4 . 100 = 92 , 74 0
Đúng 0
Bình luận (0)
Đốt cháy 37,75 ml rượu etylic cho sản phẩm qua nước vôi trong dư được 100g kết tủa
a) Xác định độ rượu trên biết Drượu, D H2O
b) Cho dung dịch trên tác dụng với Na lấy dư thì thu được bao nhiêu lít H2 ở đkc
c) Nếu dùng m g rượu 45° tác dụng với Na thì cần bao nhiêu g rượu để thu được thể tích h2 ở trên
Hòa tan m gam rượu etylic ( D = 0,8 g/ml) vào 108 ml nước ( D= 1 g/ml) tạo thành dung dịch A. Cho dung dịch A tác dụng với kim loại Na dư, thu được 85,12 lít khí H2 (đktc). Tính giá trị m và nồng độ mol của rượu etylic
nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
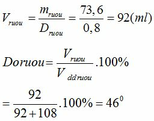
Đúng 0
Bình luận (0)
Cho m gam dung dịch rượu etylic nồng độ 29,87% tác dụng hết với Na (dư) thu được 11,76 lít khí H2 (đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml. Độ rượu của dung dịch trên là
m C2H5OH = m.29,87% = 0,2987m(gam)
=> n C2H5OH = 0,2987m/46 (mol)
m H2O = m - 0,2987m = 0,7013m(gam)
=> n H2O = 0,7013m/18(mol)
$2C_2H_5OH + 2Na \to 2C_2H_5ONa + H_2$
$2Na + 2H_2O \to 2NaOH + H_2$
n H2 = 1/2 n C2H5OH + 1/2 H2O = 11,76/22,4 = 0,525(mol)
=> 1/2 . 0,2987m/46 + 1/2 . 0,7013m/18 = 0,525
=> m = 23,1(gam)
Suy ra :
m C2H5OH = 0,2987.23,1 = 6,9(gam)
V C2H5OH = 6,9/0,8 = 8,625(ml)
m H2O = 0,7013.23,1 = 16,2(gam)
V H2O = 16,2/1 = 16,2(ml)
Vậy :
Đr = V C2H5OH / V(dd) .100 = 8,625/(8,625 + 16,2) .100 = 34,74o
Đúng 2
Bình luận (1)
Để xác định độ rượu của một loại ancol etylic (ký hiệu rượu X) người ta lấy 10ml rượu X cho tác dụng hết với Na dư thu được 2,564 lít H2 (đktc). Độ rượu X gần nhất với giá trị nào (biết dancol etylic 0,8 g/ml) A. 87,50. B. 85,60. C. 91,00. D. 92,50.
Đọc tiếp
Để xác định độ rượu của một loại ancol etylic (ký hiệu rượu X) người ta lấy 10ml rượu X cho tác dụng hết với Na dư thu được 2,564 lít H2 (đktc). Độ rượu X gần nhất với giá trị nào (biết dancol etylic = 0,8 g/ml)
A. 87,50.
B. 85,60.
C. 91,00.
D. 92,50.
Cho 20,2 gam rượu tác dụng với Na lấy dư thấy thoát ra 5,6 lít khí H2 (đktc)
a. Xác định độ rượu?
b. Nếu dùng rượu etylic 40o cho tác dụng với Na thì cần bao nhiêu gam rượu để thu được thể tích H2 nói trên?
Dung dịch A là hỗn hợp rượu etylic và nước. Cho 20,2 g A tác dụng với Na (dư) thấy thoát ra 5,6 lít khí H2 ( đktc). Xác định độ rượu, biết khối lượng riêng của rượu etylic là 0,8 gam/ml, của nước là 1g/ml.
Gọi \(\left\{{}\begin{matrix}n_{C_2H_5OH}=a\left(mol\right)\\n_{H_2O}=b\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH:
2C2H5OH + 2Na ---> 2C2H5ONa + H2
a --------------------------------------------> 0,5a
2H2O + 2Na ---> 2NaOH + H2
b --------------------------------> 0,5b
Hệ pt \(\left\{{}\begin{matrix}46a+18b=20,2\\0,5a+0,5b=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,4\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{C_2H_5OH}=0,4.46=18,4\left(g\right)\\m_{H_2O}=0,1.18=1,8\left(g\right)\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}V_{C_2H_5OH}=\dfrac{18,4}{0,8}=23\left(ml\right)\\V_{H_2O}=\dfrac{1,8}{1}=1,8\left(ml\right)\end{matrix}\right.\)
=> Độ rượu là: \(\dfrac{23}{23+1,8}=92,74^o\)
Đúng 2
Bình luận (0)