Nêu hiện tượng và viết pthh
1. Cho mẩu kim loại sodium (hoặc Potassium) vào rượu Ethanol
2.Thả mẩu kim loại Magesium Mg vào gốc đựng giấm (dd loãng của Acetic acid)
3.Cho Acetic acid vào ống nghiệm đựng bột CaO

Những câu hỏi liên quan
Chuẩn bị: Dung dịch CH3COOH 1 M, phoi bào magnesium; ống nghiệm.
Tiến hành: Cho 1 – 2 mL dung dịch acetic acid 1M vào ống nghiệm, sau đó thêm vào vài mẩu magnesium.
Yêu cầu: Quan sát, mô tả hiện tượng xảy ra và giải thích.
Tham khảo
-Hiện tượng: phoi bào magnesium tan, xuất hiện bọt khí.
-Giải thích: Acetic acid phản ứng với magnesium, làm magnesium tan và tạo khí hydrogen.
2CH3COOH + Mg → 2(CH3COO)2Mg + H2↑
Đúng 1
Bình luận (0)
Nêu hiện tượng và viết phương trình hóa học xảy ra khi cho:
a) Iron cháy trong lọ chứa khí Oxygen.
b) Dẫn luồng khí Hydrogen đi qua bột copper (II) oxide, đun nóng.
c) Cho kim loại Zinc vào ống nghiệm đựng dung dịch hydrochloric acid (HCl)
sắt cháy mãnh liệt và bắn ra vài hạt vụn
3Fe + 2O2 -to-> Fe3O4
đồng chuyển từ màu đen sang màu đỏ
CuO + H2 -to-> Cu + H2O
kẽm sủi bọt và giải phóng khí hidro
Zn + 2HCl -> ZnCl2 + H2
Đúng 1
Bình luận (1)
Nêu hiện tượng xảy ra trong các thí nghiệm dưới đây và viết phương trình hóa học để giải thích?
a) Cho một mảnh kẽm vào ống nghiệm đựng dung dịch axit clohidric
b) Cho một luồng khí hidro qua bột đồng (II) oxit nung nóng
c) Cho một mẩu kim loại Natri vào cốc nước
d) Cho vào bát sứ một cục nhỏ vôi sống (CaO) rồi rót một ít nước vào vôi sống
a) Cho một mảnh kẽm vào ống nghiệm đựng dung dịch axit clohidric
Zn+HCl->ZnCl2+H2
=>Zn tan có khí thoát ra
b) Cho một luồng khí hidro qua bột đồng (II) oxit nung nóng
H2+CuO-to>Cu+H2O
=>chất rắn chuyển từ đen sang đỏ
c) Cho một mẩu kim loại Natri vào cốc nước
2Na+2H2O->2NaOH+H2
=>Na tan có khí thoát ra
d) Cho vào bát sứ một cục nhỏ vôi sống (CaO) rồi rót một ít nước vào vôi sống
CaO+H2O->Ca(OH)2
=> CaO tan , có nhiệt độ cao
Đúng 2
Bình luận (0)
Chuẩn bị: dung dịch acetic acid 10%, dung dịch Na2CO3 10%, bột Mg; ống nghiệm, giấy quỳ.Tiến hành:1. Phản ứng với chất chỉ thị:Nhỏ một giọt dung dịch acetic acid 10% lên mẩu giấy quỳ.Quan sát và mô tả sự thay đổi màu sắc của giấy quỳ.2. Phản ứng với kim loại:- Cho 1 – 2 mL dung dịch acetic acid 10% vào ống nghiệm (1).- Thêm tiếp một ít bột Mg vào ống nghiệm (1).Quan sát và mô tả hiện tượng xảy ra trong ống nghiệm (1).3. Phản ứng với muối:- Cho 1 – 2 mL dung dịch Na2CO3 10% vào ống nghiệm (2).- T...
Đọc tiếp
Chuẩn bị: dung dịch acetic acid 10%, dung dịch Na2CO3 10%, bột Mg; ống nghiệm, giấy quỳ.
Tiến hành:
1. Phản ứng với chất chỉ thị:
Nhỏ một giọt dung dịch acetic acid 10% lên mẩu giấy quỳ.
Quan sát và mô tả sự thay đổi màu sắc của giấy quỳ.
2. Phản ứng với kim loại:
- Cho 1 – 2 mL dung dịch acetic acid 10% vào ống nghiệm (1).
- Thêm tiếp một ít bột Mg vào ống nghiệm (1).
Quan sát và mô tả hiện tượng xảy ra trong ống nghiệm (1).
3. Phản ứng với muối:
- Cho 1 – 2 mL dung dịch Na2CO3 10% vào ống nghiệm (2).
- Thêm tiếp 1 – 2 mL dung dịch acetic acid 10% vào ống nghiệm (2).
Thực hiện yêu cầu sau:
a) Quan sát và mô tả hiện tượng xảy ra trong ống nghiệm (2).
b) Viết phương trình hoá học của các phản ứng xảy ra trong các thí nghiệm trên và giải thích hiện tượng.
Tham khảo:
1. Quỳ tím chuyển sang màu đỏ vì acetic acid có tính acid.
2. Kim loại tan dần tạo thành dung dịch màu không màu và có khí không màu thoát ra.
- Mg + 2CH3COOH → (CH3COO)2Mg + H2
3. Tạo dung dịch không màu và có khí thoát ra.
- 2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
Đúng 1
Bình luận (0)
Nêu hiện tượng và viết phương trình khi cho kim loại Zinc vào ống nghiệm chứa hydrochloric acid, sau đó đốt cháy sản phẩm thu được.
Zn + 2HCl ➝ ZnCl2 + H2
Hiện tượng: viên kẽm tan dần, có bọt khí không màu thoát ra.
Đốt cháy khí H2 sẽ thấy có ngọn lửa màu xanh nhạt
2H2 + O2 ➝ 2H2O
Đúng 0
Bình luận (0)
Nêu hiện tượng và pthh
a)Cho khí Ethylene?Acetylene đi qua dung dịch Bromine Br2
b)Cho Acetic acid vào ống nhghieemj có chứa đấ vôi vooi Caco3
a) dd Br2 nhạt màu dần
C2H4 + Br2 --> C2H4Br2
C2H2 + 2Br2 --> C2H2Br4
b) Chất rắn tan dần, sủi bọt khí
2CH3COOH + CaCO3 --> (CH3COO)2Ca + CO2 + H2O
Đúng 2
Bình luận (0)
Chuẩn bị: Cồn 96°, acetic acid nguyên chất, dung dịch H2SO4 đặc, dung dịch NaCl bão hoà, ống nghiệm.Tiến hành: Cho 1 mL cồn 96° vào trong ống nghiệm. Cho tiếp vào trong ống nghiệm 1 mL acetic acid nguyên chất. Thêm vào ống nghiệm 1 – 2 giọt dung dịch sulfuric acid đậm đặc và lắc đều, dùng bông sạch nút miệng ống nghiệm. Sau đó, đun cách thuỷ trong cốc thuỷ tinh ở nhiệt độ 65 – 70 °C trong khoảng thời gian 5 – 7 phút. Làm lạnh ống nghiệm rồi cho thêm vào 2 mL dung dịch sodium chloride bão hoà. Để...
Đọc tiếp
Chuẩn bị: Cồn 96°, acetic acid nguyên chất, dung dịch H2SO4 đặc, dung dịch NaCl bão hoà, ống nghiệm.
Tiến hành: Cho 1 mL cồn 96° vào trong ống nghiệm. Cho tiếp vào trong ống nghiệm 1 mL acetic acid nguyên chất. Thêm vào ống nghiệm 1 – 2 giọt dung dịch sulfuric acid đậm đặc và lắc đều, dùng bông sạch nút miệng ống nghiệm. Sau đó, đun cách thuỷ trong cốc thuỷ tinh ở nhiệt độ 65 – 70 °C trong khoảng thời gian 5 – 7 phút. Làm lạnh ống nghiệm rồi cho thêm vào 2 mL dung dịch sodium chloride bão hoà. Để yên ống nghiệm.
Yêu cầu: Quan sát, mô tả hiện tượng và giải thích.
Chú ý an toàn: Cẩn thận khi làm việc với dung dịch H2SO4 đặc.
Hiện tượng: Phản ứng sinh ra chất lỏng, nhẹ hơn nước, có mùi thơm đặc trưng.
Giải thích bằng phương trình hoá học:
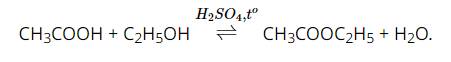
Đúng 0
Bình luận (0)
Nêu hiện tượng và viết phương trình hóa học xảy ra đối với các thí nghiệm sau: a) Cho 1 mẫu Na vào ống nghiệm đựng cồn 900 b) Nhỏ dung dịch H2SO4 loãng vào dung dịch muối Na2SiO3. c) Đưa một mẩu giấy quỳ tím vào cốc đựng nước clo. d) Cho Cu(OH)2 vào cốc đựng dung dịch CH3COOH dư
Đọc tiếp
Nêu hiện tượng và viết phương trình hóa học xảy ra đối với các thí nghiệm sau:
a) Cho 1 mẫu Na vào ống nghiệm đựng cồn 900
b) Nhỏ dung dịch H2SO4 loãng vào dung dịch muối Na2SiO3.
c) Đưa một mẩu giấy quỳ tím vào cốc đựng nước clo.
d) Cho Cu(OH)2 vào cốc đựng dung dịch CH3COOH dư
a) Mẩu Na chạy tròn trên miệng ống nghiệm, tan dần đến hết, có sủi bọt khí thoát ra ngoài
2Na + 2C2H5OH → 2C2H5ONa + H2↑
b) Hiện tượng: xuất hiện kết tủa trắng keo của H2SiO3
H2SO4 + Na2SiO3 → Na2SO4 + H2SiO3↓
c) Hiện tượng: quỳ tím đổi sang màu đỏ, sau đó mất màu
H2O + Cl2 ⇆ HCl + HClO
HCl làm quỳ tím chuyển sang màu đỏ, HClO có tính oxi hóa mạnh nên làm quỳ mất màu.
d) Hiện tượng: Cu(OH)2 tan dần đến hết, dung dịch thu được có màu xanh lam đậm
Cu(OH)2 + 2CH3COOH → (CH3COO)2Cu + 2H2O
Đúng 0
Bình luận (0)
Bài 1: Công thức cấu tạo đầy đủ của
a) Etyl clorua
b) Etyl axetat
Bài 2: Nêu hiện tượng và viết PTHH xảy ra trong các thí nghiệm sau
a) Thả mẫu kim loại Na vào cốc đựng rượu etylic C2H5OH
b) Cho CaCO3 vào cốc đựng dung dịch axit axetic CH3COOH
Bài 2 :
a) Natri tan dần, xuất hiện khí không màu không mùi thoát ra :
\(2Na + 2C_2H_5OH \to 2C_2H_5ONa + H_2\)
b) CaCO3 tan dần, xuất hiện khí không màu không mùi thoát ra :
\(CaCO_3 + 2CH_3COOH \to (CH_3COO)_2Ca + CO_2 + H_2O\)
Đúng 2
Bình luận (0)























