phân hủy 15,8gam KMnO4 thì thu được bao nhiêu lít oxi ở đktc ?
Phân hủy bao nhiêu gam KClO3 và KMnO4 để thu được 6,72 lít oxi ở đktc
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,6<------------------------------0,3
=> mKMnO4 = 0,6.158 = 94,8 (g)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,2<----------------0,3
=> mKClO3 = 0,2.122,5 = 24,5 (g)
a. PTHH: \(KMnO_4\rightarrow^{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
b. \(H=100\%\)
\(n_{KMnO_4}=\frac{3,6}{158}=0,023mol\)
Theo phương trình \(n_{O_2}=0,5n_{KMnO_4}=0,046mol\)
\(\rightarrow V_{O_2}=0,0115.22,4.100\%=0,2576l\)
c. H = 80%
\(\rightarrow V_{O_2}=0,0115.22,4.80\%=0,20608l\)
Phân hủy KMnO4,thu được K2Mn04;MnO2 và 2,24 lít khí oxi ở đktc. a)Viết phương trình hóa học xảy ra ? b)Tính khối lượng KMnO4 cần đem đi phân hủy? c)Nếu dùng hết lượng oxi trên tác dụng với thể tích của H2 là bao nhiêu lít để tạo ra hỗn hợp nổ mạnh.
nO2 = 2,24/22,4 = 0,1 (mol)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2
nKMnO4 = 0,1 . 2 = 0,2 (mol)
mKMnO4 = 0,2 . 158 = 31,6 (g(
Để tạo hh nổ mạnh nhất thì VH2 : VO2 = 2 : 1
=> VH2 = VO2 . 2 = 2,24 . 2 = 4,48 (l)
phân hủy bao nhiêu gam KMnO4,KClO3 để thu đc 4,48 lít oxi (đktc)
2KMnO4-to>K2MnO4+MnO2+O2
0,4--------------------------------------0,2
2KClO3-to>2KCl+3O2
\(\dfrac{2}{15}\)-----------------------0,2
n O2=\(\dfrac{4,48}{22,4}\)=0,2 mol
=>m KMNO4=0,4.158=63,2g
m KClO3=\(\dfrac{2}{15}\).122,5=16,33g
Phân hủy 273.4g hỗn hợp muối KClO3 và KMnO4 ta thu được 49,28 lít oxi (đktc). Lượng oxi thu được đốt cháy được bao nhiêu gam một loại than chứa 96% cacbon(còn lại là tạp chất không cháy)
nO2 = 49,28/22,4 = 2,2 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 2,2 <--- 2,2
mC = 2,2 . 12 = 26,4 (g)
mthan = 26,4/96% = 27,5 (g)
Phân hủy hoàn toàn 31,6g KMnO4 ( ở nhiệt độ cao )
1. Tính thể tích khí oxi tạo thành ( ở đktc )
2. Lượng oxi trên đủ đốt cháy hết bao nhiêu lít CH4 ( ở đktc )
3. Biết cứ 1 mol CH4 cháy hoàn toàn thì sinh ra 880KJ , hãy tính nhiệt lượng Q tạo ra hóa ra khí trên cháy hết
Biết K=39 , Mn=55, O=12, H=1, Mg=24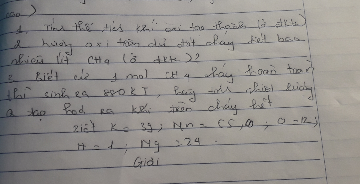
\(1) n_{KMnO_4}= \dfrac{31,6}{158} = 0,2(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{O_2} = \dfrac{1}{2}n_{KMnO_4} = 0,1(mol)\\ V_{O_2} = 0,1.22,4 = 2,24(lít)\\ 2) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ V_{CH_4} = \dfrac{1}{2}V_{O_2} = 1,12(lít)\\ 3)n_{CH_4} = \dfrac{1,12}{22,4} = 0,05(mol)\\ \text{Nhiệt lượng tỏa ra = } = 0,05.880 = 44(KJ)\)
phân hủy 31,6g kmno4 thu được bao nhiêu lít o2(đktc). Thể tíchõi thu được có đủ để đốt cháy 10,8g al không
\(n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(MOL\right);n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ 2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\left(1\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ n_{O_2\left(1\right)}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ n_{O_2\left(cần.\left(2\right)\right)}=\dfrac{3}{4}.0,4=0,3\left(mol\right)>0,1\left(mol\right)\)
Vậy thể tích khí oxy thu được không đủ đốt cháy 10,8 gam Al
a) Phân hủy hoàn toàn 63,2 gam KMnO4 sẽ thu đc bao nhiêu lít khí oxi ở đktc. Cùng lúc đó người ta cho 28 gam bột sắt tác dụng hết với dung dịch HCl, tính thể tích H2 thu đc ở đktc
b) Dẫn các khí thu đc từ các thí nghiệm trên vào bình kín không có không khí rồi thực hiện phản ứng đốt cháy. Hỏi sau phản ứng cháy chất nào dư? Dư bao nhiêu gam ?
c) Nếu dẫn thể tích H2 đó vào 1 bình kín chứa 166 gam Fe3O4 nung nóng. Sau phản ứng xong tính khối lượng Fe3O4 phản ứng và khối lượng sắt sinh ra.
a) nKMnO4= 63,2/158=0,4(mol)
nFe=0,5(mol)
PTHH: KMnO4 -to-> K2MnO4 + MnO2 + 1/2 O2
0,4________________________________0,2(mol)
=>V(O2,đktc)=0,2.22,4=4,48(l)
PTHH: Fe + 2 HCl -> FeCl2 + H2
0,5_____________________0,5(mol)
=> V(H2,đktc)=0,5.22,4=11,2(l)
b) H2 + 1/2 O2 -to-> H2O
0,5/2 > 0,2/1
=> H2 dư, O2 hết, tính theo nO2
=> nH2(dư)=0,5 - 0,2.2=0,1(mol)
=>mH2(dư)=0,1.2=0,2(g)
c) nFe3O4=166/232= 83/116(mol)
PTHH: Fe3O4 + 4 H2 -to-> 3 Fe + 4 H2O
nFe3O4(p.ứ)=0,5/4=0,125(mol)
=> mFe3O4=0,125.232=29(g)
nFe=3/4. 0,5=0,375(mol)
=>mFe=0,375.56=21(g)
để điều chế được 6,72 lít khí oxi cần phân hủy bao nhiêu gam KMnO4 biết hiệu suất phân hủy là 90%
2KMnO4-to>K2MnO4+MnO2+O2
0,6------------------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>m KMnO4pứ=0,6.158.\(\dfrac{100}{90}\)=105,33g