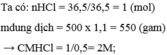Hòa tan 12.5 gam CuSO4.5H2O vào 87.5 ml nước . Tính nồng độ mol, nồng độ % của dung dịch thu được

Những câu hỏi liên quan
Bài 3.
a. Hòa tan hết 16 gamCuSO4 vào 184 gam nước thu được dung dịch CuSO4. Tính nồng độ % của dung dịch CuSO4 ?
b. Hòa tan hết 20 gam NaOH vào nước thu được 4000 ml dung dịch NaOH. Tính nồng độ mol của dung dịch NaOH ?
a)
C% CuSO4 = 16/(16 + 184) .100% = 8%
b)
n NaOH = 20/40 = 0,5(mol)
CM NaOH = 0,5/4 = 0,125M
Đúng 0
Bình luận (0)
\(a.\)
\(m_{dd_{CuSO_4\:}}=16+184=200\left(g\right)\)
\(C\%_{CuSO_4}=\dfrac{16}{200}\cdot100\%=8\%\)
\(b.\)
\(n_{NaOH}=\dfrac{20}{40}=0.5\left(mol\right)\)
\(C_{M_{NaOH}}=\dfrac{0.5}{4}=0.125\left(M\right)\)
Đúng 1
Bình luận (0)
a) \(m_{dmCUSO4}\) = 16+184 = 200g
C% = \(\dfrac{16}{200}\) x 100% =8 %
b) \(n_{NaOH}\) = \(\dfrac{20}{40}\) = 0,5 (Mol)
\(C_M\) = \(\dfrac{0.5}{4}\) = 0,125 (M) Vì 4000ml= 4l
Đúng 0
Bình luận (0)
Hòa tan 30 g NaCl vào 170 gam nước, được dung dịch có khối lượng riêng 1,1 gam/ml. Tính nồng độ phần trăm và nồng độ mol của dung dịch thu được
\(C\%=\dfrac{30}{170}.100\%=17,647\%\)
\(V_{\text{dd}}=\left(30+170\right)1,1=220ml\)
\(n_{NaCl}=\dfrac{30}{58,5}=0,513mol\)
\(C_M=\dfrac{0,513}{0,22}=0,696M\)
\(C\%_{NaCl}=\dfrac{30}{170+30}.100\%=15\%\\ C_M=C\%.\dfrac{10D}{M}=10.\dfrac{10.1,1}{58,5}=1,88M\)
Đúng 1
Bình luận (1)
Câu 1: Tính khối lượng muối NaNO3 cần lấy để khi hòa tan vào 170 g nước thì thu được dung dịch có nồng độ 15 %
Câu 2: Hòa tan 75 g tinh thể CuSO4.5H2O vào trong nước thu được 900 ml dd CuSO4. Tính CM dd này
Câu 3: Khối lượng riêng dd CuSO4 là 1,206 g/ml. Đem cô cạn 414,594 ml dd này thu được 140,625 g tinh thể CuSO4.5H2O . Tính nồng độ mol và nồng độ % dd nói trên.
Câu 1 :
Khối lượng dung dịch là : \(m_{ct}+170\)
Gọi khối lượng muối \(NaNO_3\)cần dùng là x
Ta có :\(m_{ct}=\frac{C\%.m_{dd}}{100}\)
hay \(x=\frac{15.\left(x+170\right)}{100}\)
Ta tính được x=30 (g)
Vậy khối lượng \(NaNO_3\)cần lấy là 30 g
Đúng 1
Bình luận (0)
Câu 2 :
Số mol \(CuSO_4.5H_2O\)là :
\(n_{CuSO_4.5H_2O}=\frac{m}{M}=\frac{75}{250}=0,3\left(mol\right)\)
\(\Rightarrow n_{CuSO_4}=0,3\left(mol\right);V_{dd}=900ml=0,9l\)
\(C_{M_{dd}}=\frac{n}{V}=\frac{0,3}{0,9}=\frac{1}{3}M\)
Vậy...
Đúng 0
Bình luận (0)
Câu 2. Hòa tan hoàn toàn 0,2 mol NaOH vào 500 ml H20 thu được dung dịch B. Tính nồng độ %, nồng độ mol/l của dung dịch B Câu 3. Hòa tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H20 thu được dung dịch C. Tính nồng độ %, nồng độ mol/l của dung dịch C Câu 4. Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H20 thu được dung dịch D. Tính nồng độ %, nồng độ mol/l của dung dịch D Câu 5. Hòa tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l của dung dịch E...
Đọc tiếp
Câu 2. Hòa tan hoàn toàn 0,2 mol NaOH vào 500 ml H20 thu được dung dịch B. Tính nồng độ %, nồng độ mol/l của dung dịch B Câu 3. Hòa tan hoàn toàn 2,8 gam KOH và 5,85 gam NaCl vào 600 ml H20 thu được dung dịch C. Tính nồng độ %, nồng độ mol/l của dung dịch C Câu 4. Hoà tan hoàn toàn 4,6 gam Na vào 100 gam H20 thu được dung dịch D. Tính nồng độ %, nồng độ mol/l của dung dịch D Câu 5. Hòa tan hoàn toàn 2,74 gam Ba vào 200 gam H2O thu được dung dịch E. Tính nồng độ %, nồng độ mol/l của dung dịch E Câu 6. Hòa tan hoàn toàn 5,85 gam K và 13,7 gam Ba vào 400 ml H2O thu được dung dịch F, Tính nồng độ %, nồng độ mol/l của dung dịch
Hòa tan 36,5 gam HCl vào nước, thu được 500ml dung dịch có khối lượng riêng D = 1,1 g/ml. Tính nồng độ mol và nồng độ phần trăm của dung dịch thu được.
a) Hòa tan 20 gam KCl vào 60 gam nước. Tính nồng độ phần trăm của dung dịch?b) Hòa tan 40 gam đường vào 150 ml nước (DH2O 1 g/ml). Tính nồng độ phần trăm củadung dịch?c) Hòa tan 60 gam NaOH vào 240 gam nước thu được dung dịch NaOH . Tính nồng độphần trăm dung dịch NaOH ?d) Hòa tan 30 gam NaNO3 vào 90 gam nước thu được dung dịch A. Tính nồng độ phầntrăm của dung dịch?e) Tính khối lượng NaCl có trong 150 gam dung dịch NaCl 60% ?f) Hòa tan 25 gam muối vào nước thu được dung dịch A có C% 10%. Hãy...
Đọc tiếp
a) Hòa tan 20 gam KCl vào 60 gam nước. Tính nồng độ phần trăm của dung dịch?
b) Hòa tan 40 gam đường vào 150 ml nước (DH2O = 1 g/ml). Tính nồng độ phần trăm của
dung dịch?
c) Hòa tan 60 gam NaOH vào 240 gam nước thu được dung dịch NaOH . Tính nồng độ
phần trăm dung dịch NaOH ?
d) Hòa tan 30 gam NaNO3 vào 90 gam nước thu được dung dịch A. Tính nồng độ phần
trăm của dung dịch?
e) Tính khối lượng NaCl có trong 150 gam dung dịch NaCl 60% ?
f) Hòa tan 25 gam muối vào nước thu được dung dịch A có C% = 10%. Hãy tính khối
lượng của dung dịch A thu được ?
g) Cần cho thêm bao nhiêu gam NaOH vào 120 gam dung dịch NaOH 20% để thu được
dung dịch có nồng độ 25%?
a, \(C\%_{KCl}=\dfrac{20}{20+60}.100\%=25\%\)
b, \(C\%=\dfrac{40}{40+150}.100\%\approx21,05\%\)
c, \(C\%_{NaOH}=\dfrac{60}{60+240}.100\%=20\%\)
d, \(C\%_{NaNO_3}=\dfrac{30}{30+90}.100\%=25\%\)
e, \(m_{NaCl}=150.60\%=90\left(g\right)\)
f, \(m_{ddA}=\dfrac{25}{10\%}=250\left(g\right)\)
g, \(n_{NaOH}=120.20\%=24\left(g\right)\)
Gọi: nNaOH (thêm vào) = a (g)
\(\Rightarrow\dfrac{a+24}{a+120}.100\%=25\%\Rightarrow a=8\left(g\right)\)
Đúng 2
Bình luận (0)
Hòa tan 14,2gam P2O5 vào 185,8 gam nước được dung dichjcos D=1,1g/ml. tính nồng độ phần trăm và nồng độ mol dung dịch thu được
\(n_{P_2O_5}=\dfrac{14.2}{142}=0.1\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
\(0.1............................0.2\)
\(m_{H_3PO_4}=0.2\cdot98=19.6\left(g\right)\)
\(m_{dd_{H_3PO_4}}=14.2+185.8=200\left(g\right)\)
\(C\%H_3PO_4=\dfrac{19.6}{200}\cdot100\%=9.8\%\)
\(V_{dd_{H_3PO_4}}=\dfrac{200}{1.1}=181.8\left(ml\right)=0.1818\left(l\right)\)
\(C_{M_{H_3PO_4}}=\dfrac{0.2}{0.1818}=1.1\left(M\right)\)
Đúng 3
Bình luận (0)
Ta có: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
____0,1_____________0,2 (mol)
\(\Rightarrow m_{H_3PO_4}=0,2.98=19,6\left(g\right)\)
Có: m dd sau pư = mP2O5 + mH2O = 200 (g)
\(\Rightarrow C\%_{H_3PO_4}=\dfrac{19,6}{200}.100\%=9,8\%\)
Có: V dd sau pư = \(\dfrac{200}{1,1}=\dfrac{2000}{11}\left(ml\right)=\dfrac{2}{11}\left(l\right)\)
\(\Rightarrow C_{M_{H_3PO_4}}=\dfrac{0,2}{\dfrac{2}{11}}=1,1M\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
a: hòa tan hoàn toàn 0,3 mol NaOH vào nước thu được 0,5 lít dung dịch NaOH. tính nồng độ mol của dung dịch?
b: hòa tan hoàn tàn 24 gam NaOH vào nước thu được 400ml dung dịch NaOH. tính nồng độ mol của dung dịch?
\(a,C_{M\left(NaOH\right)}=\dfrac{0,3}{0,5}=0,6M\\ b,n_{NaOH}=\dfrac{24}{40}=0,6\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,6}{0,4}=1,5M\)
Đúng 1
Bình luận (0)
a. hòa tan 9,2 gam Na2O vào nước thì thu được 500ml dung dịch. tính nồng độ mol của dung dịch?
b. hòa tan 37,6 gam K2O vào 362,4 gam nước . tính nồng độ phần trăm của dung dịch?
Sửa đề: 9,2 gam Na
\(a,n_{Na_2O}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
PTHH: \(Na_2O+H_2O\rightarrow2NaOH\)
0,4------------------>0,8
\(\rightarrow C_{M\left(NaOH\right)}=\dfrac{0,8}{0,5}=1,6M\)
\(b,n_{K_2O}=\dfrac{37,6}{94}=0,4\left(mol\right)\)
PTHH: \(K_2O+H_2O\rightarrow2KOH\)
0,4----------------->0,8
\(\rightarrow C\%_{KOH}=\dfrac{0,8.56}{362,4+37,6}.100\%=11,2\%\)
Đúng 1
Bình luận (0)