a)Tính thể tích khí H2 (đktc) cần dùng để khử hoàn toàn 24g CuO
b)Để có được lượng khí H2 dùng cho phản ứng trên , cần phải hòa tan bao nhieu gam sắt và dung dịch HCl dư
Khử hoàn toàn 24 gam Fe2O3 bằng khí H2(nung nóng),thu được sắt kim loại và nước. a. Viết PTHH xảy ra b. Tính thể tích khí H2(ở đktc) thu được c. Tính thể tích dd HCl 1.5M cần dùng để hòa tan hết lượng sắt tạo thành từ phản ứng trên.
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe_2O_3}=\dfrac{24}{160}=0,15\left(mol\right)\)
Theo PT: \(n_{H_2}=3n_{Fe_2O_3}=0,45\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,45.22,4=10,08\left(l\right)\)
c, n\(n_{Fe}=2n_{Fe_2O_3}=0,3\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{HCl}=2n_{Fe}=0,6\left(mol\right)\Rightarrow V_{HCl}=\dfrac{0,6}{1,5}=0,4\left(M\right)\)
a. Phương trình hoá học của phản ứng khử Fe2O3 bằng H2 là: Fe2O3 + 3H2 -> 2Fe + 3H2O
b. Theo phương trình trên, ta thấy 1 mol Fe2O3 cần 3 mol H2 để khử hoàn toàn. Do đó, số mol H2 cần dùng để khử hoàn toàn 24 gam Fe2O3 là:
n(H2) = 24/(2*55.85) * 3 = 2.56 (mol)
Theo định luật Avogadro, 1 mol khí ở đktc có thể chiếm thể tích là 22.4 lít. Vậy, thể tích khí H2 ở đktc thu được là:
V(H2)= n(H2) * 22.4 = 2.56 * 22.4 = 57.2 (lít)
Vậy thể tích khí H2 thu được là 57.2 lít.
c. Theo phương trình trên, ta thấy 1 mol Fe tạo thành cần 6 mol HCI để hòa tan hoàn toàn. Do đó, số mol HCI cần dùng để hòa tan hết lượng sắt tạo thành là: n(HCI) = 2 * n(H2) * 6 = 30.72 (mol)
Thể tích HCI 1.5M cần dùng là: V(HCI)= n(HCI) C(HCI)= 30.72/1.5 = 20.48 (lít)
Vậy thể tích dd HCI 1.5M cần dùng để hòa tan hết lượng sắt tạo thành là 20.48 lít.
Khử hoàn toàn 24 gam Fe3O4 bằng khí H2(nung nóng),thu được sắt kim loại và nước. a. Viết PTHH xảy ra b. Tính thể tích khí H2(ở đktc) thu được c. Tính thể tích dd HCl 1.5M cần dùng để hòa tan hết lượng sắt tạo thành từ phản ứng trên.
\(n_{Fe_3O_4}=\dfrac{24}{232}=\dfrac{3}{29}\left(mol\right)\)
PTHH :
\(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
3/29 9/29
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
9/29 18/29
\(c,V_{HCl}=\dfrac{\dfrac{18}{29}}{1,5}=\dfrac{12}{29}\left(l\right)\)
hòa tan hoàn toàn 2,7g al vào dung dịch hcl
.a>tính khối lượng hcl đã dùng .b>tính thể tích h2 (đktc) thu được sau phản ứng?P.c>nếu dùng toàn bộ lượng khí h2 bay ra ở trên đem khử 20g bột cuo ở nhiệt độ cao thì chất nào còn dư?dư bao nhiêu gam?a. Để tính khối lượng HCl đã dùng, ta cần biết số mol của Al đã phản ứng với HCl. Ta sử dụng phương trình phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
Theo đó, 2 mol Al tương ứng với 6 mol HCl. Vậy số mol HCl cần để phản ứng với 2,7 g Al là:
n(HCl) = n(Al) x (6/2) = 2,7/(27x2) x 6 = 0,05 mol
Khối lượng HCl tương ứng là:
m(HCl) = n(HCl) x M(HCl) = 0,05 x 36,5 = 1,825 g
Vậy khối lượng HCl đã dùng là 1,825 g.
b. Theo phương trình phản ứng, 2 mol Al tạo ra 3 mol H2. Vậy số mol H2 tạo ra từ 2,7 g Al là:
n(H2) = n(Al) x (3/2) = 2,7/(27x2) x 3 = 0,025 mol
Theo định luật Avogadro, 1 mol khí ở ĐKTC chiếm thể tích 22,4 L. Vậy thể tích H2 thu được là:
V(H2) = n(H2) x 22,4 = 0,025 x 22,4 = 0,56 L
P.c. CuO + H2 → Cu + H2O
Khối lượng CuO cần để khử hết 0,025 mol H2 là:
n(CuO) = n(H2)/2 = 0,0125 mol
m(CuO) = n(CuO) x M(CuO) = 0,0125 x 79,5 = 0,994 g
Vậy để khử hết H2, ta cần dùng 0,994 g CuO. Nếu dùng toàn bộ lượng H2 bay ra, chất CuO sẽ bị khử hoàn toàn thành Cu và không còn chất nào còn dư.
để khử hoàn toàn m gam một oxit sắt (FexOy) phải dùng vừa đủ 0,672 lít (đktc) khí H2. Khi đem toàn bộ lượng sắt thu được hòa tan vào 300g dung dịch HCl 7,3% (dư) thì thu được 0,448 lít (đktc) khí H2 và dung dịch A.
a/ Tìm công thức hóa học của oxit sắt trên
b/ Tính nồng độ phần trăm cái chất tan trong dung dịch A
Người ta dùng 4,48 lít khí H2 (dktc) để khử 17,4 gam oxit sắt từ. Sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn A
a) Tính m
b) Để hòa tan một lượng chất rắn a ở trên cần vừa đủ V (ml) dung dịch HCl 1M. Tính V và khối lượng muối thu được sau phản ứng
PTHH : \(Fe_3O_4+4H_2\rightarrow3Fe+4H_2O\)
.............0,05........0,2.......0,15.........
Có : \(\left\{{}\begin{matrix}n_{H_2}=0,2\left(mol\right)\\n_{Fe_3O_4}=0,075\left(mol\right)\end{matrix}\right.\)
- Theo phương pháp ba dòng .
=> Sau phản ứng H2 hết, Fe3O4 còn dư ( dư 0,025 mol )
=> \(m=m_{Fe3o4du}+m_{Fe}=14,2\left(g\right)\)
b, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
...0,15.....0,3.........0,15..............
\(Fe_3O_4+8HCl\rightarrow2FeCl_3+FeCl_2+4H_2O\)
.0,025......0,2..........0,05.........0,025...................
Có : \(V=\dfrac{n}{C_M}=\dfrac{n}{1}=n_{HCl}=0,2+0,3=0,5\left(l\right)\)
Lại có : \(m_M=m_{FeCl2}+m_{FeCl3}=30,35\left(g\right)\)
hòa tan hoàn toàn 3.6 gam mg bằng dd hcl tạo ra muối mgcl2 và khí h2
a tính thể tích khí sinh ra ở đktc
b nếu dùng toàn bộ thể tích h2 ở trên để khử 16g sắt (iii) oxit thì thu được tối đa bao nhiêu gam sắt
cíu với ạ:)<
nmg = \(\dfrac{3,6}{24}\) = 0,15 ( mol )
Mg + 2HCl → MgCl2 + H2
1 2 1 1
0,15 0,3 0,15
a) mHCl = 0,3 . 36,5 = 10,95 ( g )
b) VH2 = 0,15 . 22,4 = 3,36 ( l )
Tick dùm tớ nha, tớ giải theo trường có gì sai bỏ qua nhaaa
Hòa tan hoàn toàn 14,6 gam hỗn hợp X gồm Al và Sn bằng dung dịch HCl dư thu được 5,6 lít khí H2 (đktc). Thể tích khí O2 (đktc) cần để phản ứng hoàn toàn với 14,6 gam hỗn hợp X là:
A. 2,80 lít
B. 1,68 lít
C. 4,48 lít
D. 3,92 lít
Đáp án D
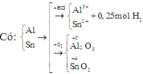
Vì trong hai thí nghiệm số oxi hóa của Sn trong sản phẩm thu được khác nhau nên ta cần tìm số mol cụ thể của mỗi kim loại trong hỗn hợp.
Một số bạn không để ý đến tính chất đặc biệt này của Sn mà cho rằng số oxi hóa của cả hai kim loại trong sản phẩm ở hai thí nghiệm là như nhau nên áp dụng ngay định luật bảo toàn mol electron:
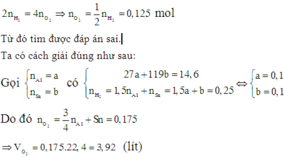
dùng khí cacbon oxit dư để khử hoàn toàn 23,2g oxit sắt từ ở nhiệt độ cao thì thu được chất rắn A. Hòa tan hoàn toàn A bằng dung dịch H2SO4 0,5M thì thu được khí B a,Tính thể tích khí B thu được ở đktc và thể tích dung dịch H2so4 0,5M cần dùng để hòa tan hết A b,đốt cháy hoàn toàn khí B.tính thể tích chất lỏng thu được sau khi đã làm ngưng ở nhiệt độ 4 độ C
PTHH: \(Fe_3O_4+4CO\xrightarrow[]{t^o}3Fe+4CO_2\uparrow\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
\(H_2+\dfrac{1}{2}O_2\xrightarrow[]{t^o}H_2O\)
Ta có: \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\) \(\Rightarrow n_{Fe}=0,3\left(mol\right)=n_{H_2SO_4}=n_{H_2}=n_{H_2O}\)
\(\Rightarrow\left\{{}\begin{matrix}V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\\V_{ddH_2SO_4}=\dfrac{0,3}{0,5}=0,6\left(l\right)\\V_{H_2O}=\dfrac{0,3\cdot18}{D_{nước}}=5,4\left(ml\right)\end{matrix}\right.\)
*P/s: \(D_{nước}=1g/ml\)
a) Tính thể tích H2 cần dùng để khử 24g Fe2O3?
b) Tính khối lượng Zn cần dùng để phản ứng với dung dịch HCl để được lượng H2 ở trên?
mong mọi người giúp
Fe2O3+3H2-to>2Fe+3H2O
0,15------0,45 mol
n Fe2O3=0,15 mol
=>VH2=0,45.22,4=10,08l
b)
Zn+2HCl->ZnCl2+H2
0,45-----------------------0,45
=>m Zn=0,45.65=29,25g