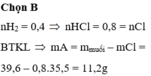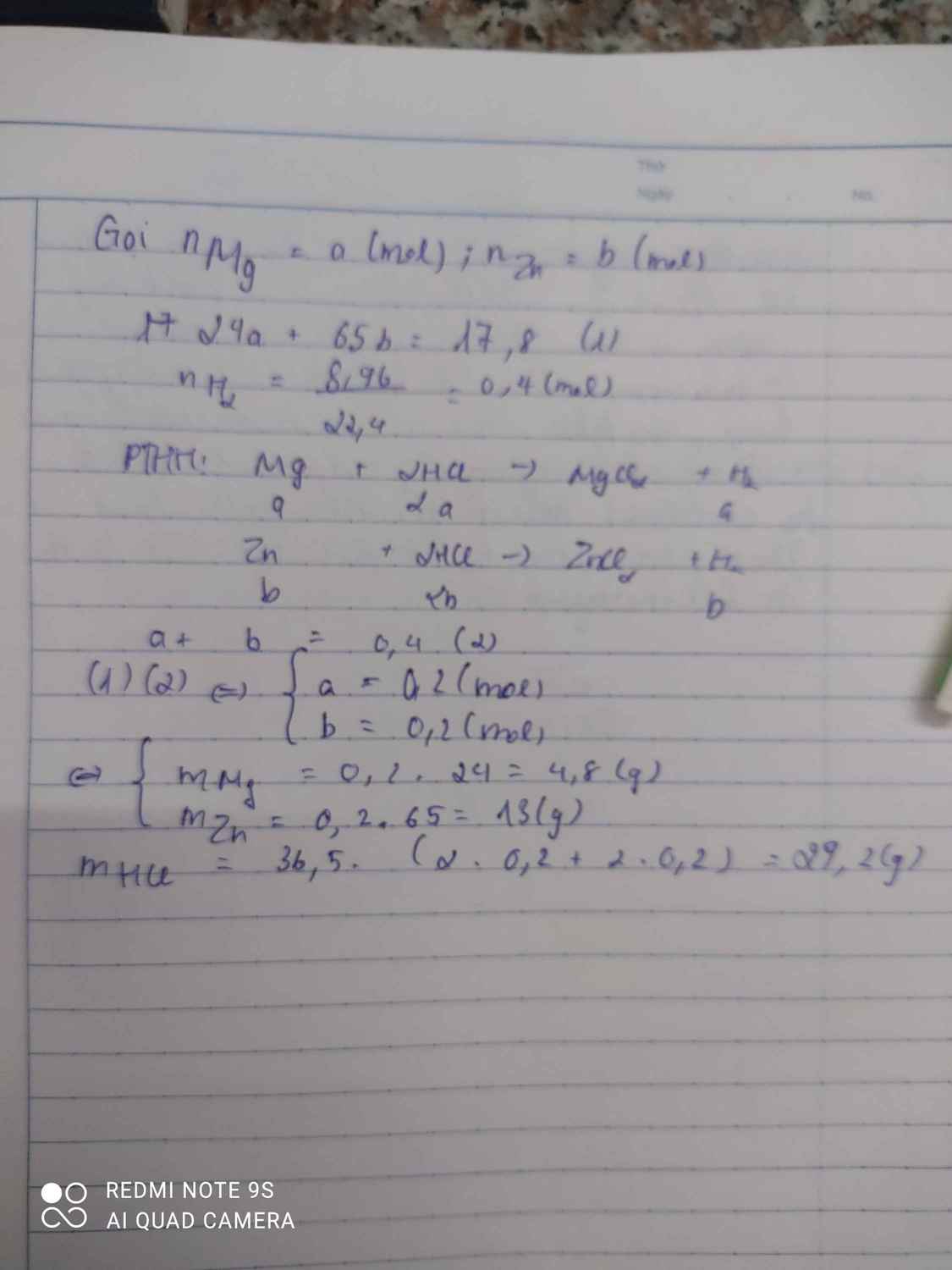Những câu hỏi liên quan
hoà tan hoàn toàn m gam hỗn hợp hai kim loại A và B bằng dung dịch HCL vừa đủ thu được 8,96 lít khí H2 ở đktc cô cạn dung dịch sau phản ứng thì thu được 39,4 gam hỗn hợp muối khan tính m
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
=> nHCl = 0,8 (mol)
Theo ĐLBTKL: mA,B + mHCl = mmuối + mH2
=> mA,B = 39,4 + 0,4.2 - 0,8.36,5 = 11 (g)
Đúng 2
Bình luận (1)
Cho 8,3 g hỗn hợp gồm Al và Fe phản ứng vừa đủ với 500 gam dung dịch HCl a% sau phản ứng thu được dung dịch chứa m gam muối và có 5,6 lít khí H2 thoát ra(dktc). Tính khối lượng mỗi kim loại, tính a và C% của các chất tan trong dung dịch sau phản ứng
Em đăng sang môn Hoá nha
Đúng 0
Bình luận (0)
Cho 8,3 g hỗn hợp gồm Al và Fe phản ứng vừa đủ với 500 gam dung dịch HCl a% sau phản ứng thu được dung dịch chứa m gam muối và có 5,6 lít khí H2 thoát ra(dktc). Tính khối lượng mỗi kim loại, tính a và C% của các chất tan trong dung dịch sau phản ứng
\(2Al+6HCl->2AlCl_3+3H_2\\ Fe+2HCl->FeCl_2+H_2\\ n_{Al}=a;n_{Fe}=b\\ 27a+56b=8,3\\ 1,5a+b=\dfrac{5,6}{22,4}=0,25\\ a=b=0,1\\ m_{Al}=27\cdot0,1=2,7g\\ m_{Fe}=8,3-2,7=5,6g\\ a=\dfrac{3a+2b}{500}\cdot36,5=3,65\%\\ m_{ddsau}=508,3-0,25\cdot2=507,8g\\ C\%_{AlCl_3}=\dfrac{133,5a}{507,8}=2,63\%\\ C\%_{FeCl_2}=\dfrac{127b}{507,8}=2,50\%\)
Đúng 1
Bình luận (0)
cho 16g hỗn hợp chứa Mg và kim loại M vào dung dịch HCL dư sau phản ứng thu dược 8,96 l khí H2 (đktc).Cùng 16 g hỗn hợp X ở trên tan hoành toàn trong dung dịch h2so4 đặc nóng dư thu được dung dịch y và 1,12 lít khí so2 (đktc) duy nhất.Viết PTHH và xác định kim loại M
-Đặt số mol của Mg và kim loại M lần lượt là : x và y
Các phương trình hóa học:
Mg + 2HCl → MgCl2 + H2
x................................................x
2M + 2nHCl → 2MCln + nH2 (có thể có)
y...................................................\(\dfrac{ny}{2}\)
Mg + 2H2SO4 → MgSO4 + SO2 + 2H2O
x....................................................x
2M + 2mH2SO4 → M2(SO4)m + mSO2 + 2mH2O
y ..........................................................\(\dfrac{my}{2}\) ![]()
Số mol của H2 là : \(\dfrac{8,96}{22,4}\) = 0,4 mol
Số mol của SO2 là : \(\dfrac{11,2}{22,4}\) = 0,5 mol
Trường hợp 1. Kim loại M không phản ứng với dung dịch HCl.
Theo bài ra và các phương trình trên ta có :
24x + My = 16 (1)
x = 0,4 (2)
x + \(\dfrac{my}{2}\)= 0,5 (3)
Từ (1), (2), (3) ta có : M = 32m
-Nếu m = 1 → M = 32 (loại)
-Nếu m = 2 → M = 64 (Cu)
-Nếu m = 3 → M = 96 (loại)
\(\rightarrow\)Vậy kim loại M là Cu
- Trường hợp 2. Kim loại M phản ứng với dung dịch HCl.
Theo bài ra và các phương trình trên ta có :
24x + My = 16 (4)
x +\(\dfrac{ny}{2}\) = 0,4 (5)
x + \(\dfrac{my}{2}\)= 0,5 (6)
Theo (5) và (6) thấy m > n
|
n |
1 | 1 | 2 |
|
m |
2 |
3 |
3 |
|
x |
0,3 |
0,35 |
0,2 |
|
y |
0,2 |
0,1 |
0,2 |
|
M |
44 (loại) |
76 (loại) |
56 (Fe) |
Vậy kim loại M là Fe
Đúng 0
Bình luận (0)
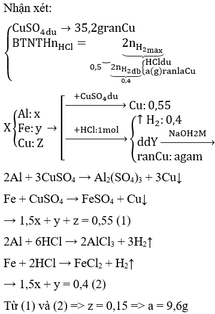
Hỗn hợp X gồm ba kim loại Al, Fe, Cu. Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn.Viết phương trình phản ứng xảy ra và tìm giá trị của a.
Đọc tiếp
Hỗn hợp X gồm ba kim loại Al, Fe, Cu. Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn.Viết phương trình phản ứng xảy ra và tìm giá trị của a.
Hòa tan m gam hỗn hợp A gồm Fe và kim loại M trong dung dịch HCl. Sau khi hai kim loại đã tan hết thu được 8,96 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được 39,6g muối khan. Giá trị của m là A. 0,11. B. 11,2. C. 11 D. 11,1.
Đọc tiếp
Hòa tan m gam hỗn hợp A gồm Fe và kim loại M trong dung dịch HCl. Sau khi hai kim loại đã tan hết thu được 8,96 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được 39,6g muối khan. Giá trị của m là
A. 0,11.
B. 11,2.
C. 11
D. 11,1.
Hòa tan m gam hỗn hợp A gồm Fe và kim loại M trong dung dịch HCl. Sau khi hai kim loại đã tan hết thu được 8,96 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được 39,6g muối khan. Giá trị của m là
A. 0,11.
B. 11,2.
C. 11.
D. 11,1.
Đáp án B
nH2 = 0,4 => nHCl = 0,8 = nCl
BTKL => mA = mmuối – mCl = 39,6 – 0,8.35,5 = 11,2g
Đúng 0
Bình luận (0)
Cho 24,2 g hỗn hợp 2 kim loại gồm Zn,Fe phản ứng hết dung dịch HCl 2,5 M sau phản ứng thu được 8,96 lít khí (đktc).
a. Tính thành phần % theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
b. Tính thể tích dd HCl đủ dùng.
c. Tính nồng độ M dung dịch muối sau phản ứng.
a) \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Đặt:n_{Zn}=x\left(mol\right);n_{Fe}=y\left(mol\right)\)
\(n_{H_2}=0,4\left(mol\right)\)
Theo đề ta có hệ \(\left\{{}\begin{matrix}65x+56y=24,2\\x+y=0,4\end{matrix}\right.\)
=> x=0,2 ; y=0,2
\(\%m_{Zn}=\dfrac{0,2.65}{24,2}.100=53,72\%;\%m_{Fe}=46,28\%\)
b)Bảo toàn nguyên tố H: \(n_{HCl}=2n_{H_2}=0,8\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,8}{2,5}=0,32\left(l\right)\)
c) \(n_{FeCl_2}=0,2\left(mol\right);n_{ZnCl_2}=0,2\left(mol\right)\)
=> \(CM_{FeCl_2}=\dfrac{0,2}{0,32}=0,625\left(mol\right)\)
\(CM_{ZnCl_2}=\dfrac{0,2}{0,32}=0,625\left(mol\right)\)
Đúng 0
Bình luận (1)
BT4.cho hỗn hợp A gồm 17,8 gam Mg và Zn tác dụng vs dung dịch HCl dư . sau phản ứng thu đc 8,96 lít H2 (đktc)
a) viết PTHH của phản ứng xảy ra .
b) tính khối lượng mỗi kim loại trong hỗn hợp A.
c)tính khối lượng HCl tối thiểu cần dùng .
lm giúp mik vsssssssss
Mg+2HCl->MgCl2+H2
x------------------------x
Zn+2HCl->ZnCl2+H2
y-------------------------y
Ta có :
\(\left\{{}\begin{matrix}24x+65y=17,8\\x+y=\dfrac{8,96}{22,4}\end{matrix}\right.\)
=>x=0,2 mol, y=0,2 mol
=>mMg=0,2.24=4,8g
=>m Zn=0,2.65=13g
=>m HCl=0,8.36,5=29,2g
Đúng 4
Bình luận (0)