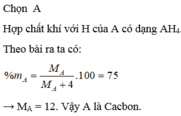A hợp với oxi tạo ra oxit có công thức A 2 O 5 . Trong hợp chất của A với hiđro thì hiđro chiếm 8,82% về khối lượng
a. Xác định A. Viết hợp chất của A với Oxi
b. Biết A thuộc chu kì mấy? nhóm mấy?

Những câu hỏi liên quan
R là nguyên tố nhóm A , công thức hợp chất khí của R với hiđro là RH3 . Trong hợp chất ôxit cao nhất của R , oxi chiếm 56,34% về khối lượng : a) xác định tên của R ; b) viết công thức electron , công thức cấu tạo phân tử hợp chất của R với hidro
HD:
CT oxit cao nhất của R với oxi là R2O5 (suy ra từ RH3).
Ta có: 80/(2R+80) = 0,5634 suy ra: R = 14 (N).
cấu tạo:
Đúng 0
Bình luận (0)
Hóa trị cao nhất vs khí H là 3
>> hóa trị cao nhất vs O là 8_3=5
>>hợp chất vs oxit cao nhất là R2O5
Có %mO=56.34%
Xét tỉ số MO/Mo+MR =%mo
Hay80/80+2×MR=0.5634
>>MR=14(N)
>>hợp chất vs oxit cao nhất là N2O5
b) hợp chất vs H là NH3
Đúng 0
Bình luận (0)
Bài 2: Một nguyên tố R tạo hợp chất với hiđro có công thức RH3 . Trong oxit cao nhất của R thì nguyên tố R chiếm 43,66% về khối lượng .
a/ Viết cấu hình e của ng/tử ng/tố R. Biết R ở chu kì 3
b/ Xác định nguyên tố R và công thức hiđroxit của R có tính axit hay bazơ?
giúp em với ạ!!!!
\(a.CToxit:R_2O_5\\ \%R=\dfrac{R.2}{R.2+16.5}=43,66\%\\ \Rightarrow R=31\\ \Rightarrow Z_R=15\\ Cấuhìnhe:1s^22s^22p^63s^23p^3\\ b.RlàPhốtpho\left(P\right),CThidroxit:P\left(OH\right)_5-^{bỏ1lầnH_2O}\rightarrow H_3PO_4,tínhaxit\)
Đúng 1
Bình luận (0)
a. Một hợp chất tạo bởi 2 nguyên tố cacbon và hiđro, trong đó hiđro chiếm 25% về khối lượng. Biết tỉ khối của khí này so với khí oxi 0,5 lần. Hãy xác định công thức hoá học của hợp chất ?b. Tính thành phần % về khối lượng mỗi nguyên tố có trong hợp chất Cu(OH)2.
Đọc tiếp
a. Một hợp chất tạo bởi 2 nguyên tố cacbon và hiđro, trong đó hiđro chiếm 25% về khối lượng. Biết tỉ khối của khí này so với khí oxi 0,5 lần. Hãy xác định công thức hoá học của hợp chất ?
b. Tính thành phần % về khối lượng mỗi nguyên tố có trong hợp chất Cu(OH)2.
a)
gọi hợp chất đó là x
\(d_{X/O_2}=\dfrac{M_x}{M_{O_2}}=\dfrac{M_X}{32}=0,5\\ =>M_X=0,5\cdot32=16\left(\dfrac{g}{mol}\right)\)
nguyên tố Cacbon chiếm: 100%-25%=75%
\(m_C=\dfrac{16\cdot75}{100}=12\left(g\right);m_H=\dfrac{16\cdot25}{100}=4\left(g\right)\)
\(n_C=\dfrac{12}{12}=1\left(mol\right);n_H=\dfrac{4}{1}=4\left(mol\right)\)
=> 1 phân tử hợp chất có có 1 nguyên tử C, 4 nguyên tử H
=> CTHH: CH4
b)
\(M_{Cu\left(OH\right)_2}=64+\left(16+1\right)\cdot2=98\left(\dfrac{g}{mol}\right)\)
\(\%m_{Cu}=\dfrac{64\cdot100}{98}=65,3\%\)
\(\%m_O=\dfrac{\left(16\cdot2\right)\cdot100}{98}=32,7\%\)
\(\%m_H=100\%-32,7\%-65,3\%=2\%\)
Đúng 1
Bình luận (1)
Gọi CTHH của hợp chất khí là CxHy
Ta có: %MC=12x30=80100⇒x=30×80100÷12=2%MC=12x30=80100⇒x=30×80100÷12=2
Vậy x=2x=2
Ta có: 12×2+1×y=3012×2+1×y=30
⇔24+y=30⇔24+y=30
⇔y=6⇔y=6
Vậy CTHH của hợp chất khí là C2H6
Đúng 0
Bình luận (0)
Một nguyên tố có công thức oxit cao nhất là R2O7, nguyên tố này tạo với hiđro một chất khí trong đó hiđro chiếm 0,78% về khối lượng. Xác định nguyên tố R; công thức hợp chất khí với Hidro; hợp chất với oxi.
1. Một ion M3+ có tổng số hạt (electron, nơtron, proton) bằng 79, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 19.a. Xác định vị trí (số thứ tự ô nguyên tố, chu kì, nhóm) của M trong bảng tuần hoàn.b. Viết cấu hình electron của các ion do M tạo ra.2. Phần trăm khối lượng của nguyên tố R trong hợp chất khí với hiđro (trong đó R có số oxi hóa thấp nhất) là a%, còn trong oxit cao nhất là b%.a. Xác định R biết a:b11:4.b. Viết công thức phân tử, công thức electron, công thức cấu tạo...
Đọc tiếp
1. Một ion M3+ có tổng số hạt (electron, nơtron, proton) bằng 79, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 19.
a. Xác định vị trí (số thứ tự ô nguyên tố, chu kì, nhóm) của M trong bảng tuần hoàn.
b. Viết cấu hình electron của các ion do M tạo ra.
2. Phần trăm khối lượng của nguyên tố R trong hợp chất khí với hiđro (trong đó R có số oxi hóa thấp nhất) là a%, còn trong oxit cao nhất là b%.
a. Xác định R biết a:b=11:4.
b. Viết công thức phân tử, công thức electron, công thức cấu tạo của hai hợp chất trên.
c. Xác định loại liên kết hóa học của R với hiđro và của R với oxi trong hai hợp chất trên.
1/Đặt Z, N lần lượt là số hạt p, n có trong nguyên tử M
ta có hệ phương trình
\(\begin{cases}2Z+N=79+3\\2Z-N=19+3\end{cases}\)\(\Rightarrow\begin{cases}Z=26\\N=30\end{cases}\)
a. Cấu hình electron nguyên tử của M là: 1s22s22p63s23p63d64s2
M ở ô thứ 26, chu kì 4 nhóm VIIIB trong bảng tuần hoàn.
b. Cấu hình electron của ion Fe2+ là: 1s22s22p63s23p63d6
Cấu hình electron của ion Fe3+ là: 1s22s22p63s23p63d5
Đúng 0
Bình luận (0)
2.
Vì R tạo được hợp chất khí với H nên R là phi kim.
Giả sử R thuộc nhóm x (x\(\ge\)4).
Theo giả thiết
công thức của R với H là RH8-x \(\Rightarrow\)a=\(\frac{R}{R+8-x}.100\)
công thức oxit cao nhất của R là R2Ox
\(\Rightarrow\) b=\(\frac{2R}{2R+16x}.100\) \(\Leftrightarrow\) b= \(\frac{R}{R+8x}.100\)
suy ra \(\frac{a}{b}=\frac{R+8x}{R+8-x}=\frac{11}{4}\)\(\Leftrightarrow R=\frac{43x-88}{7}\)
Xét bảng
a/ Vậy R là C
b/
Công thức của R với H là CH4
Công thức electron ; Công thức cấu tạo
Oxti cao nhất của R là CO2
Công thức electron O:: C ::O; Công thức cấu tạo O=C=O
c.
Trong hợp chất CH4 có \(\Delta\chi=\chi_C-\chi_H\)=2,55-0,22=0,35<0,4 nên liên kết giữa C-H là liên kết cộng hóa trị không cực
Trong hợp chất CO2 có 0, \(\Delta\chi=\chi_O-\chi_C\) =3,44-2,55=0,89
\(\Rightarrow\) 0,4<\(\Delta\chi=0,89\)<1,7 nên liên kết giữa C=O là liên kết cộng hóa trị phân cực
Đúng 0
Bình luận (0)
BT công thức oxit cao nhất, công thức hợp chất với H
(a). Nguyên tố R thuộc nhóm VA trong bảng tuần hoàn các nguyên tố hóa học. Hợp chất khí với hiđro của nguyên tố này chứa 17,64% hiđro về khối lượng. Xác định nguyên tố R?
(b). Công thức phân tử của hợp chất khí tạo bởi nguyên tố R và hiđro là RH 3 . Trong oxit mà R có hoá trị cao nhất thì oxi chiếm 74,07% về khối lượng.Xác định nguyên tố R?
Đọc tiếp
BT công thức oxit cao nhất, công thức hợp chất với H (a). Nguyên tố R thuộc nhóm VA trong bảng tuần hoàn các nguyên tố hóa học. Hợp chất khí với hiđro của nguyên tố này chứa 17,64% hiđro về khối lượng. Xác định nguyên tố R? (b). Công thức phân tử của hợp chất khí tạo bởi nguyên tố R và hiđro là RH 3 . Trong oxit mà R có hoá trị cao nhất thì oxi chiếm 74,07% về khối lượng.Xác định nguyên tố R?
a)
Do R thuộc nhóm VA
=> CTHH của R và H là: RH3
Có \(\dfrac{3}{M_R+3}.100\%=17,64\%=>M_R=14\left(g/mol\right)\)
=> R là N
b) Do CTHH của R và H là RH3
=> oxit cao nhất của R là R2O5
Có: \(\dfrac{16.5}{2.M_R+16.5}.100\%=74,07\%=>M_R=14\left(g/mol\right)\)
=> R là N
Đúng 2
Bình luận (0)
Câu 1 : Nguyên tố R thuộc nhóm A, tạo được oxit cao nhất có công thức RO3. Trong hợp chất khí với hiđro phần trăm khối lượng của R bằng 94,18%. a) Xác định nguyên tố Rb) Viết công thức phân tử và công thức cấu tạo của hiđroxit cao nhất của R.c) Cho 3,0 gam hỗn hợp X (gåm Al và Mg) hòa tan hoàn toàn bằng dung dịch hiđroxit cao nhất của R trên,giải phóng 3,36 l khí H2 ở đktc và dung dịch B. Cho B vào NaOH dư, lấy kết tủa rửa sạch nung tới khối lượng không đổi thu được m gam chất rắn. Tính % khối...
Đọc tiếp
Câu 1 : Nguyên tố R thuộc nhóm A, tạo được oxit cao nhất có công thức RO3. Trong hợp chất khí với hiđro phần trăm khối lượng của R bằng 94,18%.
a) Xác định nguyên tố R
b) Viết công thức phân tử và công thức cấu tạo của hiđroxit cao nhất của R.
c) Cho 3,0 gam hỗn hợp X (gåm Al và Mg) hòa tan hoàn toàn bằng dung dịch hiđroxit cao nhất của R trên,giải phóng 3,36 l khí H2 ở đktc và dung dịch B. Cho B vào NaOH dư, lấy kết tủa rửa sạch nung tới khối lượng không đổi thu được m gam chất rắn. Tính % khối lượng các chất trong X và giá trị của m?
Hợp chất X tạo ra oxit cao nhất có công thức là A O 2 .Trong hợp chất khí với hiđro A chiếm 75% về khối lượng. Nguyên tố A là:
A. C (M = 12)
B. Si (M = 28)
C. S (M = 32)
D. Cl (M = 35,5)
nguyên tố R tạo thành hợp chất khí với hiđro có công thức dạng chung RH3 . Trong trường hợp chất này nguyên tố R chiếm 82,35% về khối lượng . Xác định tên nguyên tố R , viết công thức hoá học của R đối với oxi và hiđro, so sánh tính chất của R với các nguyên tố kề bên trong cùng chu kì và nhóm