tính thành phân phần trăm của mỗi nguyên tố trong hợp chất Fe(III) và SO4(II)

Những câu hỏi liên quan
Cho sơ đồ sau : Fe(OH)y + H2SO4 -> Fex(SO4)y = H2O
a. Xác định các chỉ số x,y ( biết rằng x khác y ) và lập PTHH
b. Cho biết tỉ lệ số phân tử của một cặp chất tùy ý trong PTHH trên
c. Tính thành phần phần trăm của nguyên tố Fe trong hợp chất Fe(OH)y
d. Cho 10,7g Fe(OH)y tác dụng với H2SO4 tạo thành 20g Fex(SO4)y và 5,4g nước . Tính khối lượng H2SO4 đã dùng .
a) x = 2 ; y = 3
\(2Fe(OH)_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 6H_2O\)
b)
Tỉ lệ số phân tử Fe(OH)3 : số phân tử H2SO4 là 2 : 3
c)
\(\%Fe = \dfrac{56}{56 + (16 + 1).3}.100\% = 52,34\%\)
d)
Bảo toàn khối lượng :
\(m_{H_2SO_4} = m_{Fe_x(SO_4)_y} + m_{H_2O} - m_{Fe(OH)_y} = 20 + 5,4 - 10,7 = 14,7(gam)\)
Đúng 0
Bình luận (0)
Tính thành phần phần trăm theo khối lƣợng của các nguyên tố trong hợp chất sau: a) Sắt(III) oxit: Fe2O3 b) Nhôm sunfat : Al2(SO4)3
a) \(\left\{{}\begin{matrix}\%Fe=\dfrac{56.2}{160}.100\%=70\%\\\%O=100\%-70\%=30\%\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}\%Al=\dfrac{27.2}{342}.100\%=15,79\%\\\%S=\dfrac{32.3}{342}.100\%=28,07\%\\\%O=\dfrac{16.12}{342}.100\%=56,14\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Lập công thức hoá học rồi tính phân tử khối của các hợp chất có thành phần như sau: a) C (IV) và O. b) Fe (III) và SO4 (II)
a) Ta gọi: \(C_a^{IV}O_b^{II}\) (a,b: nguyên, dương)
Theo quy tắc hóa trị ta có:
a.IV=II.b
=>a/b=II/IV=2/4=1/2
=>a=1; b=2 => CTHH: CO2
PTKCO2= NTKC+ 2.NTKO=12+2.16=44(đ.v.C)
Đúng 5
Bình luận (0)
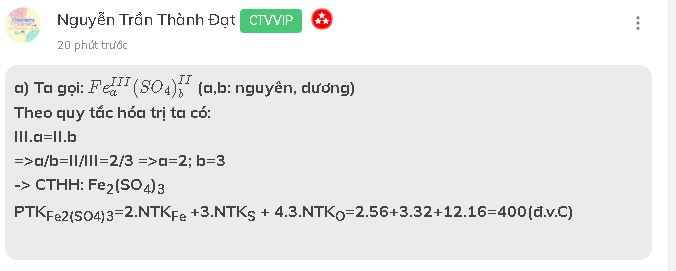
a) Ta gọi: \(Fe_a^{III}\left(SO_4\right)_b^{II}\) (a,b: nguyên, dương)
Theo quy tắc hóa trị ta có:
III.a=II.b
=>a/b=II/III=2/3 =>a=2; b=3
-> CTHH: Fe2(SO4)3
PTKFe2(SO4)3=2.NTKFe +3.NTKS + 4.3.NTKO=2.56+3.32+12.16=400(đ.v.C)
Đúng 1
Bình luận (0)
Câu 1. Tính hóa trị của mỗi nguyên tố trong các hợp chất sau:(biết NO3 hóa trị I)a) CuO b) Ba(NO3)2GCâu 2. Lập công thức hóa học của các hợp chất sau và tính phân tử khối của chúng: a) Ba (II) và O b) Al (III) và (SO4) (II)Câu 3. Nêu ý nghĩa của công thức hóa học: Ca(OH)2, CuSO4Câu 4: Kim loại M tạo ra hiđroxit M(OH)3 có phân tử khối là 103. Tính nguyên tử khối của M.Câu 5: Nguyên tử của nguyên tố X có tổng số hạt là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điệ...
Đọc tiếp
Câu 1. Tính hóa trị của mỗi nguyên tố trong các hợp chất sau:
(biết NO3 hóa trị I)
a) CuO
| b) Ba(NO3)2 G |
Câu 2. Lập công thức hóa học của các hợp chất sau và tính phân tử khối của chúng:
a) Ba (II) và O | b) Al (III) và (SO4) (II) |
Câu 3. Nêu ý nghĩa của công thức hóa học: Ca(OH)2, CuSO4
Câu 4: Kim loại M tạo ra hiđroxit M(OH)3 có phân tử khối là 103. Tính nguyên tử khối của M.
Câu 5: Nguyên tử của nguyên tố X có tổng số hạt là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Xác định số hạt proton, electron và notron trong X.
(Cho NTK của các nguyên tố: Al = 27; O = 16; H = 1; Zn = 65, Fe = 56, S = 32, Na = 23)
Bài 1.
a) Cu có hóa trị ll.
O có hóa trị ll.
b) Ba có hóa trị ll.
NO3 có hóa trị l.
Đúng 0
Bình luận (0)
Bài 2.
a) \(BaO\Rightarrow137+16=153\left(đvC\right)\)
B) \(Al_2\left(SO_4\right)_3\Rightarrow2\cdot27+3\cdot32+16\cdot12=342\left(đvC\right)\)
Đúng 0
Bình luận (0)
Bài 3.
Theo bài ta có: \(M_M+3\cdot17=103\Rightarrow M_M=52\)
Vậy M là nguyên tử Crom.
KHHH: Cr
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
nguyên tố x có trong hợp chất x(OH)2 biết nguyên tố x chiếm 54,054% xác định nguyên tố x và viết công thức phân tử hợp chất (tính thành phần, phần trăm về khối lượng của mỗi nguyên tố trong hợp chất)
a. Xác định hóa trị của nguyên tố Fe trong hợp chất sau: FeCl2? Biết Cl có hóa trị I
b. Lập công thức hóa học của các hợp chất sau: Cu (II) và O ; Al ( III) và SO4 (II).
\(a.Đặt:Fe^xCl^I_2\left(x:nguyên,dương\right)\\ \Rightarrow x.1=I.2\\ \Leftrightarrow x=\dfrac{I.2}{1}=II\\ \Rightarrow Fe\left(II\right)\\ b.Đặt:Cu_a^{II}O^{II}_b\left(a,b:nguyên,dương\right)\\ \Rightarrow a.II=b.II\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{2}{2}=\dfrac{1}{1}\\ \Rightarrow\left\{{}\begin{matrix}a=1\\b=1\end{matrix}\right.\\ \Rightarrow CTHH:CuO\\Đặt:Al^{III}_x\left(SO_4\right)^{II}_y\left(a,b:nguyên,dương\right)\\ \Rightarrow x.III=y.II\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{II}{III}=\dfrac{2}{3}\\ \Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\\ \Rightarrow CTHH:Al_2\left(SO_4\right)_3\)
Đúng 2
Bình luận (0)
a) Gọi hóa trị của Fe là: x.
Theo quy tắc hóa trị ta có:
x*1=1*2
x=2
Vậy hóa trị của Fe: 2
b) Cu(II) và O(II) => CuO
Al(III) và SO4(II) => Al2(SO4)3
Đúng 0
Bình luận (0)
a) Lập công thức hóa học của những hợp chất hai nguyên tố sau: P (III) và H; C (IV) và S (II); Fe (III) và O.
b) Lập công thức hóa học của những hợp chất tạo bởi một nguyên tố và nhóm nguyên tử như sau:
Na (I) và OH (I); Cu (II) và (SO4) (II); Ca (II) và (NO3)(I).
a. P (III) và H: có công thức dạng chung là 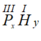
Theo quy tắc hóa trị ta có: x.III = y.I 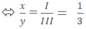 ⇒ x =1 ; y =3
⇒ x =1 ; y =3
⇒ PxHy có công thức PH3
C (IV) và S(II): có công thức dạng chung là 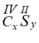
Theo quy tắc hóa trị ta có: x.IV = y.II 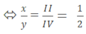 ⇒ x =1 ; y =2
⇒ x =1 ; y =2
⇒ CxSy có công thức CS2
Fe (III) và O: có công thức dạng chung là 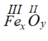
Theo quy tắc hóa trị ta có: x.III = y.II 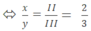 ⇒ x =2 ; y =3
⇒ x =2 ; y =3
⇒ FexOy có công thức Fe2O3
b. Na (I) và OH(I): có công thức dạng chung là 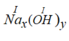
Theo quy tắc hóa trị ta có: x.I = y.I 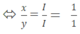 ⇒ x =1 ; y =1
⇒ x =1 ; y =1
⇒ Nax(OH)y có công thức NaOH
Cu (II) và SO4(II): có công thức dạng chung là 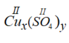
Theo quy tắc hóa trị ta có: x.II = y.II 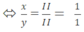 ⇒ x =1 ; y =1
⇒ x =1 ; y =1
⇒ Cux(SO4)y có công thức CuSO4
Ca (II) và NO3(I): có công thức dạng chung là 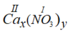
Theo quy tắc hóa trị ta có: x.II = y.I 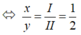 ⇒ x =1 ; y =2
⇒ x =1 ; y =2
⇒ Cax(NO3)y có công thức Ca(NO3)2
Đúng 0
Bình luận (0)
hợp chất X gồm nguyên tố kim loại R liê kết với nhóm SO4. Phân tử X nặng hơn phân tử Oxi gấp 12.5 lần
a. Xác định nguyên tố R
b. Tính thành phần phần trăm kh/lượng của ng/tố R trong hợp chất X
Giúp mình với ạ, gấp lắm
bạn kiểm tra lại đề giúp mình xem có đúng ko?
Đúng 0
Bình luận (0)
Lập công thức hóa học và tính phân tử khối của các hợp chất tạo bởi một nguyên tố và
nhóm nguyên tử sau: Fe (III) và nhóm (SO4)