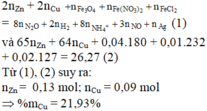cho 6,5 gam kẽm phản ứng với dung dịch chứa 10 gam HCl. toàn bộ lượng H2 thu được đem phản ứng với Fe3O4 ( giải sử sản phẩm thử phản ứng là Fe). tính khối lượng Fe thu đc

Những câu hỏi liên quan
Cho 19,5 gam kẽm phản ứng với dung dịch chứa 40 gam H2SO4. Toàn bộ lượng H2 thu được đem phản ứng với một oxit bazơ. Sau phản ứng thu được 11,2 gam kim loại. Xác định CTHH của oxit bazơ? Gọi tên oxit bazơ?
Gọi hóa trị kim loại R cần tìm là \(x\) \(\left(x\in\left\{2;3;\dfrac{8}{3}\right\}\right)\)
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
\(R_2O_x+xH_2\underrightarrow{t^o}2R+xH_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\n_{H_2SO_4}=\dfrac{40}{98}=\dfrac{20}{49}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) H2SO4 còn dư, Zn phản ứng hết
\(\Rightarrow n_R=\dfrac{0,6}{x}\left(mol\right)\) \(\Rightarrow M_R=\dfrac{11,2}{\dfrac{0,6}{x}}=\dfrac{56x}{3}\)
Ta thấy \(x=3\) thì \(M_R=56\) nên kim loại cần tìm là Sắt
+) Công thức của oxit bazơ: Fe2O3
+) Gọi tên: Sắt (III) oxit
Đúng 0
Bình luận (0)
Hòa tan 5,6 gam Fe trong dung dịch chứa 10,95 gam HCl đến phản ứng hoàn toàn theo
phương trình phản ứng: Fe + HCl → FeCl2 + H2. Tính khối lượng FeCl2 tạo thành? Tính
thể tích H2 thu được ở đktc ?
Em đăng câu hỏi sang môn hóa nha em ơi
Đúng 0
Bình luận (0)
Hòa tan 5,6 gam Fe trong dung dịch chứa 10,95 gam HCl đến phản ứng hoàn toàn theo
phương trình phản ứng: Fe + HCl → FeCl2 + H2. Tính khối lượng FeCl2 tạo thành? Tính
thể tích H2 thu được ở đktc ?
a) nFe= 5,6/56=0,1(mol)
nHCl=10,95/36,5=0,3(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
Ta có: 0,3/2 > 0,1/1
=> HCl dư, Fe hết, tính theo nFe
-> nH2=nFeCl2=nFe=0,1(mol)
=> V(H2,đktc)=0,1.22,4=2,24(l)
mFeCl2=0,1.127=12,7(g)
Đúng 1
Bình luận (0)
Hòa tan 5,6 gam Fe trong dung dịch chứa 10,95 gam HCl đến phản ứng hoàn toàn theo phương trình phản ứng: Fe + HCl → FeCl2 + H2. Tính khối lượng FeCl2 tạo thành? Tính thể tích H2 thu được ở đktc ?
\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(n_{HCl}=\dfrac{10.95}{36.5}=0.3\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Lập tỉ lệ :
\(\dfrac{0.2}{1}>\dfrac{0.3}{2}\Rightarrow Fedư\)
Khi đó :
\(n_{FeCl_2}=n_{H_2}=\dfrac{1}{2}\cdot n_{HCl}=\dfrac{1}{2}\cdot0.3=0.15\left(mol\right)\)
\(m_{FeCl_2}=0.15\cdot127=19.05\left(g\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)
Đúng 1
Bình luận (1)
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ Vì:\dfrac{0,1}{1}< \dfrac{0,3}{2}\\ \Rightarrow HCldư\\ \Rightarrow n_{FeCl_2}=n_{Fe}=n_{H_2}=0,1\left(mol\right)\\ \Rightarrow m_{FeCl_2}=127.0,1=12,7\left(g\right)\\ V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Ta có:nFe= 5,6/56=0,1(mol)
nHCl=10,95/36,5=0,3(mol)
PTHH: Fe + 2 HCl -> FeCl2 + H2
Ta có: 0,3/2 > 0,1/1
=> HCl dư, Fe hết, tính theo nFe
-> nH2=nFeCl2=nFe=0,1(mol)
=> VH2(đktc)=0,1.22,4=2,24(l)
mFeCl2=0,1.127=12,7(g)
Đúng 0
Bình luận (0)
Cho 11,2 gam Fe tác dụng với dung dịch HCL . sau phản ứng thu được sắt ( II) clorua và khí Hidro.
Tính mFeCl2
b, Tính Vh2
C. Người ta đem đốt cháy lượng H2 đó sử dụng 4,48 lít khí oxi (đktc). Tính khối lượng H2O thu được sau phản ứng
`Fe + 2HCl -> FeCl_2 + H_2`
`0,2` `0,2` `0,2` `(mol)`
`n_[Fe]=[11,2]/56=0,2(mol)`
`a)m_[FeCl_2]=0,2.127=25,4(g)`
`b)V_[H_2]=0,2.22,4=4,48(l)`
`c)n_[O_2]=[4,48]/[22,4]=0,2(mol)`
`2H_2 + O_2` $\xrightarrow{t^o}$ `2H_2 O`
`0,2` `0,1` `0,2` `(mol)`
Ta có:`[0,2]/2 < [0,2]/1`
`=>O_2` dư
`=>m_[H_2 O]=0,2.18=3,6(g)`
Đúng 2
Bình luận (4)
Cho 11,2 gam Fe tác dụng với dung dịch HCL . sau phản ứng thu được sắt ( II) clorua và khí Hidro.
Tính mFeCl2
b, Tính Vh2
C. Người ta đem đốt cháy lượng H2 đó sử dụng 4,48 lít khí oxi (đktc). Tính khối lượng H2O thu được sau phản ứng
tham khảo
a) nFe= mFeMFe=11,256=0,2(mol)mFeMFe=11,256=0,2(mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
b) Theo PTHH và đề bài , ta có:
nH2=nFe=0,2(mol)nH2=nFe=0,2(mol)
Thể tích khí hiđro thu được (đktc):
=> VH2(đktc)=nH2.22,4=0,2.22,4=4,48(l)VH2(đktc)=nH2.22,4=0,2.22,4=4,48(l)
c) Ta có: nHCl= 2.nFe= 2.0,2=0,4(mol)
Khối lượng HCl cần dùng trong phản ứng:
mHCl=nHCl.MHCl= 0,4.36,5= 14,6(g)
d) Ta có:
nFeCl2=nFe=0,2(mol)nFeCl2=nFe=0,2(mol)
Khối lượng FeCl2 tạo thành:
mFeCl2=nFeCl2.MFeCl2=0,2.127=25,4(g)mFeCl2=nFeCl2.MFeCl2=0,2.127=25,4(g)
Đúng 2
Bình luận (1)
Để hòa tan hoàn toàn 28,8 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe cần vừa đủ 180 gam dung dịch HCl 18,25%. Sau phản ứng thu được V lít khí H2 và dung dịch B. Cho toàn bộ lượng H2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 1,6 gam.a) Nếu cô cạn dung dịch B thì thu được bao nhiêu gam muối khan.b) Nếu hỗn hợp A ban đầu tỉ lệ mol Fe2O3 : FeO 1:1. Tính nồng độ phần trăm của mỗi chất có trong dung d...
Đọc tiếp
Để hòa tan hoàn toàn 28,8 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe cần vừa đủ 180 gam dung dịch HCl 18,25%. Sau phản ứng thu được V lít khí H2 và dung dịch B. Cho toàn bộ lượng H2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 1,6 gam.
a) Nếu cô cạn dung dịch B thì thu được bao nhiêu gam muối khan.
b) Nếu hỗn hợp A ban đầu tỉ lệ mol Fe2O3 : FeO = 1:1. Tính nồng độ phần trăm của mỗi chất có trong dung dịch B.
Cho 11,2 gam Fe tác dụng với dung dịch HCL . sau phản ứng thu được sắt ( II) clorua và khí Hidro.
Tính mFeCl2
b, Tính Vh2
C. Người ta đem đốt cháy lượng H2 đó sử dụng 4,48 lít khí oxi (đktc). Tính khối lượng H2O thu được sau phản ứng
Mọi người giải giúp em câu C với ạ
\(\begin{array} {l} a)\\ Fe+2HCl\to FeCl_2+H_2\\ n_{Fe}=\dfrac{11,2}{56}=0,2(mol)\\ n_{FeCl_2}=n_{Fe}=0,2(mol)\\ m_{FeCl_2}=0,2.127=25,4(g)\\ b)\\ n_{H_2}=n_{Fe}=0,2(mol)\\ V_{H_2}=0,2.22,4=4,48(l)\\ c)\\ n_{O_2}=\dfrac{4,48}{22,4}=0,2(mol)\\ 2H_2+O_2\xrightarrow{t^o}2H_2O\\ \dfrac{n_{H_2}}{2}<n_{O_2}\to O_2\text{ dư}\\ n_{H_2O}=n_{H_2}=0,2(mol)\\ m_{H_2O}=0,2.18=3,6(g) \end{array}\)
Đúng 1
Bình luận (0)
a: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
nên \(n_{FeCl_2}=0,2\left(mol\right)\)
\(m_{FeCl_2}=0.2\cdot127=25,4\left(g\right)\)
b: \(V_{H_2}=0.2\cdot22.4=4.48\left(lít\right)\)
Đúng 10
Bình luận (1)
Hỗn hợp X gồm Zn, Cu, Fe3O4, Fe(NO3)2 và FeCl2 (trong đó nguyên tố Fe chiếm 19,186% về khối lượng). Cho 26,27 gam X tan hoàn toàn vào dung dịch chứa 0,69 mol HCl, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y (trong đó các muối có khối lượng là 43,395 gam) và 1,232 lít (đktc) hỗn hợp khí Z gồm N2O và khí H2 có khối lượng 1,37 gam. Cho dung dịch AgNO3 dư vào dung dịch Y, kết thúc phản ứng thấy thoát ra 0,015 mol khí NO (sản phẩm khử duy nhất của NO3-) đồng thời thu được 106,375 gam k...
Đọc tiếp
Hỗn hợp X gồm Zn, Cu, Fe3O4, Fe(NO3)2 và FeCl2 (trong đó nguyên tố Fe chiếm 19,186% về khối lượng). Cho 26,27 gam X tan hoàn toàn vào dung dịch chứa 0,69 mol HCl, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y (trong đó các muối có khối lượng là 43,395 gam) và 1,232 lít (đktc) hỗn hợp khí Z gồm N2O và khí H2 có khối lượng 1,37 gam. Cho dung dịch AgNO3 dư vào dung dịch Y, kết thúc phản ứng thấy thoát ra 0,015 mol khí NO (sản phẩm khử duy nhất của NO3-) đồng thời thu được 106,375 gam kết tủa. Thành phần phần trăm theo khối lượng của Cu có trong hỗn hợp X gần nhất với giá trị nào sau đây?
A. 32%.
B. 22%.
C. 31%.
D. 45%.