.Cho sắt (III) clorua FeCl3 tác dụng với 5,5 gam kali hidroxit thu được 7 gam sắt (III) hiđroxit Fe(OH)3 và 8,25 kali clorua. Khối lượng FeCl3 đã tham gia vào phản ứng trên *
A 9,7gam
B 9 gam
C 9,5 gam
D 9,75gam
Cho sắt (III) clorua FeCl3 tác dụng với 3,36 gam kali hidroxit thu được 2,14gam sắt (III) hidroxit Fe(OH)3 và 4,47 kali clorua. a) Viết phương trình hóa học của phản ứng b) Khối lượng FeCl3 đã tham gia vào phản ứng trên
a) PTHH: FeCl3 + 3KOH → Fe(OH)3 + 3KCl
b) Theo ĐLBTKL ta có:
\(m_{FeCl_3}+m_{KOH}=m_{Fe\left(OH\right)_3}+m_{KCl}\)
\(\Leftrightarrow m_{FeCl_3}=m_{Fe\left(OH\right)_3}+m_{KCl}-m_{KOH}=2,14+4,47-3,36=3,25\left(g\right)\)
Bài 2: Cho 5,6 gam Fe tác dụng hết với khí Clo (Cl2) thu được hợp chất Sắt (III) clorua (FeCl3)
a/ Tính thể tích khí Cl2 (đktc) đã tham gia phản ứng
b/ Tính khối lượng FeCl3 tạo thành sau phản ứng
Cho biết: Fe = 56; Cl = 35,5
\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(0.1.......0.15..........0.1\)
\(V_{Cl_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(m_{FeCl_3}=0.1\cdot162.5=16.25\left(g\right)\)
Cho 20 gam sắt III sunfat F e 2 S O 4 3 tác dụng với natri hidroxit NaOH, thu được 10,7 gam sắt III hidroxit F e ( O H ) 3 và 21,3 gam natri sunfat N a 2 S O 4 . Xác định khối lượng natri hidroxit tham gia vào phản ứng.
Sơ đồ
Sắt (III) sunfat + Natri hidroxit → Sắt (III) hidroxit + natri sunfat
Áp dụng ĐLBTKL, ta có
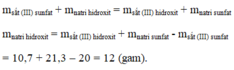
Cho 11,2 g sắt tác dụng vừa đủ với khí clo (Cl2)sau phản ứng thu được muối sắt (III) clorua (FeCl3) A. Tính thể tích khí clo cần dùng . B. Tính khối lượng muối sắt (III) clorua (FeCl3) biết Cl = 35,5 .Fe = 56.
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ 2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\\ n_{Cl_2}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ n_{FeCl_3}=n_{Fe}=0,2\left(mol\right)\\ a,V_{Cl_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ b,m_{FeCl_3}=162,5.0,2=32,5\left(g\right)\)
a, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{FeCl_3}=n_{Fe}=0,2\left(mol\right)\Rightarrow m_{FeCl_3}=0,2.162,5=32,5\left(g\right)\)
Cho 20 gam sắt(III) sunfat Fe2(SO4)3 tác dụng với natri hiđroxit NaOH, thu được 10,7 gam sắt(III) hiđroxit Fe(OH)3 và 21,3 gam natri sunfat Na2SO4. Số mol natri hiđroxit tham gia vào phản ứng là :
A. 0,5 mol.
B. 9,4 mol.
C. 12 mol.
D. 0.3 mol.
Theo ĐLBTKL:
\(m_{Fe_2\left(SO_4\right)_3}+m_{NaOH}=m_{Fe\left(OH\right)_3}+m_{Na_2SO_4}\)
=> \(m_{NaOH}=10,7+21,3-20=12\left(g\right)=>n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right)\)
=> D
Cho 20 gam sắt(III) sunfat F e 2 S O 4 3 tác dụng với natri hiđroxit (NaOH) thu được 10,7 gam sắt(III) hiđroxit F e 2 S O 4 3 và 21,3 gam natri sunfat N a 2 S O 4 Tính khối lượng natri hiđroxit tham gia phản ứng.
Cho 100 gam dung dịch kali hidroxit 14% tác dụng hết với dung dịch đồng (II) clorua 25%. a. Tính khối lượng dung dịch đồng (II) clorua đã tham gia phản ứng. b. Tính khối lượng kết tủa thu được sau phản ứng. c. Tính nồng độ phần trăm của chất trong dung dịch thu được sau phản ứng. d. Nung kết tủa Cu(OH)2 thu được trong không khí đến khối lượng không đổi. Tính khối lượng chất rắn thu được sau khi nung.
\(n_{KOH}=\dfrac{100.14}{100.56}=0,25(mol)\\ 2KOH+CuCl_2\to Cu(OH)_2\downarrow+2KCl\\ \Rightarrow n_{CuCl_2}=n_{Cu(OH)_2}=0,125(mol);n_{KCl}=0,25(mol)\\ a,m_{CuCl_2}=0,125.135=16,875(g)\\ b,m_{Cu(OH)_2}=0,125.98=12,25(g)\\ c,C\%_{KCl}=\dfrac{0,25.74,5}{100+16,875-12,25}.100\%=17,8\%\\ d,Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\\ \Rightarrow n_{CuO}=0,125(mol)\\ \Rightarrow m_{CuO}=0,125.80=10(g)\)
Cho 7,1 gam hỗn hợp A gồm kẽm và sắt (III) oxit tác dụng hết với axit clohiđric thu được 1,344 lít khí ở đktc và dung dịch chứa ZnCl2, FeCl3.
a/ Tính khối lượng axit tham gia phản ứng.
b/ Khí sinh ra phản ứng vừa đủ với 3,92 gam hỗn hợp B gồm CuO và Fe3O4 nung nóng. Xác định khối lượng các chất có trong chất rắn sau phản ứng (gồm Cu và Fe)
a)
$Zn + 2HCl \to ZnCl_2 + H_2$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
Theo PTHH : $n_{Zn} = n_{H_2} = 0,06(mol)$
$\Rightarrow n_{Fe_2O_3} = \dfrac{7,1-0,06.65}{160} = 0,02(mol)$
Theo PTHH : $n_{HCl} = 2n_{Zn} + 6n_{Fe_2O_3} = 0,24(mol)$
$m_{HCl} = 0,24.36,5 = 8,76(gam)$
b)
Gọi $n_{CuO} = x(mol) ; n_{Fe_3O_4} = y(mol) \Rightarrow 80a + 232y = 3,92(1)$
$CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
Theo PTHH : $n_{H_2} =x + 4y = 0,06(2)$
Từ (1)(2) suy ra: x = 0,02; y = 0,01
$n_{Cu} = 0,02(mol) \Rightarrow m_{Cu} = 0,02.64 = 1,28(gam)$
$n_{Fe} = 0,01.3 = 0,03(mol) \Rightarrow m_{Fe} = 0,03.56 = 1,68(gam)$
Áp dụng định luật bảo toàn khối lượng:
BT1: Cho 11,2 g Fe phản ứng vừa đủ với 21,3 g clo. Sau phản ứng sinh ra sắt(III) clorua (FeCl3).
a. Lập PTHH.
b. Tính khối lượng FeCl3 thu được.
c. Nếu có 9.1023 nguyên tử sắt phản ứng thì cần bao nhiêu phân tử clo và sinh ra bao nhiêu phân tử sắt(III) clorua?
BT2: Đốt cháy hoàn toàn 1,5 kg than (có thành phần chính là C), dùng hết 3,2 kg oxi và sinh ra 4,4 kg khí cacbonic(CO2).
a. Lập PTHH.
b. Tính hàm lượng C chứa trong mẫu than trên.
BT1 :
Bảo toàn khối lượng :
\(m_{FeCl_3}=m_{Fe}+m_{Cl_2}=11.2+21.3=32.5\left(g\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
\(1.5.....2.25......1.5\)
\(n_{Fe}=\dfrac{9\cdot10^{23}}{6\cdot10^{23}}=1.5\left(mol\right)\)
Số phân tử Cl2 : \(2.25\cdot6\cdot10^{23}=13.5\cdot10^{23}\left(pt\right)\)
Số phân tử FeCl3 : \(1.5\cdot6\cdot10^{23}=9\cdot10^{23}\left(pt\right)\)
BT2:
\(C+O_2\underrightarrow{^{^{t^0}}}CO_2\)
Bảo toàn khối lượng :
\(m_C+m_{O_2}=m_{CO_2}\)
\(m_C=m_{CO_2}-m_{O_2}=4.4-3.2=1.2\left(kg\right)\)
\(\%C=\dfrac{1.2}{1.5}\cdot100\%=80\%\)