Tính thành phần % khối lượng các ng.tố trong hợp chất: Fe3O4 ; H2SO4.
(giúp mk với ;^;)
Hợp chất A có p.tử gồm 2ng.tử Fe và 3 ng.tử O.
a) viết CTHH của hợp chất A
b) Xđ thành phần % theo khối lượng các ng.tố hóa học có trong hợp chất A
c) Trong 2 mol p.tử A có nhiêu mol ng.tử của mỗi ng.tố ?
a) Fe2O3
b) %Fe = (2 .56).100%/160=70%
%O = 100% - 70% = 30 %
c) Trong 2 mol phân tử A có : 4 mol nguyên tử Fe và 6 mol nguyên tử O
a) Công thức hóa học của A: Fe2O3
b) \(\%m_{Fe}=\frac{56.2}{56.2+16.3}.100\%=70\%\)
\(\Rightarrow\%m_O=100\%-70\%=30\%\)
c) Trong 2 mol phân tử A có 4 mol Fe và 6 mol O
Cho Fe cháy trong O ở nhiệt độ cao, thu được Oxit sắt từ (Fe3O4).a, Hãy tính MFe3O4 tạo thành nếu sử dụng hết 16,8g Feb, Tính thành phần % về khối lượng của nguyên tố Fe trong hợp chất Fe3O4
1) 1 hợp chất tạo bởi ng.tố M chưa có hoá trị với ng.tố O trong đó M chiếm 60% về khối lượng
a) Tìm CT hợp chất
b) Tính hoá trị của M
Gọi CTHH của hợp chất là: MxOy
Theo đề bài ra ta có: MM.x / MM.x + 16y = 60%
<=> 40MM.x = 960y => MM = 960y / 40x = 2y/x . 12
Vì 2y/x là hoá trị của M => 2y/x có thể nhận các giá trị: 1,2,3,4,5,6,7,8/3
Thay các giá trị trên chỉ có gtrị 2y/x = 2 và MM = 24
Công thức của hợp chất là MgO và hoá trị của M là 2
a)%M+%O=100%
->60%+%O=100%
->%O=100%-60%=40%
Gọi CTHH là MxOy-> hóa trị của M là 2y/x->2y/x có thể nhận các giá trị 1,2,3,4,5,6,7,8/3
%M/%O=60%/40%=3/2
Mm.x/Mo.y=Mm.x/16y
=3/2
->Mm=24y/x=2y/x.12
+)2y/x=1->Mm=12
+)2y/x=2->Mm=24
+)2y/x=3->Mm=36
+)2y/x=8/3->Mm=32
+)2y/x=4->Mm=48
+)2y/x=5->Mm=60
+)2y/x=6->Mm=72
+)2y/x=7->Mm=84
-->CTHH:MgO
b)hóa trị của M là 2
tìm thành phần phần trăm ( theo khối lượng ) của các nguyên tố hóa học có trong nhưng hợp chất sau
a/Fe2O3 b/Fe3O4 c/SO3 d/CuSO4 g/CH4
a) Fe2O3----> \(\dfrac{56.2}{56.2+16.3}.100\%=70\%\\ =>100\%-70\%=30\%\)
b) Fe3O4---->\(\dfrac{56.3}{56.3+16.4}.100\%=72,41\%\\ =>100\%-72,41\%=27,59\%\)
c)SO3---->\(\dfrac{32}{32+16.3}.100\%=40\%\\ =>100\%-40\%=60\%\)
Câu 1: Thành phần phần trăm về khối lượng của nguyên tố Fe trong hợp chất Fe3O4 là:
A. 72,4%
B. 68,8%
C. 76%
D. 62,5%
Câu 2: Hợp chất X có khối lượng mol phân tử là 232 g/mol, thành phần phần trăm khối lượng của Fe là 72,41%, còn lại là của O. Công thức hóa học của X là
A. Fe3O4.
B. FeO.
C. Fe3O2.
D. Fe2O3.
Câu 3: Trong 1 mol phân tử FeCl3 có bao nhiêu gam nguyên tử clo?
A. 71,0 gam.
B. 35,5 gam.
C. 142,0 gam
D. 106,5 gam.
Câu 4: Có bao nhiêu mol nguyên tử O trong 1 mol phân tử N2O5?
A. 2 mol.
B. 4 mol.
C. 5 mol.
D. 3 mol.
Câu 5: Khối lượng của Fe trong 92,8 g Fe3O4 là
A. 25,6 g.
B. 67,2 g.
C. 80 g.
D. 10 g.
Câu 1: Thành phần phần trăm về khối lượng của nguyên tố Fe trong hợp chất Fe3O4 là:
A. 72,4%
B. 68,8%
C. 76%
D. 62,5%
Câu 2: Hợp chất X có khối lượng mol phân tử là 232 g/mol, thành phần phần trăm khối lượng của Fe là 72,41%, còn lại là của O. Công thức hóa học của X là
A. Fe3O4.
B. FeO.
C. Fe3O2.
D. Fe2O3.
Câu 3: Trong 1 mol phân tử FeCl3 có bao nhiêu gam nguyên tử clo?
A. 71,0 gam.
B. 35,5 gam.
C. 142,0 gam
D. 106,5 gam.
Câu 4: Có bao nhiêu mol nguyên tử O trong 1 mol phân tử N2O5?
A. 2 mol.
B. 4 mol.
C. 5 mol.
D. 3 mol.
Câu 5: Khối lượng của Fe trong 92,8 g Fe3O4 là
A. 25,6 g.
B. 67,2 g.
C. 80 g.
D. 10 g.
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:
a) CO và CO2.
b) Fe3O4 và Fe2O3.
c) SO2 và SO3.
a) Hợp chất CO có MCO = 12 + 16 = 28 g/mol
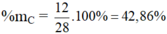
%mO = 100 – 42,86 = 57,14%
Hợp chất CO2: có MCO2 = 12 + 32 = 44 g/mol
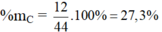
%mO = 100 – 27,3 = 72,7%
b) Hợp chất Fe3O4: MFe3O4 = 3.56 + 4.16 = 232 g/mol
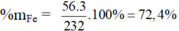
%mO = 100 – 72,4 = 27,6%
Hợp chất Fe2O3: MFe2O3 = 2.56 + 3.16 = 160 g/mol
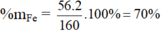
%mO = 100 – 70 = 30%
c) Hợp chất SO2 : MSO2 = 32 + 2.16 = 64 g/mol
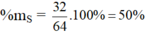
%mO = 100 – 50 = 50%
Hợp chất SO3 : MSO3 = 32 + 16.3 = 80 g/mol
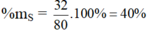
%mO = 100 – 40 = 60%
Nêu các bước tiến hành tính thành phần % khối lượng của các nguyên tố khi biết CTHH của hợp chất? Áp dụng: Tính thành phần % khối lượng của các nguyên tố trong các hợp chất: SO2, CuSO4, H3PO4, K2CO3
+ Bước 1: Tính M của hợp chất.
+ Bước 2: Xác định số mol nguyên tử mỗi nguyên tố trong hợp chất.
Ví dụ 1: Xác định thành phần phần trăm theo khối lượng của các nguyên tố có trong hợp chất KNO3
Lời giải
+ MKNO3 = 39_+ 14+16.3=101 gam
+ Trong 1 mol KNO3 có:
1 mol nguyên tử K
1 mol nguyên tử N
3 mol nguyên tử O
+ %K= (39.100):101=36,8%
+ %N= (14.100):101=13,8%
+ %K= (48.100):101=47,6%
Hoặc %O=100%-(36,8%+13,8%)=47,6%
Ví dụ 2: Tính thành phần phần trăm theo khối lượng của các nguyên tố có trong hợp chất Fe2O3
Lời giải
+ MFe2O3 = 56.2+16.3= 160 gam
+ Trong 1 mol Fe2O3 có:
2 mol nguyên tử Fe
3 mol nguyên tử O
+ %Fe = (112.100):160 = 70%
+ %O = (48.100):160 = 30%
Hoặc %O = 100% - 70% = 30%
*bn áp dụng theo cái này nha
Nêu các bước tiến hành tính thành phần % khối lượng của các nguyên tố khi biết CTHH của hợp chất? Áp dụng: Tính thành phần % khối lượng của các nguyên tố trong các hợp chất: SO2, CuSO4, H3PO4, K2CO3
Đốt cháy 20 gam bột sắt trong bình chứa V lít khí O2 đo ở đktc thu được 26,4 gam hỗn hợp chất rắn X gồm Fe và Fe3O4. Biết các phản ứng xảy ra hoàn toàn.
a. Tính giá trị của V?
b. Tính phần trăm khối lượng Fe3O4 trong hỗn hợp X?
c. Tính khối lượng KClO3 hoặc KMnO4 cần dùng để điều chế ra lượng oxi cho phản ứng học trên?
a)
Theo ĐLBTKL: \(m_{Fe\left(bđ\right)}+m_{O_2}=m_X\)
=> \(m_{O_2}=26,4-20=6,4\left(g\right)\)
=> \(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\Rightarrow V=0,2.22,4=4,48\left(l\right)\)
b)
PTHH: 3Fe + 2O2 --to--> Fe3O4
0,2------->0,1
=> \(\%m_{Fe_3O_4}=\dfrac{0,1.232}{26,4}.100\%=87,88\%\)
c)
- Nếu dùng KClO3
PTHH: 2KClO3 --to--> 2KCl + 3O2
\(\dfrac{0,4}{3}\)<-----------------0,2
=> \(m_{KClO_3}=\dfrac{0,4}{3}.122,5=\dfrac{49}{3}\left(g\right)\)
- Nếu dùng KMnO4:
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,4<--------------------------------0,2
=> \(m_{KMnO_4}=0,4.158=63,2\left(g\right)\)