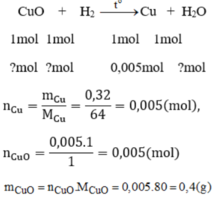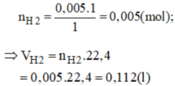Cho khí hidro dư đi qua đồng (II) oxit nóng màu đen, người ta thu được 0,32g kim loại đồng màu đỏ và hơi nước ngưng tụ. Tính lượng nước ngưng tụ thu được sau phản ứng.

Những câu hỏi liên quan
Cho khí hidro dư đi qua đồng (II) oxit nóng màu đen, người ta thu được 0,32g kim loại đồng màu đỏ và hơi nước ngưng tụ. Tính lượng đồng (II) oxit tham gia phản ứng.
Cho khí hidro dư đi qua đồng (II) oxit nóng màu đen, người ta thu được 0,32g kim loại đồng màu đỏ và hơi nước ngưng tụ. Tính thể tích khí hidro ở đktc đã tham gia phản ứng.
Cho khí hidro dư đi qua đồng (II) oxit nóng màu đen, người ta thu được 0,32g kim loại đồng màu đỏ và hơi nước ngưng tụ. Viết phương trình hóa học xảy ra.
cho khí hiđro dư đi qua bột đồng ( II ) oxit CuO nóng màu đen , người ta thu được 1,6g kim loại đồng màu đỏ và một lượng hơi nước ngưng tụ , khối lượng đồng ( II ) oxit phản ứng là
Ta có: \(n_{Cu}=\dfrac{1,6}{64}=0,025\left(mol\right)\)
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT ta có: \(n_{CuO}=n_{Cu}=0,025\left(mol\right)\)
Khối lượng đồng (II) oxit phản ứng là:
\(m_{CuO}=0,025.80=2\left(g\right)\)
Đúng 0
Bình luận (0)
\(n_{Cu}=\dfrac{1,6}{64}=0,025\left(mol\right)\)
PTHH: \(H_2+CuO\underrightarrow{t^0}Cu+H_2O\)
Theo PTHH: \(n_{CuO}:n_{Cu}=1:1\Rightarrow n_{CuO}:n_{Cu}=0,025\left(mol\right)\)
\(\Rightarrow m_{CuO}=n_{CuO}.M_{CuO}=0,025.80=2\left(g\right)\)
Đúng 0
Bình luận (0)
PTHH. CuO + H2 -> H2O + Cu
Theo bài:
nCu = \(\dfrac{1,6}{64}=0,025\left(mol\right)\)
Theo pthh và bài có:
nCuO = nCu = 0,025 (mol)
=>mCuO = 0,025 . 80 = 2 (g)
Đúng 0
Bình luận (0)
Cho luồng khí Hydrogen dư đi qua ống sứ đựng bột Copper (II) Oxide nung nóng, bột Oxide màu đen chuyển thành kim loại đồng màu đỏ và hơi nước ngưng tụa) Viết PTHH của phản ứng xảy ra?b) Cho biết thu được `12,8` g kim loại đồng, hãy tính:`-` Khối lượng Cu (II) Oxide đã tham gia phản ứng.`-` Thể tích khí Hydrogen ở đkc `(25^0 C` và `1` bar`)` đã tham gia phản ứng.`-` Khối lượng hơi nước ngưng tụ tạo thành sau phản ứng._____Yc: Không copy, sao chép câu trả lời từ các nguồn khác. Hoàn toàn là câu tr...
Đọc tiếp
Cho luồng khí Hydrogen dư đi qua ống sứ đựng bột Copper (II) Oxide nung nóng, bột Oxide màu đen chuyển thành kim loại đồng màu đỏ và hơi nước ngưng tụ
a) Viết PTHH của phản ứng xảy ra?
b) Cho biết thu được `12,8` g kim loại đồng, hãy tính:
`-` Khối lượng Cu (II) Oxide đã tham gia phản ứng.
`-` Thể tích khí Hydrogen ở đkc `(25^0 C` và `1` bar`)` đã tham gia phản ứng.
`-` Khối lượng hơi nước ngưng tụ tạo thành sau phản ứng.
_____
Yc: Không copy, sao chép câu trả lời từ các nguồn khác. Hoàn toàn là câu trả lời của mình.
\(H_2+CuO\rightarrow\left(t^o\right)Cu+H_2O\)
0,2 0,2 0,2 0,2
\(b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\)
\(m_{CuO}=0,2.80=16\left(g\right)\)
\(V_{H_2}=0,2.24,79=4,958\left(l\right)\)
\(m_{H_2O}=0,2.18=3,6\left(g\right)\)
Đúng 3
Bình luận (0)
Cho 11,2 lít khí hiđro tác dụng với CuO thu được kim loại đồng màu đỏ gạch và hơi nước a) Viết PTHH b) Tính khối lượng đồng thu được sau phản ứng c) Thể tích hơi nước thu được sau phản ứng
\(n_{H_2}=\dfrac{V_{H_2}}{22,4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
a) \(H_2+CuO\rightarrow Cu+H_2O\)
0,5---0,5-------0,5----0,5
Khối lượng đồng thu được:
\(m_{Cu}=n_{Cu}.M_{Cu}=0,5.64=32\left(g\right)\)
Thể tích hơi nước sau phản ứng:
\(V_{H_2O}=n_{H_2O}.22,4=0,5.22,4=11,2\left(l\right)\)
Đúng 2
Bình luận (0)
Dẫn dòng khí H2 dư đi qua 8 g bột CuO màu đen nung nóng thấy tạo ra bột Cu màu đỏ kèm theo hơi nước a.xác định khối lượng đồng thu được sau khi phản ứng kết thúc b.tính thể tích khí hiđro ở điều kiện tiêu chuẩn đã tham gia phản ứng trên
1. Cho khí Hidro dư qua đồng (II) Oxit (CuO) nóng màu đen, người ta thu được 0,32 g kim loại đồng màu đỏ và hơi nước ngưng tụ
a. Viết phương trình hóa học xảy ra
b. Tính khối lượng CuO tham gia phản ứng?
c. Tính thể tích khí Hidro ở điều kiện tiêu chuẩn (đktc) đã tham gia phản ứng?
d. Tính khối lượng nước ngưng tụ thu được sau phản ứng
2. Đốt cháy hoàn toàn 0, 3 mol khí metan (CH4) trong không khí sinh ra 13,2 gam khí cacbon dioxit và 10,8 gam nước. Hãy tính thể tích cần dùng ở điều kiện ti...
Đọc tiếp
1. Cho khí Hidro dư qua đồng (II) Oxit (CuO) nóng màu đen, người ta thu được 0,32 g kim loại đồng màu đỏ và hơi nước ngưng tụ
a. Viết phương trình hóa học xảy ra
b. Tính khối lượng CuO tham gia phản ứng?
c. Tính thể tích khí Hidro ở điều kiện tiêu chuẩn (đktc) đã tham gia phản ứng?
d. Tính khối lượng nước ngưng tụ thu được sau phản ứng
2. Đốt cháy hoàn toàn 0, 3 mol khí metan (CH4) trong không khí sinh ra 13,2 gam khí cacbon dioxit và 10,8 gam nước. Hãy tính thể tích cần dùng ở điều kiện tiêu chuẩn. (Biết rằng khí metan cháy trong không khí là tác dụng với khí oxi. Và oxi chiếm 1/5 thể tích không khí)
Bài 1:
a) H2 + CuO \(\underrightarrow{to}\) Cu + H2O
\(n_{Cu}=\dfrac{0,32}{32}=0,01\left(mol\right)\)
b) Theo PT: \(n_{CuO}=n_{Cu}=0,01\left(mol\right)\)
\(\Rightarrow m_{CuO}=0,01\times80=0,8\left(g\right)\)
c) Theo PT: \(n_{H_2}=n_{Cu}=0,01\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,01\times22,4=0,224\left(l\right)\)
d) Theo pT: \(n_{H_2O}=n_{Cu}=0,01\left(mol\right)\)
\(\Rightarrow m_{H_2O}=0,01\times18=0,18\left(g\right)\)
Đúng 0
Bình luận (0)
Bài 2:
\(m_{CH_4}=0,3\times16=4,8\left(g\right)\)
CH4 + 2O2 \(\underrightarrow{to}\) CO2 + 2H2O
Theo ĐL BTKL ta có:
\(m_{CH_4}+m_{O_2}=m_{CO_2}+m_{H_2O}\)
\(\Leftrightarrow4,8+m_{O_2}=13,2+10,8\)
\(\Leftrightarrow m_{O_2}=13,2+10,8-4,8=19,2\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{19,2}{32}=0,6\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,6\times22,4=13,44\left(l\right)\)
\(\Rightarrow V_{KK}=13,44\times5=67,2\left(l\right)\)
Đúng 0
Bình luận (0)
Cho khí hiđrô (H_2) đi qua đồng (II) oxit (CuO) nung nóng màu đen, người ta thu được 0.32g kim laoij đồng (Cu) màu đỏ và hơi nước (H_2O) ngưng tụ:
a) Viết phương trình hóa học xảy ra
b) Tính khối lượng đồng (II) oxit tham gia phản ứng
c) Tính thể tích khí hiđrô ở đktc đã tham gia phản ứng
( Biết: M_{Cu} 64g/mol ; M_O 16g/mol)
Đọc tiếp
Cho khí hiđrô (\(H_2\)) đi qua đồng (II) oxit (CuO) nung nóng màu đen, người ta thu được 0.32g kim laoij đồng (Cu) màu đỏ và hơi nước (\(H_2O\)) ngưng tụ:
a) Viết phương trình hóa học xảy ra
b) Tính khối lượng đồng (II) oxit tham gia phản ứng
c) Tính thể tích khí hiđrô ở đktc đã tham gia phản ứng
( Biết: \(M_{Cu}\)= 64g/mol ; \(M_O\)= 16g/mol)
Ta có: \(n_{Cu}=\dfrac{0,32}{64}=0,005\left(mol\right)\)
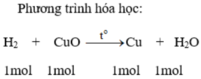
a, PTHH: CuO + H2 -to-> H2 + CuO
b, Ta có: \(n_{CuO}=n_{H_2}=n_{Cu}=0,005\left(mol\right)\)
=> \(m_{CuO}=0,005.80=0,4\left(g\right)\)
c) \(V_{H_2\left(đktc\right)}=0,005.22,4=0,112\left(l\right)\)
Đúng 0
Bình luận (0)
nCu=m/M=0,32/64=0,005 (mol)
PT:
CuO + H2 -t0-> Cu +H2O
1...........1............1...........1 (mol)
0,005<- 0,005<-0,005->0,005 (mol)
b) => mCuO=n.M=0,005.80=0,4 (g)
c) VH2=n.22,4=0,005.22,4=0,112(lít)
Đúng 0
Bình luận (0)