Biết rằng, kim loại nhôm tác dụng với axit sunfuric H 2 S O 4 tạo ra chat nhôm sunfat A l 2 S O 4 3 và khí hidro. Viết chương trình hóa học của phản ứng. Hiểu như thế nào về tỉ lệ số nguyên tử, số phân tư giữa các chất trong phản ứng?

Những câu hỏi liên quan
Biết rằng, kim loại nhôm tác dụng với axit sunfuric
H
2
S
O
4
tạo ra chat nhôm sunfat
A
l
2
S
O
4
3
và khí hidro. Cũng câu hỏi như trên, nếu có
3
,
01
.
10
23
...
Đọc tiếp
Biết rằng, kim loại nhôm tác dụng với axit sunfuric H 2 S O 4 tạo ra chat nhôm sunfat A l 2 S O 4 3 và khí hidro. Cũng câu hỏi như trên, nếu có 3 , 01 . 10 23 nguyên tử Al.
Nếu có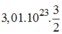 nguyên tử Al tác dụng với:
nguyên tử Al tác dụng với:
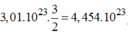 phân tử
H
2
S
O
4
phân tử
H
2
S
O
4
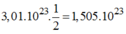 phân tử
A
l
2
S
O
4
3
.
phân tử
A
l
2
S
O
4
3
.
Và tạo ra: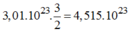 phân tử
H
2
phân tử
H
2
Đúng 0
Bình luận (0)
Biết rằng, kim loại nhôm tác dụng với axit sunfuric
H
2
S
O
4
tạo ra chat nhôm sunfat
A
l
2
S
O
4
3
và khí hidro. Nếu có
6
,
02
.
10
23
nguyên tử Al sẽ tác dụn...
Đọc tiếp
Biết rằng, kim loại nhôm tác dụng với axit sunfuric H 2 S O 4 tạo ra chat nhôm sunfat A l 2 S O 4 3 và khí hidro. Nếu có 6 , 02 . 10 23 nguyên tử Al sẽ tác dụng được với bao nhiêu phân tử H 2 S O 4 tạo ra bao nhiêu phân tử A l 2 S O 4 3 và bao nhiêu phân tử H 2 ?
Nếu có có 6 , 02 . 10 23 nguyên tử Al sẽ tác dụng với:
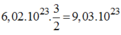 phân tử
H
2
S
O
4
phân tử
H
2
S
O
4
Và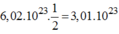 phân tử
A
l
2
S
O
4
3
phân tử
A
l
2
S
O
4
3
Tạo ra: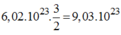 phân tử
H
2
phân tử
H
2
Đúng 0
Bình luận (0)
Biết rằng kim loại nhôm tác dụng với axit sunfuric
H
2
S
O
4
tạo ra khi hidro H2 và chất nhôm sunfat
A
l
2
S
O
4
3
. Lập phương trình hóa học của phản ứng.
Đọc tiếp
Biết rằng kim loại nhôm tác dụng với axit sunfuric H 2 S O 4 tạo ra khi hidro H2 và chất nhôm sunfat A l 2 S O 4 3 . Lập phương trình hóa học của phản ứng.
2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
Đúng 0
Bình luận (0)
Biết rằng kim loại nhôm tác dụng với axit sunfuric
H
2
S
O
4
tạo ra khi hidro
H
2
và chất nhôm sunfat
A
l
2
S
O
4
3
. Cho biết tỉ lệ giữa sô nguyên tử Al lần lượt với số phân tử của ba chất tr...
Đọc tiếp
Biết rằng kim loại nhôm tác dụng với axit sunfuric H 2 S O 4 tạo ra khi hidro H 2 và chất nhôm sunfat A l 2 S O 4 3 . Cho biết tỉ lệ giữa sô nguyên tử Al lần lượt với số phân tử của ba chất trong phản ứng.
Số nguyên tử Al: số phân tử H 2 S O 4 = 2:3
Số nguyên tử Al : số phân tử A l 2 S O 4 3 = 2: 1
Số nguyên tử Al : số phân tử H 2 = 2:3
Đúng 0
Bình luận (0)
Biết rằng kim loại nhôm tác dụng với axit sunfuric H2SO4 tạo ra nhôm sunfat Al2(SO4)3 và khí hiđro
A) lậpphương trình hóa học của phản ứng
B) cho biết tỉ lệ số nguyên tử nhôm lần lượt với số phân tử của 3 chất khác trong phản ứng
a) 2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2
b) Số nguyên tử Al : số phân tử H2SO4 = 2 : 3
Số nguyên tử Al : số phân tử Al2(SO4)3 = 2 : 1
Số nguyên tử Al : số phân tử H2 = 2 : 3
Đúng 0
Bình luận (0)
a) 2Al+ 3H2SO4 -> Al2(SO4)3 +3 H2
b) Tỉ lệ của:
- Nguyên tử Al với Số phân tử H2SO4
2:3
- Nguyên tử Al với số phân tử Al2(SO4)3
2:1
- Nguyên tử Al với số phân tử H2
2:3
Đúng 0
Bình luận (0)
a/ PTHH: 2Al + 3H2SO4 ===> Al2(SO4)3 + 3H2
b/ Tỉ lệ:
Số nguyên tử nhôm : số phân tử H2SO4 = 2 : 3Số nguyên tử nhôm : số phân tử Al2(SO4)3 = 2 : 1Số nguyên tử nhôm : số phân tử H2 = 2 : 3
Đúng 0
Bình luận (0)
Câu 7: Cho nhôm tác dụng với axit sunfuric sinh ra muối nhôm sunfat và 17,92 lít khí hidro đo ở đktc. Tính khối lượng axit phản ứng, muối sinh ra và kim loại phản ứng.
Câu 8: Cho nhôm oxit tác dụng với axit nitric sinh ra muối nhôm sunfat và 7,2g nước . Tính khối lượng axit phản ứng, muối sinh ra và kim loại phản ứng.
giúp mik với nha :)))
Câu 7 :
\(n_{H2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
\(\dfrac{8}{15}\) 0,8 \(\dfrac{4}{15}\) 0,8
\(n_{H2SO4}=\dfrac{0,8.3}{3}=0,8\left(mol\right)\)
⇒ \(m_{H2SO4}=0,8.98=78,4\left(g\right)\)
\(n_{Al2\left(SO4\right)3}=\dfrac{0,8.1}{3}=\dfrac{4}{15}\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=\dfrac{4}{15}.342=91,2\left(g\right)\)
\(n_{Al}=\dfrac{0,8.2}{3}=\dfrac{8}{15}\left(mol\right)\)
⇒ \(m_{Al}=\dfrac{8}{15}.27=14,4\left(g\right)\)
Chúc bạn học tốt
Đúng 3
Bình luận (1)
bài 8
Al2O3+6HNO3->2Al(NO3)3+3H2
\(\dfrac{2}{15}\)------------0,8-------\(\dfrac{4}{15}\)----------0,4 mol
n H2O=\(\dfrac{7,2}{18}\)=0,4 mol
=>m Al2O3=\(\dfrac{2}{15}\).102=13,6g
=>m HNO3=0,8.63=50,4g
=>m Al(NO3)3=\(\dfrac{4}{15}\).213=56,8g
Đúng 2
Bình luận (0)
Bài 7
2Al+3H2SO4->Al2(SO4)3+3H2
\(\dfrac{8}{15}\)------0,5-----------\(\dfrac{4}{15}\)--------0,8
n H2=\(\dfrac{17,92}{22,4}\)=0,8 mol
=>m Al= \(\dfrac{8}{15}\).27=14,4g
=>m HCl=0,5.36,5=18,25g
=>m Al2(SO4)3=\(\dfrac{4}{15}\).342=91,2g
Đúng 4
Bình luận (0)
Xem thêm câu trả lời
Cho kim loại nhôm tác dụng với axit sunfuric (H2SO4) tạo ra khí hidro (H2) và hợp chất nhôm sunfat Al2(SO4)3.
a) Lập PTHH.
b) Cho biết tỉ lệ nguyên tử nhôm Al lần lượt với ba chất còn lại trong phản ứng hóa học.
bạn vô link này đi sẽ có nhiều người giúp https://www.facebook.com/groups/1515719195121273/
Đúng 0
Bình luận (0)
Cho 27gam kim loại nhôm Al tác dụng với dung dịch axit sunfuric H2 SO4 thu được171gam muối nhôm sunfat Al2 (SO4) và 3 gam khi hidro H2
a) Lập phương trình hóa học
Cho biết tỉ lệ giữa số nguyên tử nhôm lần lượt với số phân tử của ba chất trong phản ứng
b) Tính khối lượng của axit sunfuric H2 SO4
a) PTHH là: 2Al + H2SO4 → Al2(SO4) + H2.
Tỉ lệ giữa số nguyên tử Al lần lượt với số phân tử của ba chất trong phản ứng đều là 2:1
b) nAl =27/27 = 1 (mol)
theo PTHH ta có: số mol của H2SO4 = 1/2 * nAl = 1/2*1 =0.5 (mol)
khối lượng của H2SO4 là: 0.5 * (1*2+32+16*4) =49 (g).
Đúng 0
Bình luận (0)
Nhôm tác dụng với axit sunfuric tạo ra nhôm sunfat và khí hidro
a) Viết PTHH xảy ra
b) Tính thể tích khí hidro(ở đktc) thu được khi có 10,8 gam nhôm phản ứng
c) Tính khối lượng axit H2SO4 đã phản ứng để thu được 11,2 lít khí hidro( ở đktc)
HD:
a,
2AL+3H2SO4=>AL2(SO4)3+3H2
b,
Ta có: nAL=10.8/27=0.4(mol)
theo phương trình ta có: nH2=3/2nAL=0.6(mol)
=> VCO2=0.6*22.4=13.44(lít)
c,
Ta có: nH2=11.2/22.4=0.5(mol)
theo phương trình ta có: nH2SO4=nH2=0.5(mol)
=>mH2SO4=0.5*98=49(g)
Đúng 0
Bình luận (3)


















