Cho sơ đồ phản ứng: Fe 3 O 4 + HNO 3 → Fe ( NO 3 ) 3 + NO + H 2 O
Sau khi cân bằng, tỉ lệ số phân tử bị oxi hóa và số phân tử bị khử là
A. 28 : 3.
B. 1 : 3.
C. 3 : 1.
D. 3: 28.
cho các sơ đồ phản ứng sau:
a) Fe+O2--->Fe2O3
b) Al2O3+HCl---> AlCl3+H2O
c) Cu+HNO3--->Cu(NO3)2+NO2+H2Olập phương trình hoá học của các phản ứng trên. cho biết tỷ lệ số nguyên tử phân tư của phản ứng (a) (b)a) 4Fe+3O2--->2Fe2O3
Tỉ lệ: số nguyên tử Fe : số phân tử O2 : số phân tử Fe2O3
b) Al2O3 + 6HCl ---> 2AlCl3 + 3H2O
Tỉ lệ: số phân tử Al2O3 : số phân tử HCl : số phân tử AlCl3 : số phân tử H2O = 1 : 6 : 2 : 3
c) Cu+4HNO3 --->Cu(NO3)2+2NO2+2H2OTỉ lệ: số nguyên tử Cu : số phân tử HNO3 : số phân tử Cu(NO3)2 : số phân tử NO2 : số phân tử H2O = 1 : 4 : 1 : 2 : 2
Bài 1: Cho sơ đồ của các phản ứng sau:
a) HgO → Hg + O 2 .
b) Fe(OH) 3 → Fe 2 O 3 + H 2 O
Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử, số phân tử của các
chất trong mỗi phản ứng.
Bài 2: Cho sơ đồ phản ứng sau:
Na 2 CO 3 + CaCl 2 → CaCO 3 + NaCl.
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ số phân tử của 4 cặp chất trong phản ứng (tùy chọn).
Bài 3: Biết rằng kim loại magie Mg tác dụng với axit sunfuric H 2 SO 4 tạo ra khí
hiđro H 2 và chất magie sunfat MgSO 4 .
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ số nguyên tử magie lần lượt với số phân tử của ba chất khác
trong phản ứng.
Bài 4: Biết rằng photpho đỏ P tác dụng với khí oxi tạo hợp chất P 2 O 5 .
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ số nguyên tử P lần lượt với số phân tử của hai chất khác
trong phản ứng.
Bài 5: Lập PTHH:
1/ Al + O 2 = Al2O3
2 / Al(0H)3 = Al2O3 + H2O
3/ Al203 + HCl = AlCl3 + H20
4/ Al + HCl → AlCl3 + H2
5/ CH4 + O2 = CO2 + H2O
6/ Fe + HCl → FeCl 2 + H 2
7/ K 2 O + H 2 O → KOH
8/ Na + H 2 O → NaOH + H 2
9/ Fe + Cl2 -> FeCl3
10/ CaCl 2 + Na 2 CO 3 -> NaCl + CaCO 3
Bài 5:
\(1:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
2: \(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
\(3:Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
4: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
5: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
6: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
7: \(K_2O+H_2O\rightarrow2KOH\)
8: \(2Na+2H_2O\rightarrow2NaOH+H_2\uparrow\)
9: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
10: \(CaCl_2+Na_2CO_3\rightarrow CaCO_3\downarrow+2NaCl\)
Cho các sơ đồ phản ứng sau: a) Fe3 O4 +CO => Fe + H2 OO
b) MnO2 + HCl => MnCl2 + Cl2 + H2 O
c) HNO3 +Cu => Cu(NO3)2 + NO + H2 O
Hãy lập các PTHH và cho biết tỉ lệ số phân tử của các chất, cặp chất trong từng phản ứng.
a; Fe3O4 +4CO => 3Fe + 4H2O
Số phân tử Fe3O4 : số phân tử CO:số nguyên tử Fe:số phân tử H2O=1:4:3:4
b) MnO2 + 4HCl => MnCl2 + Cl2 + 2H2O
tương tự
c) 8HNO3 +3Cu => 3Cu(NO3)2 + 2NO + 4H2O
tương tự
Lập phương trình hoá học cho các sơ đồ phản ứng sau:
a/ Na + O 2 ---> Na 2 O
b/ Fe + O 2 ---> Fe 3 O 4
c/ Al + HCl ---> AlCl 3 + H 2
d/ NaOH + H 2 SO 4 ---> Na 2 SO 4 +H 2 O
e/ Ba + O 2 BaO.
f/ KClO 3 KCl + O 2 .
g/Fe + O 2 Fe 3 O 4 .
h/ Al + CuSO 4 Al 2 (SO 4 ) 3 + Cu.
\(a,4Na+O_2\xrightarrow{t^o}2Na_2O\\ b,3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ c,2Al+6HCl\to 2AlCl_3+3H_2\\ d,2NaOH+H_2SO_4\to Na_2SO_4+2H_2O\\ e,2Ba+O_2\xrightarrow{t^o}2BaO\\ f,2KClO_3\xrightarrow[MnO_2]{t^o}2KCl+3O_2\\ g,3Fe+2O_2\xrightarrow{t^o}Fe_3O_4\\ h,2Al+3CuSO_4\to Al_2(SO_4)_3+3Cu\)
Cho sơ đồ phản ứng Fe2O3 + CO ----> FexOy + CO2
lập phương trình hóa học của phản ứng
Bài làm:
xFe2O3 + (3x - 2y ) CO (tº) ----> 2 FexOy + (3x- 2y )CO2
Chúc bạn học giỏi
Câu 01:
Lập các phương trình phản ứng OXHK sau theo phương pháp thăng bằng electron
a. Al + O 2 → Al 2 O 3 .
b. Fe + H 2 SO 4 đặc, nóng → Fe 2 (SO 4 ) 3 + SO 2 + H 2 O
c. Fe 3 O 4 + HNO 3 → Fe(NO 3 ) 3 + NO 2 + H 2 O.
d. Al + HNO 3 → Al(NO 3 ) 3 + NO + N 2 O + H 2 O. Biết tỉ khối hỗn hợp khí (NO, N 2 O) so với H 2 =19,2.
e. M + HNO 3 → M(NO 3 ) n + N x O y + H 2 O.
Câu 02:
Hòa tan hoàn toàn 20,85 gam hỗn hợp Al, Fe vào dung dịch HCl 20% (đủ) thu được dung dịch X và 11,76 lít (đktc) khí.
a.Tính % khối lượng từng kim loại trong hỗn hợp đầu.
b. Tính khối lượng dung dịch HCl 20% cần dùng.
c. Cô cạn cẩn thận dung dịch X thu được bao nhiêu gam muối khan?
Câu 1:
a) 4Al + 3O2 --to--> 2Al2O3
| 2Al0 -6e --> Al2+3 | x2 |
| O20 +4e--> 2O-2 | x3 |
b) 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 +6 H2O
| 2Fe0-6e-->Fe2+3 | x1 |
| S+6 +2e--> S+4 | x3 |
c) Fe3O4 + 10HNO3 --> 3Fe(NO3)3 + NO2 + 5H2O
| \(Fe_3^{+\dfrac{8}{3}}-1e->3Fe^{+3}\) | x1 |
| \(N^{+5}+1e->N^{+4}\) | x1 |
d) \(10Al+38HNO_3->10Al\left(NO_3\right)_3+2NO+3N_2O+19H_2O\)
\(\dfrac{30.n_{NO}+44.n_{N_2O}}{n_{NO}+n_{N_2O}}=19,2.2=38,4=>\dfrac{n_{NO}}{n_{N_2O}}=\dfrac{2}{3}\)
| Al0 -3e --> Al+3 | x10 |
| 38H+ + 8NO3- +30e--> 2NO + 3N2O + 19H2O | x1 |
e) \(\left(5x-2y\right)M+\left(6nx-2ny\right)HNO_3->\left(5x-2y\right)M\left(NO_3\right)_n+nN_xO_y+\left(3nx-ny\right)H_2O\)
| M0-ne--> M+n | x(5x-2y) |
| \(xN^{+5}+\left(5x-2y\right)e->N_x^{+\dfrac{2y}{x}}\) | xn |
Cho sơ đồ phản ứng sau: Fe → FeCl2 → Fe(OH)2 → Fe(OH)3 → Fe2O3 → Fe → FeCl3
Mỗi mũi tên là một phản ứng, hãy cho biết có bao nhiêu phản ứng là phản ứng oxi hoá khử
A. 3
B. 4
C. 5
D. 6
Cho sơ đồ phản ứng sau: Fe → FeCl2 → Fe(OH)2 → Fe(OH)3 → Fe2O3 → Fe → FeCl3
Mỗi mũi tên là một phản ứng, hãy cho biết có bao nhiêu phản ứng là phản ứng oxi hoá khử
A. 3
B. 4
C. 5
D. 6
Đáp án B
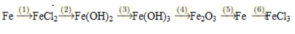
Các phản ứng oxi hóa khử gồm : (1), (3), (5), (6)
Câu 3. Hãy hoàn thành các sơ đồ phản ứng sau và cho biết tỉ lệ số nguyên tử, phân tử giữa các chất trong mỗi phản ứng? 1) Fe2O3 + H2 Fe + H2O 2) Na + H2 O NaOH + H2 3) Fe2O3 + H2SO4 Fe2(SO4)3 + H2O 4) Al + H2SO4 Al2(SO4)3 + H2 5) Cu + O2 CuO 6) Al + O2 Al2O3 7) FeO + HCl FeCl2 + H2O 8) ZnO + HCl ZnCl2 + H2O
1, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\) (1:3:2:3)
2, \(2Na+2H_2O\rightarrow2NaOH+H_2\) (2:2:2:1)
3, \(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\) (1:3:1:3)
4, \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\) (2:3:1:3)
5, \(2Cu+O_2\underrightarrow{t^o}2CuO\) (2:1:2)
6, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\) (4:3:2)
7, \(FeO+2HCl\rightarrow FeCl_2+H_2O\) (1:2:1:1)
8, \(ZnO+2HCl\rightarrow ZnCl_2+H_2O\) (1:2:1:1)
Cho sơ đồ Fe + O2 ---> Fe3O4. Nếu có 4.48 lít khí O2 phản ứng. Hãy tính mFe = ? và mFe3O4 (bằng 2 cách)
Cách 1 :
PTHH : \(3Fe+2O_2\rightarrow Fe_3O_4\)
..............0,3........0,2........0,1..........
\(n_{O_2}=\frac{V}{22,4}=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}m_{Fe}=n.M=16,8\left(g\right)\\m_{Fe_3O_4}=n.M=23,2\left(g\right)\end{matrix}\right.\)
Cách hai :
\(n_{O_2}=\frac{V}{22,4}=0,2\left(mol\right)\)
=> \(m_{O_2}=n.M=6,4\left(g\right)\)
-> \(n_{\left(O\right)}=0,4\left(mol\right)\)
=> \(n_{Fe_3O_4}=\frac{1}{4}n_{\left(O\right)}=0,1\left(mol\right)\)
=> \(m_{Fe_3O_4}=n.M=23,2\left(g\right)\)
- Định luật bảo toàn khối lượng :
\(m_{Fe}+m_{O_2}=m_{Fe_3O_4}\)
=> mFe = 16,8 ( g )