Sục C O 2 vào 200 gam dung dịch C a O H 2 , kết quả thí nghiệm được biểu diễn bằng đồ thị sau :
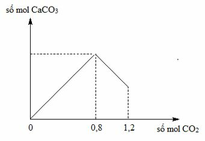
Nồng độ % chất tan trong dung dịch sau phản ứng là
A. 30,45%
B. 35,40%
C. 34,05%
D. 45,03%
Bµi 1. Dẫn CO2 sục vào dung dịch hỗn hợp gồm NaOH và Ba(OH)2. Viết tất cả các phản ứng hóa học có thể xảy ra.
Bài 2. Cho 4,48 lit SO2 (đktc) tác dụng với 200 gam dung dịch NaOH 6%. Tính C% chất tan trong dung dịch thu được.
Bài 3. Cho 9,4 gam K2O vào nước. tính m SO2 cần phản ứng với dung dịch trên để tạo thành:
a. Muối trung hòa.
b. Muối axit.
c. Hỗn hợp muối axit và muối trung hòa theo tỉ lệ số mol là 1 : 2.
Bài 4. Cho 4,48 lit CO2 (đktc) tác dụng với 200 gam dung dịch KOH nồng độ x%, cô cạn dung dịch được 25,7 gam chất rắn. Tính giá trị x.
Bài 5. Cho V lit CO2 (đktc) tác dụng với 200 gam dung dịch NaOH 8%, sau phản ứng, làm bay hơi hết nước của dung dịch thu được 21 gam chất rắn. Tính giá trị V.
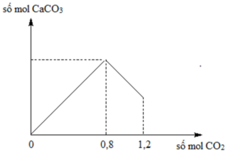
Sục CO2 vào 200 gam dung dịch Ca(OH)2 ta có kết quả theo đồ thị như hình bên. Tính C% của chất tan trong dung dịch sau phản ứng?
A. 30,45%.
B. 34,05%.
C. 35,40%.
D. 45,30%.
Chọn đáp án A
Vì ↓ cực đại = 0,8 mol ⇒ nCa(OH)2 = 0,8 mol và ∑nCO2 = 1,2 mol.
+ Từ đồ ⇒ sau khi cho 1,2 mol CO2 vào dung dịch chứa 0,8 mol Ca(OH)2 ta có:
nCaCO3 = 1,2 – 0,8 = 0,4 mol.
⇒ Bảo toàn canxi ⇒ nCa(HCO3)2 = 0,8 – 0,4 = 0,4 mol.
⇒ mDung dịch sau phản ứng = 1,2×44 + 200 – 0,4×100 = 212,8 gam.
⇒ C%Ca(HCO3)2 = 0 , 4 . 162 212 , 8 ≈ 30,45% ⇒ Chọn A
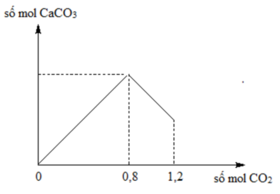
Sục CO2 vào 200 gam dung dịch Ca(OH)2 ta có kết quả theo đồ thị như hình bên. Tính C% của chất tan trong dung dịch sau phản ứng?
A. 30,45%.
B. 34,05%.
C. 35,40%
D. 45,30%.
Đáp án A
Vì ↓ cực đại = 0,8 mol ⇒ nCa(OH)2 = 0,8 mol và ∑nCO2 = 1,2 mol.
+ Từ đồ ⇒ sau khi cho 1,2 mol CO2 vào dung dịch chứa 0,8 mol Ca(OH)2 ta có:
nCaCO3 = 1,2 – 0,8 = 0,4 mol.
⇒ Bảo toàn canxi ⇒ nCa(HCO3)2 = 0,8 – 0,4 = 0,4 mol.
⇒ mDung dịch sau phản ứng = 1,2×44 + 200 – 0,4×100 = 212,8 gam.
⇒ C%Ca(HCO3)2 =  ≈ 30,45%
≈ 30,45%
Sục 3,36 lít hỗn hợp gồm SO2 và CO2 vào 200 ml dung dịch NaOH 1M. Sau đó cô cạn dung dịch tạo ra 17,9 gam muối khan.
a, Tính %V mỗi khí đã dùng
Đốt cháy hoàn toàn một hidrocacbonat A rồi ngưng tụ sản phẩm thu được a gam H2O và V lít CO2 . Sục V lít CO2 vào dung dịch Ca(OH)2 vừa đủ thu được 100g kết tủa. Cho a gam H2O tác dụng với Na dư thu được 11,2 lít H2 (đktc). Xác định công thức phân tử của A. Biết rằng nếu sục 1,12 lít khí A (đktc) vào dung dịch Br2 dư thì thấy khối lượng dung dịch tăng 1,4g
Ta có :
\(\text{nCaCO3=1 nH2=0.5}\)
\(\text{CO2+Ca(OH)2-->CaCO3+H2O}\)
1..................................1..........................(mol)
\(\text{2H2O+2Na-->2NaOH+H2}\)
1..........................0,.5............................(mol)
nCO2=nH2O---> Hidrocacbon có công thức CnH2n
Khi tác dụng với Br2 nCnH2n=0.05
\(\text{CnH2n+Br2-->CnH2nBr2}\)
0,05..........0,05.............................(mol)
m dung dịch tăng là mCnH2n phản ứng
Ta có :
\(\text{14n*0.05=1.4-->n=2}\)
-->A là C2H4 etylen
Sục 6,72 lit khí CO2 vào 700 ml dung dịch Ca(OH)2 aM thu được m gam kết tủa. Nếu sục 8, 96 lit khí CO2 vào 700 ml dung dịch Ca(OH)2 aM cũng thu được m gam kết tủa.(biết các khí đều đo ở đktc) Tìm giá trị của a?
CO2+OH(-) --->HCO3(-)
0,1 -->0,1
CO2+2OH(2-) ---> CO3(2-) +H2O
0,3 -->0,6
-->a=0,5
Bài 2: Sục 11,2 lit khí CO2 vào 200 gam dung dịch NaOH 10% được dung dịch A. Tính nồng độ các chất có trong dung dịch sau phản ứng
\(n_{CO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{NaOH}=\dfrac{200.10\%}{40}=0,5\left(mol\right)\)
Xét \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{0,5}{0,5}=1\) => Tạo muối NaHCO3
PTHH: NaOH + CO2 --> NaHCO3
0,5--------------->0,5
mdd sau pư = 0,5.44 + 200 = 222 (g)
mNaHCO3 = 0,5.84 = 42 (g)
\(C\%=\dfrac{42}{222}.100\%=18,919\%\)
Bài 1:Lượng nước cất cần thêm vào 200 gam dung dịch NaCl 15% để thu được dung dịch NaCl có nồng độ 5% là bao nhiêu ml?
Bài 2:
a)Ở 20 độ C,10 gam nước hòa tantoois đa 20 gam đường.Khối lượng đường cần dùng hòa tan vào 200 gam nước ở 20 độ C để thu được dung dịch bão hòa là bao nhiêu?
b)Biết độ tan cuả NaCl ở 25 độ C là 36,2gam. Khối lượng của NaCl có thể tan trong 500gam nước để tạo thành dung dịch bão hòa là bao nhiêu?
Câu III
1. Cho m gam hỗn hợp X gồm Na2CO3, MgO, a mol Fe3O4 và 2a mol KHCO3 vào 400 gam dung dịch H2SO4 17,15%. Sau khi phản ứng xảy ra hoàn toàn thi được khí CO2 ; dung dịch chứa (m+42,68) gam muôi sunfat trung hòa và 345,44, gam nước. Tìm giá trị của m và a.
2. Cho b gam hỗn hợp oxit sắt gồm FeO, Fe2O3, Fe3O4 tan vừa hết trong dung dịch H2SO4 loãng tạo thành dung dịch Y, cô cạn dung dịch Y, thu được 70,4 gam muối khan. Mặt khác nếu sục khí clo dư vào dung dịch Y rồi cô cạn thì thu được 77,5 gam muối khan. Hãy tính b
Câu 1 :
\(\text{mH2SO4 = mdd H2SO4×C%:100% = 400 × 17,15% :100% = 68,6 (g)}\)
=> mH2O trong dd H2SO4 = 400 – 69,6 = 331,4 (g)
=> nH2SO4 = mH2SO4 : M H2SO4 = 68,6 : 98 = 0,7 (mol)
mH2O sinh ra do pư = 345,44 – m H2O trong dd H2SO4 = 345,44 – 331,4 = 14,04 (g)
\(\text{=> nH2O sinh ra = 14,04 : 18 = 0,78 (mol)}\)
\(\text{m (g) hhX + 400 gam H2SO4 → (m+ 42,68) gam muối sunfat + CO2 + 345,44 gam H2O}\)
Bảo toàn khối lượng ta có:
\(\text{m + 400 = m + 42,68 + mCO2 + 345,44}\)
\(\text{=> mCO2 = 400 – 42,68 – 345,44 = 11,88 (g)}\)
\(\text{=> nCO2 = 11,88 : 44 = 0,27 (mol)}\)
BTNT “H” có: nH(trong KHCO3) + nH (trong H2SO4) = nH(trong H2O)
\(\text{→ 2a + 2×0,7 = 2×0,78}\)
→ 2a = 0,16
→ a = 0,08 (mol)
→ nFe3O4 = 0,08 (mol) và nKHCO3 = 0,16 (mol)
Bảo toàn nguyên tố “C” có: nCO2 = nNa2CO3 + nKHCO3
\(\text{→ 0,27 = nNa2CO3 + 0,16}\)
\(\text{→ nNa2CO3 = 0,27 – 0,16 = 0,11 (mol)}\)
\(\text{Na2CO3 + H2SO4 → Na2SO4 + CO2 + H2O (1)}\)
\(\text{MgO + H2SO4 → MgSO4 + H2O (2)}\)
\(\text{Fe3O4 + 4H2SO4 → Fe2(SO4)3 + FeSO4 + 4H2O (3)}\)
\(\text{KHCO3 + H2SO4 → K2SO4 + CO2 + H2O (4)}\)
Theo các PTHH trên ta có:
Ta có: nH2SO4 = nNa2CO3 + nMgO + 1/4 nFe3O4 + nKHCO3
\(\text{→ 0,7 = 0,11 + nMgO + 1/4 ×0,08 + 0,16}\)
\(\text{→ nMgO = 0,52 (mol)}\)
Vậy hhX gồm: Na2CO3: 0,11 (mol); MgO: 0,52 (mol); Fe3O4: 0,08 (mol) và KHCO3: 0,16 (mol)
\(\text{→ mX = 0,11×106 + 0,52×40 + 0,08×232 + 0,16×100 = 67,02}\)
Câu 2 :
Do Fe3O4 = FeO.Fe2O3 nên ta quy đổi hỗn hợp thành FeO và Fe2O3
Đặt nFeO = a và nFe2O3 = b (mol)
- Khi FeO, Fe2O3 tác dụng với H2SO4:
\(\text{FeO + H2SO4 -> FeSO4 + H2O}\)
x--------------------->x
\(\text{Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O}\)
y-------------------------> y
\(\text{=> m muối = 152x + 400y = 70,4 (1)}\)
- Sục Cl2 dư vào dd Y:
\(\text{6FeSO4 + 3Cl2 -> 2Fe2(SO4)3 + 2FeCl3}\)
------------------------->x/3------------------>x/3
=> Muối chứa:
\(\text{nFe2(SO4)3 = x/3+y (mol)}\)
\(\text{nFeCl3 = x/3 (mol)}\)
=> m muối \(\text{= 400(x/3+y) + 162,5.(x/3) = 77,5 (2)}\)
Giải (1) (2) được x = 0,2 và y = 0,1
=> b = m hỗn hợp\(\text{= 0,2.72 + 0,1.160 = 30,4 gam }\)
Sục khí CO2 vào 200 gam dung dịch Ba(OH)2 17,1% thu được a gam kết tủa và dung dịch X. Cho Ca(OH)2 dư vào dung dịch X thu được b gam kết tủa. Tổng khối lượng kết tủa thu được hai lần là 49,4 gam. Số mol của CO2 là
A. 0,2 mol.
B. 0,494 mol.
C. 0,3 mol.
D. 0,4 mol.
Chọn đáp án C
Quy quá trình thành: CO2 + 0,2 mol Ba(OH)2 + Ca(OH)2 dư → 49,4g ↓
⇒ nCaCO3 = (49,4 - 0,2 × 197) ÷ 100 = 0,1 mol. Bảo toàn nguyên tố Cacbon:
nCO2 = nBaCO3 + nCaCO3 = 0,2 + 0,1 = 0,3 mol ⇒ chọn C.