Trong dãy hợp chất của sắt FeO, Fe 2 O 3 , Fe 3 O 4 , Fe x O y , FeS, Fe S 2 oxi hoá của sắt lần lượt là
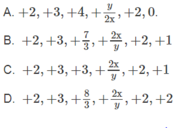
Hợp chất trong đó sắt chiếm 70% khối lượng là hợp chất nào trong số các hợp chất sau ?
a) FeO b) Fe2O3 c) Fe3O4 d) Fe
Hợp chất trong đó sắt chiếm 70% khối lượng là hợp chất nào trong số các hợp chất sau ?
a) FeO b) Fe2O3 c) Fe3O4 d) Fe
Giải
%mO=30%
\(\frac{56x}{56x+72}\)
=>x=3
=>Fe2O3
1 Nếu hàm lượng phần trăm của 1 kim loại trong hợp chất của kim loại với nhóm (CO3) LÀ 40% thì hàm lượng % của kim loại đó trong hợp chất của nó với nhóm (PO4) là bao nhiêu?
2 Có các hợp chất của sắt FeO; Fe2O3; Fe3O4. Nếu hàm lượng của sắt trong hợp chất là 72,41% theo khối lượng thì đó là hợp chất nào?
1. CO3 = 12+ 16.3 = 60g
kim loại đó mkl = 40% = 40g = Ca
PO4 = 31 + 16.4 = 95
% Ca = 40/(95+40).100% = 29,6%
2. % Fe trong fe0 = 56/(56+16) = 77,41%
vay nó là FeO
Khi phân tích một hợp chất gồm 3 nguyên tố Fe, S, O
Người ta thất rằng %Fe = 28%, S = 24%, %O còn lại. Hãy lập công thức hóa học của hợp chất, biết rằng hợp chất có 2 nguyên tử Fe.
2/ Sắt kết hợp với oxi tạo thành 3 hợp chất là FeO, Fe2O3, Fe3O4. Hãy cho biết %O trong hợp chất nào là nhiều nhất.
2) \(\%m_{\dfrac{O}{FeO}}=\dfrac{16}{72}.100\approx22,222\%\\ \%m_{\dfrac{O}{Fe2O3}}=\dfrac{3.16}{160}.100=30\%\\ \%m_{\dfrac{O}{Fe3O4}}=\dfrac{64}{232}.100\approx27,586\%\)
Bài 1:
%mO=48%
M(phân tử)= (2.56)/28%=400(g/mol)
Số nguyên tử S: (24% . 400)/32= 3(nguyên tử)
Số nguyên tử O: (48% . 400)/16= 12(nguyên tử)
=> CTHH: Fe2(SO4)3
Câu 1: Tìm hóa trị của các nguyên tố trong mỗi trường hợp sau:
a) Photpho trong hợp chất P2O5
b) Lưu huỳnh trong hợp chất SO3, FeS2( Sắt hóa trị II )
c) Sắt trong hợp chất FeCl3, FeCl2, FeO , Fe2O3, Fe(OH)3, FeSO4, Fe2(SO4)
a, Gọi x là hóa trị của P.
Ta có: 2x = 2.5
=> x = 5.
Vậy hóa trị của P trong hợp chất này là hóa trị V.
b, SO3
Gọi x là hóa trị của S.
Ta có: x = 2.3
=> x = 6.
Vậy hóa trị của S trong hợp chất này là hóa trị VI.
FeS2
Gọi x là hóa trị của S.
Ta có: 2x = 2.1
=> x = 1.
Vậy hóa trị của S trong hợp chất này là hóa trị I.
c, FeCl3
Gọi x là hóa trị của Fe.
Ta có: x = 3.1
=> x = 3.
Vậy hóa trị của Fe trong hợp chất này là hóa trị III.
FeCl2
Gọi x là hóa trị của Fe.
Ta có: x = 2.1
=> x = 2.
Vậy hóa trị của Fe trong hợp chất này là hóa trị II.
FeO
Gọi x là hóa trị của Fe.
Ta có: x = 2.1
=> x = 2.
Vậy hóa trị của Fe trong hợp chất này là hóa trị II.
Fe2O3
Gọi x là hóa trị của Fe.
Ta có: 2x = 3.2
=> x = 3.
Vậy hóa trị của Fe trong hợp chất này là hóa trị III.
Fe(OH)3
Gọi x là hóa trị của Fe.
Ta có: x = 3.1
=> x = 3.
Vậy hóa trị của Fe trong hợp chất này là hóa trị III.
FeSO4
Gọi x là hóa trị của Fe.
Ta có: x = 2.1
=> x = 2.
Vậy hóa trị của Fe trong hợp chất này là hóa trị II.
Fe2(SO4)3
Gọi x là hóa trị của Fe.
Ta có: 2x = 3.2
=> x = 3.
Vậy hóa trị của Fe trong hợp chất này là hóa trị III.
a/ P có hóa trị V
b/ SO3 => S : VI
FeS2 => S : I
c/ FeCl3 => Fe: III
FeCl2 => Fe: II
FeO => Fe: II
Fe2O3 => Fe: III
Fe(OH)3 ==> Fe: III
FeSO4 => Fe: II
Fe2(SO4)3 => Fe : III
a) O có hóa trị II
P có hóa tri V
b) + SO3
O có hóa trị II
S có hóa trị VI
+ FeS2
S có hóa trị I
Fe có hóa trị II
c) Cl có hóa trị I
O có hóa trị II
H có hóa trị I
+ FeCl3 ⇒ Fe có hóa trị III
+ FeCl2 ⇒ Fe có hóa trị II
+ FeO ⇒ Fe có hóa trị II
+ Fe2O3 ⇒ Fe có hóa trị III
+ Fe(OH)3 ⇒ Fe có hóa trị III
+ FeSO4 ⇒ Fe có hóa trị II
⇒ S có hóa trị VI
+ Fe2(SO4)3 ⇒ Fe có hóa trị III
⇒ S có hóa trị VI
Mấy ad chuyên hóa giải dùm :))
1, Khi phân tích 1 hợp chất gồm 3 n/tố Fe , S , O
Người ta thất rằng %Fe = 28% , S = 24% , %O còn lại . Hãy lập CTHH của hợp chất , biết rằng hợp chất có 2 n/tử Fe
2, Sắt kết hợp với Oxi tạo thành 3 hợp chất là FeO , Fe2O3 , Fe3O4 . Hãy cho biết %O trong hợp chất nào là nhiều nhất
Giải được hậu tạ 9 sì pe ((:
1.Gọi CTC: FexSyOz
Theo đề : x = 2; 2*56/(2*56+32y+16z)=0,28
=> Mh/c= 400
=> y= 400. 24%/32=3
=> z=400.48%/16= 12
=> Fe2(SO4)3
2.
FeO : %mO = 16/(56+16)= 2/9
Fe2O3 : %mO= 16*3/(56*2+16*3)=3/10
Fe3O4: %mO=16*4/(56*3+16*4)=8/29
1. Gọi công thức hóa học của hợp chất là : FExSyOz. Theo đề bài ra ta có :
Khối lượng của Fe có trong hợp chất là : 56 . 2 = 112 (g)
Khối lượng của hợp chất đó là :\(\frac{112.100\%}{28\%}=400\)(g)
Khối lượng của nguyên tử S có trong hợp chất là :\(\frac{400.24\%}{100\%}=96\)(g)
Số nguyên tử S có trong hợp chất là : 96 :32 = 3 (nguyên tử)
Số nguyên tử O có trong hợp chất là : (400 - 112 - 96) : 16 = 12 (nguyên tử)
=> Công thức hóa học của hợp chất là : Fe2(SO4)3
1) Gọi CTHH của hợp chất là \(Fe_x,S_y,O_z\)
x : y : z = \(2:\frac{24}{32}:\frac{100-28-24}{16}\)(vì Fe có 2 nguyên tử)
x : y : z = 2 : 1 : 3
CTHH của hợp chất là \(Fe_2SO_3\)
2) %mO (trong FeO) = \(\frac{16\cdot100}{16+56}=22,22\%\)
%mO (trong \(Fe_2O_3\)) =\(\frac{16\cdot3\cdot100}{56\cdot2+16\cdot3}=30\%\)
%mO (trong \(Fe_3O_4\)) = \(\frac{16\cdot4\cdot100}{56\cdot3+16\cdot4}=27,59\%\)
Vậy \(Fe_2O_3\)có %O nhiều nhất
Cho các hợp chất của sắt: Fe2O3, FeS2, FeSO4, Fe3O4, FeO, Fe(SO4)3. Hãy cho biết trong các hợp chất trên thì:
a) Hợp chất nào có hàm lượng sắt cao nhất ?
b) Hợp chất nào có hàm lượng sắt thấp nhất
CuO
\(\%_{Cu}=\frac{64}{64+16}.100\%=80\%\)
CuS2
\(\%_{Cu}=\frac{64}{64+32.2}.100\%=50\%\)
CuS
\(\%_{Cu}=\frac{64}{64+32}.100\%=66,67\%\)
CuSO3
\(\%_{Cu}=\frac{64}{64+32+16.3}.100\%=44,44\%\)
CuSO4
\(\%_{Cu}=\frac{64}{64+32+16.4}.100\%=40\%\)
Cu2O
\(\%_{Cu}=\frac{64}{64.2+16}.100\%=88,89\%\)
\(\Rightarrow\) Cu2O nhiều đồng nhất
Vậy CuSO4 ít đồng
Tính hóa trị của các nguyên tố
a, Sắt trong các hợp chất FeO ; Fe2O3
b, Lưu huỳnh trong các hợp chất SO2 , SO3
c, Clo trong các hợp chất HCl và Cl2O
d, Crom trong hợp chất CrO
a, Gọi x là hóa trị của sắt trong FeO , ta có :
1 × x = 1 × II
=> x = II
Tương tự ta có hóa trị của sắt trong hợp chất Fe2O3
2 × x = 3 × II
=> x = III
b, Gọi x là hóa trị của Lưu Huỳnh trong hợp chất SO2 , ta có :
1 × x = 2 × II
=> x = IV
Tương tự ta có hóa trị của lưu huỳnh trong hợp chất SO3 :
1 × x = 3 × II
=> x = VI
c, Gọi x là hóa trị của Clo trong hợp chất HCl , ta có :
1 × x = 1 × I
=> x = I
Tương tự ta có hóa trị của Clo trong hợp chất Cl2O :
2 × x = 1 × II
=> x = I
d, Gọi x là hóa trị của Cr trong hợp chất CrO , ta có :
1 × x = 1 × II
=> x = II
a, + FeO
XĐ: x=1,y=1
a=?,b=II
theo QT hóa trị ta có:
a.a=y.b=>1.a=1.II
=>a=II
Vậy sắt trong ct FeO có hóa trị là II
+Fe2O3
XĐ: x=2,y=3
a=?,b=II
theo quy tắc hóa trị ta có:
x.a=b.y=>2.a=3.II
=>a=3
vậy sắt trong ct Fe2O3 có hóa trị là III
B, +SO2
XĐ:x=1,y=2
a=?,b=II
theo quy tắc hóa trị ta có:
x.a=y.b=>1.a=2.II=>a=4
vậy lưu huỳnh trong ct SO2 có hóa trị là IV
+ SO3
XĐ: x=1,y=3
a=?,b=II
theo qt hóa trị ta có:
x.a=y.b=>1.a=3.II=>a=6
vậy lưu huỳnh trong công thức SO3 có hóa trị là VI
c, +HCl
XĐ:x=1, y=1
a=I,b=?
theo qt hóa trị ta có:
x.a=y.b=>1.I=1.b
=>b=I
vậy Cl trong công thức HCl có hóa trị là I
+Cl2O
XĐ: x=2,y=1
a=?,b=II
theo qt hóa trị ta có:
x.a=y.b=>2.a=1.II
=>a=1
vậy Cl trong ct Cl2O có hóa trị là I
Trình bày phương pháp giải nhanh để sắp xếp thứ tự tăng dần phần trăm khối lượng của sắt trong các hợp chất sau :
FeS, Fe2O3, FeO, FeS2, Fe3O4, FeSO4, Fe2(SO4)3
\(\%M_{Fe}=\dfrac{M_{Fe}}{M_{hh}}.100\%\)
\(Fe_2(SO_4)_3, FeSO_4, FeS_2, FeS, Fe_2O_3, Fe_3O_4, FeO\)
Hãy thực hiện các yêu cầu sau :
a) Tìm hoá trị của Sắt ( Fe ) trong hợp chất FeO
b) Tìm hoá trị của Lưu huỳnh ( S ) trong hợp chất SO3
a. Gọi hóa trị của Fe là a ta có 1 x a = 1 x II ( Theo quy tắc hóa trị )
Suy ra a = II hay hóa trị của Fe trong hợp chất là II
b. Gọi hóa trị của S là a ta có 1 x a = 3 x II ( Theo quy tắc hóa trị )
Suy ra a= IV hay hóa trị của S trong hợp chất là IV
a/ Đặt hóa trị của Fe trong hợp chất FeO là a
Vì O trong mọi hợp chất đều có hóa trị là 2
Theo qui tắc hóa trị, ta có:
\(1\times a=2\times1\Rightarrow a=2\)
Vậy hóa trị của Fe trong hợp chất FeO là 2
b/ Đặt hóa trị của S trong hợp chất SO3 là x
Vì O trong mọi hợp chất đều có hóa trị là 2
Theo qui tắc hóa trị ta có:
\(1\times x=2\times3\)
=> x = 6
Vậy hóa trị của S trong hợp chất SO3 là 6
Đặt a là hoá trị của Fe.
Ta có công thức Fe^aO^II
Áp dụng quy tắc hoá trị ax = by ta có: a.1= II.1
=> a=II.1/1=II.
Hoá trị của Fe là II
Tương tự của S sẽ là VI