Nêu hiện tượng, viết phương trình háo học khi tiến hành thí nghiệm rắc nhẹ bột nhôm lên ngọn lửa đèn cồn. Cho biết vai trò của nhôm trong phản ứng đó.

Những câu hỏi liên quan
Rắc bột nhôm mịn lên ngọn lửa đèn cồn trong không khí. Quan sát hiện tượng, ta thấy bột nhôm cháy trong không khí với A. ngọn lửa màu lam nhạt, tỏa nhiều nhiệt. B. ngọn lửa sáng chói, tỏa nhiều nhiệt. C. ngọn lửa màu nâu đỏ, tỏa nhiều nhiệt. D. ngoạt lửa xanh mờ, tỏa nhiều nhiệt.
Đọc tiếp
Rắc bột nhôm mịn lên ngọn lửa đèn cồn trong không khí.
Quan sát hiện tượng, ta thấy bột nhôm cháy trong không khí với
A. ngọn lửa màu lam nhạt, tỏa nhiều nhiệt.
B. ngọn lửa sáng chói, tỏa nhiều nhiệt.
C. ngọn lửa màu nâu đỏ, tỏa nhiều nhiệt.
D. ngoạt lửa xanh mờ, tỏa nhiều nhiệt.
Đáp án B
Khi đốt, bột nhôm cháy sáng trong không khí với ngọn lửa sáng chói, tỏa nhiều nhiệt, tạo ra Al2O3 (chất rắn, màu trắng).
4Al + 3O2 → t 0 2Al2O3.
Đúng 1
Bình luận (0)
Các thao tác tiến hành thí nghiệm sau: 1. Đốt cháy natri trên ngọn lửa đèn cồn. 2. Cho một lượng natri bằng hạt ngo vào muỗng lấy hóa chất. 3. Mở nắp lọ đựng oxi. 4. Đưa nhanh muỗng có Na đang cháy vào lọ đựng khí oxi có sẵn trong một lớp cát. 5. Quan sát hiện tượng, viết phương trình phản ứng và xác định vai trò của chất tham gia phản ứng. Thứ tự hợp lí (từ trái sang phải) các thao tác khi tiến hành đốt cháy natri trong lọ chứa khí oxi là: A. 1, 2, 3, 4, 5, 6 B. 2, 1, 3, 4, 6, 5 C. 2, 1, 3, 4...
Đọc tiếp
Các thao tác tiến hành thí nghiệm sau:
1. Đốt cháy natri trên ngọn lửa đèn cồn.
2. Cho một lượng natri bằng hạt ngo vào muỗng lấy hóa chất.
3. Mở nắp lọ đựng oxi.
4. Đưa nhanh muỗng có Na đang cháy vào lọ đựng khí oxi có sẵn trong một lớp cát.
5. Quan sát hiện tượng, viết phương trình phản ứng và xác định vai trò của chất tham gia phản ứng.
Thứ tự hợp lí (từ trái sang phải) các thao tác khi tiến hành đốt cháy natri trong lọ chứa khí oxi là:
A. 1, 2, 3, 4, 5, 6
B. 2, 1, 3, 4, 6, 5
C. 2, 1, 3, 4, 5, 6
D. 3, 1, 2, 4, 5, 6
Các thao tác tiến hành thí nghiệm sau: 1. Đốt cháy natri trên ngọn lửa đèn cồn. 2. Cho một lượng natri bằng hạt ngo vào muỗng lấy hóa chất. 3. Mở nắp lọ đựng oxi. 4. Đưa nhanh muỗng có Na đang cháy vào lọ đựng khí oxi có sẵn trong một lớp cát. 6. Quan sát hiện tượng, viết phương trình phản ứng và xác định vai trò của chất tham gia phản ứng. Thứ tự hợp lí (từ trái sang phải) các thao tác khi tiến hành đốt cháy natri trong lọ chứa khí oxi là: A. 1, 2, 3, 4, 5, 6. B. 2, 1, 3, 4, 6, 5. C. 2, 1, 3,...
Đọc tiếp
Các thao tác tiến hành thí nghiệm sau:
1. Đốt cháy natri trên ngọn lửa đèn cồn.
2. Cho một lượng natri bằng hạt ngo vào muỗng lấy hóa chất.
3. Mở nắp lọ đựng oxi.
4. Đưa nhanh muỗng có Na đang cháy vào lọ đựng khí oxi có sẵn trong một lớp cát.
6. Quan sát hiện tượng, viết phương trình phản ứng và xác định vai trò của chất tham gia phản ứng.
Thứ tự hợp lí (từ trái sang phải) các thao tác khi tiến hành đốt cháy natri trong lọ chứa khí oxi là:
A. 1, 2, 3, 4, 5, 6.
B. 2, 1, 3, 4, 6, 5.
C. 2, 1, 3, 4, 5, 6.
D. 3, 1, 2, 4, 5, 6.
Rắc nhẹ bột nhôm Al trên ngọn lửa đèn cồn. Hiện tượng gì xảy ra? Hãy viết phương trình hóa học của phản ứng trên.
Hiện tương : Bột nhôm cháy sáng..Xuất hiện bột màu trắng (Al2O3)
4Al+3O2--->2Al2O3
Đúng 0
Bình luận (0)
Hiện tượng : Cháy sáng hiện bột trắng
PTHH. 4Al+ 3O2---> 2Al2O3
Đúng 0
Bình luận (0)
Cho hình vẽ điều chế oxi trong phòng thí nghiệm: – Viết phương trình hóa học của phản ứng. – Vì sao có thể thu khí oxi bằng phương pháp đẩy nước? – Vì sao miệng ống nghiệm đựng KMnO4 lắp hơi nghiêng xuống? – Nêu vai trò của bông khô? – Khi dừng thí nghiệm nên tắt đèn cồn trước hay tháo ống dẫn khí ra trước? Tại sao?
Đọc tiếp
Cho hình vẽ điều chế oxi trong phòng thí nghiệm:
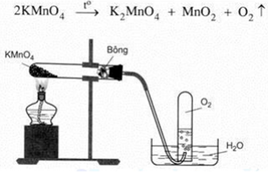
– Viết phương trình hóa học của phản ứng.
– Vì sao có thể thu khí oxi bằng phương pháp đẩy nước?
– Vì sao miệng ống nghiệm đựng KMnO4 lắp hơi nghiêng xuống?
– Nêu vai trò của bông khô?
– Khi dừng thí nghiệm nên tắt đèn cồn trước hay tháo ống dẫn khí ra trước? Tại sao?
– Dùng phương pháp đẩy nước là hợp lí vì oxi ít tan trong nước và oxi thu được có độ tinh khiết cao.
– Oxi nặng hơn không khí, khi đốt nóng KMnO4 thì áp suất tại đó cao hơn nên
– Oxi sinh ra sẽ di chuyển xuống phía dưới ống nơi áp suất thấp hơn và dễ dàng thoát ra ống dẫn khí. – Bông khô có vai trò hút ẩm.
– Khi dừng thí nghiệm nên tắt đèn cồn trước sau đó mới tháo ống dẫn khí.
Đúng 0
Bình luận (0)
đốt nóng 7,44 gam Photpho đỏ trên ngọn lửa đèn cồn rồi đưa nhanh vào lọ thủy tinh chứa 8,0 gam khí Oxi đến khi phản ứng hoàn toàn thì thu được chất rắn X
a, Nêu hiện tượng quan sát được khi mẩu photpho cháy
b, viết phương trình hóa học của phản ứng và tính khối lượng chất rắn X thu được biết Photpho cháy chỉ tạo một sản phẩm là điphotpho pentaoxit
a) P cháy sáng , có khí trắng bám bình
4P+5O2-to>2P2O5
0,2----0,25------0,1 mol
n P=\(\dfrac{7,44}{31}\)=0,24 mol
n O2=\(\dfrac{8}{32}\)=0,25 mol
P dư :
=>m cr=0,1.142+0,04.31=15,44g
Đúng 2
Bình luận (0)
a, Phản ứng sáng chói, P cháy trong O2 tạo ra chất rắn màu trắng dạng bột là P2O5
\(b,n_P=\dfrac{7,44}{31}=0,24\left(mol\right)\\ n_{O_2}=\dfrac{8}{32}=0,25\left(mol\right)\\ PTHH:4P+5O_2\underrightarrow{t^o}2P_2O_5\\ LTL:\dfrac{0,24}{4}>\dfrac{0,25}{5}\Rightarrow P.dư\\ Theo.pt:n_{P_2O_5}=\dfrac{2}{5}n_{O_2}=\dfrac{2}{5}.0,25=0,1\left(mol\right)\\ m_{P_2O_5}=0,1.142=14,2\left(g\right)\\ Theo.pt:n_{P\left(pư\right)}=\dfrac{4}{5}n_{O_2}=\dfrac{4}{5}.0,25=0,2\left(mol\right)\\ m_{P\left(dư\right)}=\left(0,24-0,2\right).31=1,24\left(g\right)\\ m_X=1,24+14,2=15,44\left(g\right)\)
Đúng 1
Bình luận (0)
Hãy cho biết hiện tượng xảy ra khi nhúng một viên kẽm vào:
a, Nhúng viên kẽm vào dd HCl
b, Rắc bột nhôm trên ngọn lửa đèn cồn
c, Cho mẩu Natri vào nước đựng nước cất có pha thêm dd phenolphtalein
a, Chất rắn màu xám sẫm Kẽm (Zn) tan dần và xuất hiện bọt khí do khí Hidro (H2) tạo thành.
b, Cháy sáng trong không khí với ngọn lửa sáng chói, tỏa nhiều nhiệt, tạo ra Al2O3 .
c, Mẫu Na chuyển động nhanh trên mặt nước , tan dần cho đến hết, có khí H2 bay ra, phản ứng toả nhiều nhiệt đồng thời dung dịch chuyển sang màu hồng .
Đúng 1
Bình luận (0)
a) Hiện tượng :
- Viên kẽm tan dần trong dd axit
- Xuất hiện bọt khí không màu thoát ra
b) Hiện tượng : Có chất rắn màu trắng xuất hiện
c) Hiện tượng :
+ Mẩu Natri tan dần
+ Xuất hiện bọt khí không màu thoát ra
+ Dung dịch trong suốt chuyển dần sang màu đỏ
Đúng 0
Bình luận (0)
Tiến hành Thí nghiệm 1 theo hướng dẫn. Nêu hiện tượng xảy ra. Giải thích và viết phương trình hoá học của phản ứng.

Tham khảo:
- Khi nhỏ vài giọt dung dịch acetic acid lên mẩu giấy quỳ tím, mẩu quỳ tím hóa đỏ vì acetic acid có tính acid.
- Khi cho vào ống nghiệm thứ nhất chứa dung dịch acetic acid vài mẩu magnesium, mẩu magnesium tan và xuất hiện bọt khí.
→ Giải thích: Acetic acid phản ứng với magnesium, làm magnesium tan và tạo khí hydrogen.
2CH3COOH + Mg → 2(CH3COO)2Mg + H2↑
- Khi cho vào ống nghiệm thứ hai chứa acetic acid 1 thìa sodium carbonate, sodium carbonate tan và xuất hiện bọt khí.
→ Giải thích: Acetic acid phản ứng với sodium carbonate, sinh ra khí carbon dioxide.
2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2↑
Đúng 0
Bình luận (0)
Nhỏ chậm nước vào nhôm cacbua
Mô tả hiện tượng và viết các phương trình hóa học của các phản ứng để minh họa cho thí nghiệm
Hiện tượng thí nghiệm: Al4C3 tan dần, có hiện tượng sủi bọt khí, xuất hiện kết tủa keo trắng.
Al4C3 + 12H2O → 4Al(OH)3 ↓ + 3CH4 ↑
Đúng 0
Bình luận (0)




















