Đốt cháy hoàn toàn 4,48 l hỗn hợp gồm CH4 và C2H4 cần vừa đủ 5,6 l không khí có chứa 1/5 oxi
a) viết PTHH
b) xác định số mol mỗi chất trong hỗn hợp
c) Xác định thể tích của CO2
đốt cháy hoàn toàn 5,6 g hỗn hợp a gồm s và c (trong a, số mol của s gấp đôi số mol của c) trong không khí, sau phản ứng thu được hỗn hợp khí b. các thể tích khí đo ở đktc a) viết PTHH 2)thể tchs không khí tối thiểu cần đốt để đốt cháy hỗn hợp A, biết oxi chiếm 20% thể tích không c)tỉ khối b và ch4 khí
ĐỐT cháy hoàn toàn 5,6 lít hỗn hợp khí gồm CH4 và C2H4 phải dùng hết 14 lít khí ôxi thì vừa đủ. a)tính khối lượng của các chất khí trong hỗn hợp. b)tính thể tích khí CO2 sinh ra
\(Đặt:n_{CH_4}=a\left(mol\right);n_{C_2H_4}=b\left(mol\right)\left(a,b>0\right)\\ PTHH:CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\\ \Rightarrow\left\{{}\begin{matrix}a+b=0,25\\2a+3b=0,625\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,125\\b=0,125\end{matrix}\right.\\ a,m_{hh}=m_{CH_4}+m_{C_2H_4}=16.0,125+28.0,125=5,5\left(g\right)\\ b,V_{CO_2\left(đktc\right)}=22,4.\left(a+2b\right)=8,4\left(l\right)\)
Câu 4: Đốt cháy một hỗn hợp gồm CH4 và C2H2 có thể tích là 33,6 lít (đktc) thu được 56 lít khí CO2 (đktc).
a. Xác định thành phần % về thể tích các khí trong hỗn hợp?
b. Tính khối lượng của oxi cần để đốt cháy hoàn toàn hỗn hợp khí trên?
a, \(CH_4+2O_2\underrightarrow{t^o}CO_2+H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\left(1\right)\)
Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{56}{22,4}=2,5\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,5\left(mol\right)\\n_{C_2H_2}=1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,5.22,4}{33,6}.100\%\approx33,33\%\\\%V_{C_2H_2}\approx66,67\%\end{matrix}\right.\)
b, Theo PT: \(n_{O_2}=2n_{CH_4}+\dfrac{5}{2}n_{C_2H_2}=3,5\left(mol\right)\Rightarrow m_{O_2}=3,5.32=112\left(g\right)\)
Để đốt cháy hoàn toàn 4,48 lít hỗn hợp khí X gồm CH4 và C2H4 cần dùng vừa đủ 11,2 lít khí oxi, sau phản ứng thu được sản phẩm gồm khí cacbon đioxit và hơi nước.
a) Viết các phương trình phản ứng xảy ra.
b) Tính % thể tích mỗi khí trong hỗn hợp X. Biết các thể tích khí đo ở đktc.
Để đốt cháy 5,6 lít khí etilen cần phải dùng:
a) Bao nhiêu lít oxi?
b) Bao nhiêu lít không khí chứa 1/5 thể tích oxi? Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Hỗn hợp A gồm CH4 và C2H4. Đốt cháy hoàn toàn 3,36 lít hỗn hợp A (đktc) thì thu được 8,8g khí cacbonic. Hãy tính thành phần % thể tích của mỗi khí trong hỗn hợp.
Câu 1:
\(a,PTHH:C_2H_4+5O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(Theo.PTHH:n_{O_2}=5.n_{C_2H_4}=5.0,25=1,25\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=1,25.22,4=28\left(l\right)\)
\(b,\Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2\left(đktc\right)}=5.28=140\left(l\right)\)
B1:
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
Vì số mol tỉ lệ thuận với thể tích, đồng thời nhìn PTHH, ta sẽ được:
\(a,V_{O_2\left(đktc\right)}=3.V_{C_2H_4\left(đktc\right)}=3.5,6=16,8\left(l\right)\)
\(b,V_{kk}=5.V_{O_2\left(đktc\right)}=16,8.5=84\left(l\right)\)
B2:
Đặt số mol metan, etylen lần lượt là a,b (mol) (a,b>0)
\(n_{hh}=n_{CH_4}+n_{C_2H_4}=a+b=\dfrac{3,36}{22,4}=0,15\left(1\right)\)
PTHH: CH4 +2 O2 -to-> CO2 +2 H2O
C2H4 +3 O2 -to-> 2CO2 + 2H2O
\(n_{CO_2\left(tổng\right)}=a+2b=\dfrac{8,8}{44}=0,2\left(mol\right)\left(2\right)\)
(1), (2) =>a=0,1; b=0,05
Số mol tỉ lệ tương ứng với thể tích. Nên:
\(\%V_{CH_4}=\%n_{CH_4}=\dfrac{0,1}{0,15}.100\approx66,667\%\\ \Rightarrow\%V_{C_2H_4}\approx33,333\%\)
\(Đặt:n_{CH_4}=a\left(mol\right),n_{C_2H_4}=b\left(mol\right)\)
\(\Rightarrow a+b=0.15\left(1\right)\)
\(n_{CO_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{t^0}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^0}2CO_2+2H_2O\)
\(\Rightarrow a+2b=0.2\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.05\)
Vì : tỉ lệ thể tích tương ứng với tỉ lệ số mol :
\(\%n_{CH_4}=\dfrac{0.1}{0.15}\cdot100\%=66.67\%\)
\(\%n_{C_2H_4}=100-66.67=33.33\%\)
Chúc em học tốt !!
Đặt \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\)
\(\Sigma n_{hhkA}=\dfrac{3,36}{22,4}=0,15\\ \rightarrow x+y=0,15\left(1\right)\)
\(PTHH:CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
(mol)........x....->...2x.......x..............2x
\(PTHH:C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
(mol)........y......->...3y...........2y........2y
\(\Sigma n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ \rightarrow x+2y=0,2\)
Giải hpt (1) (2) ta được x=0,1 ; y=0,05
\(\%V_{CH_4}=\dfrac{0,1.22,4}{3,36}.100\%=66,67\%\\ \%V_{C_2H_4}=100\%-66,67\%=33,33\%\)
Gọi số mol của metan(CH4) là x, số mol của tean(C2H6) là y
CH4+O2−→CO2
C2H6+O2−→2CO2
nA = x+ y= 3,36\22,4=0,150 mol (1)
nCO2 = x + 2y=4,4822,4= 0,20 mol
Từ (1) và (2) => x = 0,1mol; y=0,05mol
⇒ %VCH4 =0,1\0,15.100%= 66,7% và %VC2H6
Đốt cháy hoàn toàn cacbon bằng một lượng khí oxi dư, người ta thu được hỗn hợp khí gồm có khí cacbonic C O 2 và khí oxi O 2 dư.
Hãy xác định phần trăm theo khối lượng và thành phần phần trăm theo thể tích của khí oxi trong mỗi hỗn hợp sau: 3 mol khí cacbonic và 5 mol khí oxi.
Khối lượng của các khí:
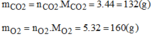
Thành phần phần trăm theo khối lượng:
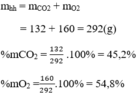
Thành phần phần trăm theo thể tích:
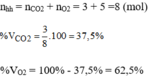
Hỗn hợp khí A chứa hiđro, một ankan và một anken. Đốt cháy hoàn toàn 100 ml A, thu được 210 ml khí C O 2 . Nếu đun nóng nhẹ 100 ml A có mặt chất xúc tác Ni thì còn lại 70 ml một chất khí duy nhất. Các thể tích khí đều đo ở cùng một điều kiện.
1. Xác định công thức phân tử và phần trăm thể tích của từng chất trong hỗn hợp A.
2. Tính thể tích oxi vừa đủ để đốt cháy hoàn toàn 100 ml A.
1. Khi đun nóng A có mặt chất xúc tác Ni, chỉ còn lại 1 chất khí duy nhất. Vậy ankan và anken trong A có cùng số nguyên tử cacbon.
Giả sử trong 100 ml A có x mol C n H 2 n + 2 ; y mol C n H 2 n và z mol H 2 .
x + y + z = 100 (1)
Khi đốt cháy hoàn toàn 100 ml A :
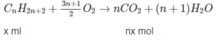
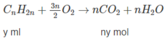
2 H 2 + O 2 → 2 H 2 O
Thể tích C O 2 : n(x + y) = 210 (2)
Khi đun nóng A có mặt chất xúc tác Ni:
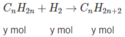
x + y = 70 (3)
y = z (4)
Giải hộ phương trình, tìm được n = 3; x = 40 ; y = z = 30.
Thành phần thể tích của hỗn hợp A là : C 3 H 8 : 40% ; C 3 H 6 : 30%; H 2 : 30%
2. Thể tích O 2 là 350 ml.
Bài 1. Đốt cháy hoàn toàn 13,44 lít (đktc) hỗn hợp gồm C2H2 và C2H4 thu được 18 gam nước. Xác định thành phần % thể tích của mỗi chất khí trong hỗn hợp?
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
x x
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
y 2y
Gọi x là số mol của C2H2 (x,y>0)
y là số mol của C2H4
Ta có : \(22,4x+22,4y=13,44\)
\(n_{H_2O}=\dfrac{18}{18}=1\left(mol\right)\)
\(n_{H_2O}=2x+y=1\) ( Theo PTHH )
Ta có hệ PT :
\(\left\{{}\begin{matrix}22,4x+22,4y=13,44\\x+2y=1\end{matrix}\right.\)
Giải hệ PT , ta có :
x = 0,2
y = 0,4
\(V_{C_2H_2}=0,2.22,4=4,48\left(l\right)\)
\(\%V_{C_2H_2}=\dfrac{4,48}{13,44}.100\%\approx33,33\%\)
\(\%V_{C_2H_4}=\dfrac{0,4.22,4}{13,44}.100\%\approx66,67\%\)