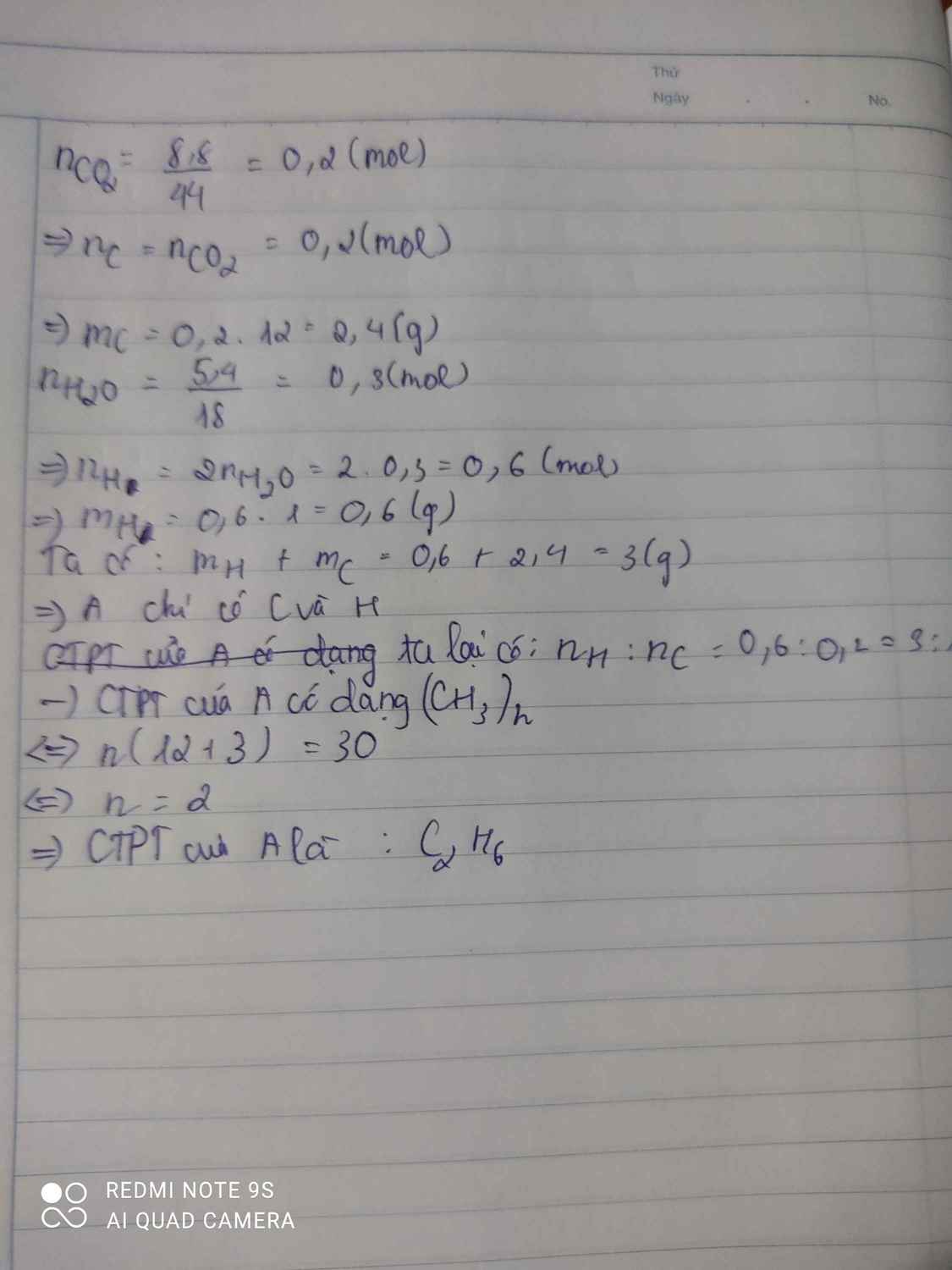Đốt cháy 0,6 g chất hữu cơ A thì thu được 0,88 gam CO2 và 0,36 gam H2O biết khối lượng mol của A = 6 g/mol Tìm ctpt của hợp chất sau

Những câu hỏi liên quan
1. Đốt cháy hoàn toàn 0,58 gam một hyđrocacbon A được 1,76 gam CO2 và 0,9 gam H2O. Biết A có khối lượng riêng DA ≈2,59 gam/lít. Tìm CTPT A.
2. Đốt cháy hoàn toàn 4,6 gam chất hữu có A thu được 4,48 lít CO2 (đktc) và 5,4 gam H2O. dA/kk = 1,58. Xác định CTPT của A?
3. Tìm CTPT của hợp chất sau : Đốt cháy 0,6 g chất hưũ cơ có A thì thu được 0,88 g CO2 và 0.36 g H2O và kl mol của A = 60 g/mol.
1) \(n_{CO2}=\frac{1,76}{44}=0,04\left(mol\right)\)
\(=>n_C=0,4\left(mol\right)\Rightarrow m_C=0,4.12=0,48\left(g\right)\)
\(n_{H2O}=\frac{0,9}{18}=0,05\left(mol\right)\)
\(\Rightarrow n_H=2n_{H2O}=0,1\left(mol\right)\Rightarrow m_H=0,1\left(g\right)\)
\(m_H+m_C\left(0,58\right)=m_A\Rightarrow\) A gồm 2 nguyên tố C,H
\(n_C:n_H=0,04:0,1=2:5\)
\(M_A=2,59.22,4=58\)
=>CTHH:C4H10
Bài 2
\(n_{CO2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_C=n_{CO2}=0,2\left(mol\right)\Rightarrow m_C=0,2.12=2,4\left(g\right)\)
\(n_{H2O}=\frac{5,4}{18}=0,3\left(mol\right)\)
\(\Rightarrow n_H=2n_{H2O}=0,6\left(mol\right)=>m_H=0,6\left(g\right)\)
\(m_H+m_C\left(3\right)< m_A\)
=>A gồm 3 nguyên tố C,H,O
\(m_O=4,6-3=1,6\left(g\right)=>n_O=\frac{1,6}{16}=0,1\left(MOL\right)\)
\(n_C:n_H:n_O=0,2:0,6:0,1=2:6:1\)
\(PTK:1,58.29=46\)
=>CTPT:C2H6O
3. Tìm CTPT của hợp chất sau : Đốt cháy 0,6 g chất hưũ cơ có A thì thu được 0,88 g CO2 và 0.36 g H2O và kl mol của A = 60 g/mol.
\(n_{CO2}=\frac{0,88}{44}=0,02\left(mol\right)\)
\(n_C=n_{CO2}=0,02\left(mol\right)=>m_C=0,02.12=0,24\left(g\right)\)
\(n_{H2O}=\frac{0,36}{18}=0,02\left(mol\right)\)
\(n_H=2n_{H2O}=0,04\left(mol\right)=>m_H=0,04\left(g\right)\)
\(m_C+m_H\left(0,28\right)< 0,6\)
=>A gồm 3 nguyên tố C,H,O
\(m_O=0,6-0,28=0,32\Rightarrow n_O=\frac{0,32}{32}=0,02\left(mol\right)\)
\(n_C:n_H:n_O=0,02:0,04:0,02=1:2:1\)
PTK:60
=>CTPT:C2H4O2
Mà DA = 2,59 g/l ⇒ MA = 2,59.22,4 = 58g
n= MA/ M C2H5 = 58/29 =2
Vậy CTPT của A là C4H10.
Bài 2
nCO2 = 4,48/22,4 = 0,1 mol ⇒ nC = 0,2 mol mC = 2,4 g
nH2O = 5,4/18 = 0,3 mol ⇒ nH = 0,3.2 = 0,6 mol mH = 0,6g
⇒ mO =4,6 - 2,4 - 0,6 = 1,6g ⇒ nO/A = 1,6/16 = 0,1 mol
Vậy A gồm C, H và O.
Gọi CTTQ của A là CxHyOz, ta có:
Vậy CTĐGN của A là (C2H6O)n.
dA/kk = 1,58 ⇒ MA = 1,58.29 = 46g
⇒ n = 1
Vậy công thức phân tử của A là C2H6O
Đốt cháy 3 gam hợp chất hữu cơ B thu được 8,8 gam CO2 và 5,4 gam H2O . Biết phân tử khối của B là 30 g / mol . Tìm CTPT của B
Đốt cháy 3 gam hợp chất hữu cơ B thu được 8,8 gam CO2 và 5,4 gam H2O . Biết phân tử khối của B là 30 g / mol . Tìm CTPT của B
Gọi CTHH của B là \(C_xH_y\)
\(n_B=\dfrac{m_B}{M_B}=\dfrac{3}{30}=0,1mol\)
\(n_C=n_{CO_2}=\dfrac{8,8}{44}=0,2mol\)
\(n_H=2n_{H_2O}=2\cdot\dfrac{5,4}{18}=0,6mol\)
Số nguyên tử cacbon:
\(\overline{C}=\dfrac{n_C}{n_B}=\dfrac{0,2}{0,1}=2\)
Số nguyên tử hidro:
\(\overline{H}=\dfrac{n_H}{n_B}=\dfrac{0,6}{0,1}=6\)
Vậy CTPT của B là \(C_2H_6\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 4,5 gam 1 hợp chất hữu cơ A thu được 6,6 gam CO2 và 2,7 gam H2O. Biết khối lượng mol của phân tử hợp chất hữu cơ là 60g/mol. Xác định CTHH của hợp chất hữu cơ
\(TrongA:n_C=n_{CO_2}=0,15\left(mol\right)\\ n_H=2n_{H_2O}=0,3\left(mol\right)\\ \Rightarrow n_O=\dfrac{4,5-12.0,15-0,3.1}{16}=0,15\left(mol\right)\\ \Rightarrow CTPT:C_xH_yO_z\\ Tacó:x:y:z=0,15:0,3:0,15=1:2:1\\ \Rightarrow CTĐGN:\left(CH_2O\right)_n\\ Tacó:\left(12+2+16\right).n=60\\ \Rightarrow n=2\\ Vậy:CTHHcủaA:C_2H_4O_2\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 4,6 gam hợp chất hữu cơ X thu được 8,8 gam CO2 và 5,4 gam H2O. Biết Mx = 46 (g/mol). Xác định CTPT của X
nC = nCO2 = 8,8/44 = 0,2 (mol)
nH = 2 . nH2O = 2 . 5,4/18 = 0,6 (mol)
nO = (4,6 - 0,2 . 12 - 0,6)/16 = 0,1 (mol)
CTPT: CxHyOz
=> x : y : z = 0,2 : 0,6 : 0,1 = 2 : 6 :1
(C2H6O)n = 46
=> n = 1
=> CTPT: C2H6O
Đúng 3
Bình luận (0)
Câu 3:
a, Đốt cháy 5,6 g chất hữu cơ A, thu được 13,2 g CO2 và 3,6 g H2O. Lập CTPT của A biết tỉ khối của A so với khí nitơ bằng 2.
b, Đốt cháy 3 gam chất hữu cơ A, thu được 8,8 gam CO2 và 5,4 gam H2O. Tìm công thức phân tử của A.Biết tỉ khối hơi của A so với H2 bằng 15
1, Bảo toàn khối lượng: mO2 = mCO2 + mH2O – mA = 11,2 g
=> nO2 = 11,2 /32 = 0,35 mol
nCO2 = 0,3 mol, nH2O = 0,2 mol
Bảo toàn nguyên tố: nC(A) = nC(CO2) = nCO2 =0,3 mol
nH(A) = nH(H2O) = 2nH2O =0,4 mol
nO(A) = nO(H2O) + nO(CO2) – nO(O2)= 0,3.2+0,2 -0,35.2= 0,1 mol
Gọi CTPT của A là CxHyOz
=> x : y : z = nC(A) : nH(A) : nO(A) = 3 : 4 : 1
=> CT tối giản của A là C3H4O => CTPT A có dạng (C3H4O)n
MA = 14.2.2=56 => n = 1
Vậy CTPT của A là C3H4O
Đúng 2
Bình luận (0)
b/ n CO2 = 8,8 : 44 = 0,2 mol => m c = 0,2 x 12 = 2,4( g)
n H2O = 5,4 : 18 = 0,3 mol => mH = 0,3 x 2 = 0,6 (g)
Khối lượng của C và H trong A là : 2,4 + 0,6 = 3 (g)
A chỉ chứa hai nguyên tố là C và H
b/ Công thức của A là CxHy ta có:
x ; y = ( mc ; 12) : ( mH : 1) = ( 2,4 : 12) : ( 0,6 : 1) = 1 : 3
Công thức phân tử của A có dạng ( CH3) n . Vì MA =15.2
=> 15 n =30
Nếu n = 1 không đảm bảo hoá trị C
Nếu n = 2 Công thức phân tử của A là C2H6
Đúng 1
Bình luận (0)
a, nC = 13,2/44 = 0,3 (mol)
nH = 2 . 3,6/18 = 0,4 (mol)
nO = (5,6 - 12 . 0,3 - 0,4)/16 = 0,1 (mol)
CTPT: CxHyOz
=> x : y : z = 0,3 : 0,4 : 0,1 = 3 : 4 : 1
=> (C3H4O) = 28 . 2 = 56 (g/mol)
=> n = 1
CTPT: C3H4O
b, nC = 8,8/44 = 0,2 (mol)
nH = 2 . 5,4/18 = 0,6 (mol)
Xét mC + mH = 0,2 . 12 + 0,6 = 3
=> A chỉ có C và H
CTPT: CxHy
=> x : y = 0,2 : 0,6 = 1 : 3
=> (CH3)n = 15 . 2 = 30 (g/mol)
=> n = 2
CTPT: C2H6
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 6 gam hợp chất hữu cơ A thu được 8,8 gam khí CO2 và 3,6 gam H2O a) hợp chất chứa những nguyên tố hóa học nào ?b)Xác định CTPT của A biết khối lượng mol của A là 60 gamc) Viết CTCT chi tiết và thu gọn của A biết phân tử A có nhóm-COOHd) Viết PTHH của A với dung dịch NaOHGIÚP MÌNH VỚI Ạ MÌNH CẢM ƠN
Đọc tiếp
đốt cháy hoàn toàn 6 gam hợp chất hữu cơ A thu được 8,8 gam khí CO2 và 3,6 gam H2O a) hợp chất chứa những nguyên tố hóa học nào ?
b)Xác định CTPT của A biết khối lượng mol của A là 60 gam
c) Viết CTCT chi tiết và thu gọn của A biết phân tử A có nhóm-COOH
d) Viết PTHH của A với dung dịch NaOH
GIÚP MÌNH VỚI Ạ MÌNH CẢM ƠN
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\) -> \(n_C=0,2\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\) -> \(n_H=0,4\)
\(m_C+m_H=0,2.12+0,4=2,8\left(g\right)\)
-> Trong A có \(m_O=6-2,8=3,2\left(g\right)\)
\(n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là \(C_xH_yO_z\)
\(x:y:z=n_C:n_H:n_O=0,2:0,4:0,2=1:2:1\)
\(\Leftrightarrow\left(CH_2O\right)_n=60.\Rightarrow n=2\)
a. CTPT của A là \(C_2H_4O_2\)
b. CTCT thu gọn:
\(CH_3COOH\)
mình không gõ được CTCT chi tiết (bạn lên mạng xem nhé)
c. \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
Đúng 1
Bình luận (0)
1. Hợp chất hữu cơ (A) gồm 3 nguyên tố. Khi đốt cháy A trong khí oxi chỉ thu được CO2 và H2O. Biết khối lượng mol của A bằng 60 g/mol và nguyên tố oxi chiếm 53,33% theo khối lượng.
Tìm CTPT của A.
Giả sử có 1 mol A => mA = 1.60 = 60(g)
=> \(m_O=\dfrac{53,33.60}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTPT: CxHyO2
=> 12x + y + 32 = 60
=> 12x + y = 28
=> Chọn x = 2; y = 4
=> CTPT: C2H4O2
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 2,1 gam hợp chất hữu cơ A gồm có hai nguyên tố ta thu được 6,6 gam CO2 và 2,7 gam nước. Tìm công thức phân tử của A biết khối lượng mol của A là 28 g/mol
Đọc tiếp
Đốt cháy hoàn toàn 2,1 gam hợp chất hữu cơ A gồm có hai nguyên tố ta thu được 6,6 gam CO2 và 2,7 gam nước. Tìm công thức phân tử của A biết khối lượng mol của A là 28 g/mol
Anh hỗ trợ rồi nha em
Đúng 0
Bình luận (0)