Đốt cháy toàn hoàn 0,1 mol hợp chất hữu cơ (D) cần vừa đủ 14,4 gam oxi thấy sinh ra 13,2 gam CO2 và 7,2 gam nước a) tìm phân tử khối của D b) Xác định công thức phân tử của D

Những câu hỏi liên quan
Bài 2: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ A thu được 13,2 gam khí CO2 và 7,2 gam nước. a) A có những nguyên tố nào? b) Tìm công thức phân tử của A biết khối lượng mol của A bằng 44 gam/mol c) Viết CTCT đầy đủ và thu gọn của A. Giúp với ạ mai e thi r
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 (đktc) và 10,8 gam nước. Biết rằng 7,2 gam X có số mol bằng số mol của 3,2 gam khí oxi.
a) Xác định công thức phân tử của X.
b) Viết tất cả các công thức cấu tạo có thể có của X.
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam hợp chất hữu cơ X thu được 11,2 lít CO2 (đktc) và 10,8 gam nước. Biết rằng 7,2 gam X có số mol bằng số mol của 3,2 gam khí oxi.
a) Xác định công thức phân tử của X.
b) Viết tất cả các công thức cấu tạo có thể có của X.
\(n_C=n_{CO_2}=0,5\left(mol\right);n_H=2.n_{H_2O}=2.\dfrac{10,8}{18}=1,2\left(mol\right)\\ m_C+m_H=0,5.12+1,2.1=7,7,2\\ \Rightarrow X.ko.có.oxi\left(O\right)\\ \Rightarrow CTTQ:C_xH_y\left(x,y:nguyên,dương\right)\\ x:y=n_C:n_H=0,5:1,2=5:12\\a, \Rightarrow x=5;y=12\Rightarrow CTPT.X:C_5H_{12}\\ b,CH_3-CH_2-CH_2-CH_2-CH_3\\ CH_3-CH\left(CH_3\right)-CH_2-CH_3\\ CH_3-C\left(CH_3\right)_2-CH_3\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam chất hữu cơ A cần phải dùng 19,2 gam oxi, thu được 26,4 gam CO 2 và 10,8 gam H 2 O . Xác định công thức phân tử của A biết 170 gam/mol > d > 190 gam/mol.
M A = 30n → 170 < 30n < 190
→ n = 6.
Công thức phân tử của A là C 6 H 12 O 6
Đúng 0
Bình luận (0)
Câu 31: Đốt cháy hoàn toàn 4,4 gam hợp chất hữu cơ A thu được 13,2 gam khí CO2 và 7,2 gam nước.
a) A có những nguyên tố nào?
b) Tìm công thức phân tử của A biết khối lượng mol của A bằng 44 gam/mol
c) Viết CTCT đầy đủ và thu gọn của A.
a, Bảo toàn C: \(n_C=\dfrac{13,2}{44}=0,3\left(mol\right)\)
Bảo toàn H: \(n_H=\dfrac{2.7,2}{18}=0,8\left(mol\right)\)
Xét mH + mC = 0,3.12 + 0,8 = 4,4 => A chỉ có C và H
b, CTPT CxHy
=> x : y = 0,3 : 0,8 = 3 : 8
=> (C3H8)n = 44
=> n = 1
CTPT: C3H8
c, CTCT:
\(CH_3-CH_2-CH_3\)
Đúng 3
Bình luận (0)
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{13,2}{44}=0,3mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{7,2}{18}=0,8mol\)
\(n_O=\dfrac{4,4-\left(0,3.12+0,8\right)}{16}=0mol\)
=> A gồm C và H
\(CTHH:C_xH_y\)
\(x:y=0,3:0,8=3:8\)
\(CTĐG:\left(C_3H_8\right)n=44\)
\(\Leftrightarrow n=1\)
\(\rightarrow CTPT:C_3H_8\)
CTCT đầy đủ:
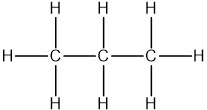
CTCT thu gọn:\(CH_3-CH_2-CH_3\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 9 gam một hh chất hữu cơ A thì thu được 13,2 gam khí cacboic và 5,4 gam nước .Phân tử khối của hợp chất hữu cơ là 180.Hãy xác định công thức phân tử của hợp chất hữu cơ đó
Xem chi tiết
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,6.1 = 4,2 (g) < mA
⇒ A có các nguyên tố C, H và O.
⇒ mO = 9 - 4,2 = 4,8 (g)
\(\Rightarrow n_O=\dfrac{4,8}{16}=0,3\left(mol\right)\)
Giả sử CTPT của A là CxHyOz. (x, y, z nguyên dương)
⇒ x : y : z = 0,3 : 0,6 : 0,3 = 1: 2 : 1
⇒ CTĐGN của A là (CH2O)n (n nguyên dương)
Mà: MA = 180 (g/mol)
\(\Rightarrow n=\dfrac{180}{12+2+16}=6\left(tm\right)\)
Vậy: A là C6H12O6.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Đốt cháy hoà toàn 4,5 gam một hợp chất hữu cơ A thấy sinh ra 6,6 gam khí CO2 và 2,7 gam H2O. Biết khối lượng mol của A bằng 60. Xác định công thức phân tử của A.
\(n_{CO_2}=\dfrac{m}{M}=\dfrac{6,6}{44}=0,15\left(mol\right)\\ \Rightarrow n_C=n_{CO_2}=0,15\left(mol\right)\\ n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\\ \Rightarrow n_H=2.n_{H_2O}=2.0,15=0,3\left(mol\right)\\ \Rightarrow n_O=\dfrac{4,5-0,3-0,15.12}{16}=0,15\left(mol\right)\\ Đặt.CTHH.của.A:C_xH_yO_z\)
\(\Rightarrow x:y:z=0,15:0,3:0,15=1:2:1\\ \Rightarrow CTPT.của.A.có.dạng:\left(CH_2O\right)_n\\ Mà.M_A=60\\ \Leftrightarrow\left(12+2+16\right).n=60\\ \Leftrightarrow n=2\\ Vậy.CTPT.của.A.là:C_2H_4O_2\)
Đúng 1
Bình luận (0)
Đốt cháy hoà toàn 4,5 gam một hợp chất hữu cơ A thấy sinh ra 6,6 gam khí CO2 và 2,7 gam H2O. Biết khối lượng mol của A bằng 60. Xác định công thức phân tử và viết công thức cấu tạo của A
Vì đốt cháy A thu CO2 và H2O nên A có C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\Rightarrow n_H=0,15.2=0,3\left(mol\right)\)
⇒ mC + mH = 0,15.12 + 0,3.1 = 2,1 (g) < mA
⇒ A có C, H và O.
⇒ mO = 4,5 - 2,1 = 2,4 (g)
\(\Rightarrow n_O=\dfrac{2,4}{16}=0,15\left(mol\right)\)
Giả sử: CTPT của A là CxHyOz.
⇒ x : y : z = 0,15 : 0,3 : 0,15 = 1:2:1
⇒ CTĐGN của A là (CH2O)n.
Mà: MA = 60 (g/mol)
\(\Rightarrow n=\dfrac{60}{12+2+16}=2\)
Vậy: CTPT của A là C2H4O2.
⇒ CTCT: CH3COOH và HCOOCH3.
Bạn tham khảo nhé!
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn 3,75 gam một chất hữu cơ A, thu được 11 gam CO2 và 6,75 gam H2O. Biết khối lượng mol của A là 30 gam. Xác định công thức phân tử của A.
a) A hợp chất hữu cơ A gồm những nguyên tố nào ?
b) xác định công thức phân tử của hợp chất hữu cơ A
c) Dẫn toàn bộ khí sinh đi qua bình đựng dung dịch NaOH dư. Tính khối lượng muối tạo thành.
a, có nCO2=11/44=0,25 mol
có nC=nCO2=0,25mol=>mC=12.0,25=3(g)
có nH2O=6,75/18=0,375mol
có nH=2nH2O=2.0,375=0,75mol=>mH=0,75(g)
=>mH+mC=0,75+3=3,75=mA
=> A gồm nguyên tố C và H
b, gọi CTPT A là CxHy
có x/y=nC/nH=0,25/0,75=1/3
=> công thức thực nghiệm (CH3)n<=>CnH3n
có MA=30 gam/mol<=>12n+3n=30<=>n=2
vậy CTPT của A là C2H6
c;PTHH: CO2+2NaOH->Na2CO3+H2O
=> nNa2CO3=nCO2=0,25mol=>mNa2CO3=0,25.106=26,5 gam
Đúng 0
Bình luận (2)
Đốt cháy hoàn toàn 9,2 gam chất hữu cơ X thu được 13,2 gam CO2 và 7,2 gam
H2O.
a. Xác định công thức đơn giản nhất của X.
b. Xác định công thức phân tử của X, biết tỉ khối hơi của X so với H2 là 46.
\(n_{CO_2}=\dfrac{13.2}{44}=0.3\left(mol\right)\)
\(n_{H_2O}=\dfrac{7.2}{18}=0.4\left(mol\right)\)
\(n_O=\dfrac{9.2-0.3\cdot12-0.4\cdot2}{16}=0.3\left(mol\right)\)
\(n_C:n_H:n_O=0.3:0.8:0.3=3:8:3\)
CT đơn giản nhất : C3H8O3
\(M_X=46\cdot2=92\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow92n=92\)
\(\Rightarrow n=1\)
\(CT:C_3H_8O_3\)
Đúng 2
Bình luận (0)
a)
$n_C = n_{CO_2} = \dfrac{13,2}{44} = 0,3(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{7,2}{18} = 0,8(mol)$
$n_O = \dfrac{9,2 -0,3.12 - 0,8.1}{16} = 0,3(mol)$
Ta có :
$n_C : n_H : n_O = 0,3: 0,8 : 0,3 = 3 : 8:3$
Vậy CTĐGN là $C_3H_8O_3$
b)
CTPT : $(C_3H_8O_3)_n$
Ta có :
$M_X = (12.3 + 8 + 16.3)n = 46.2 \Rightarrow n = 1$
Vậy CTPT là $C_3H_8O_3$
Đúng 1
Bình luận (0)






















