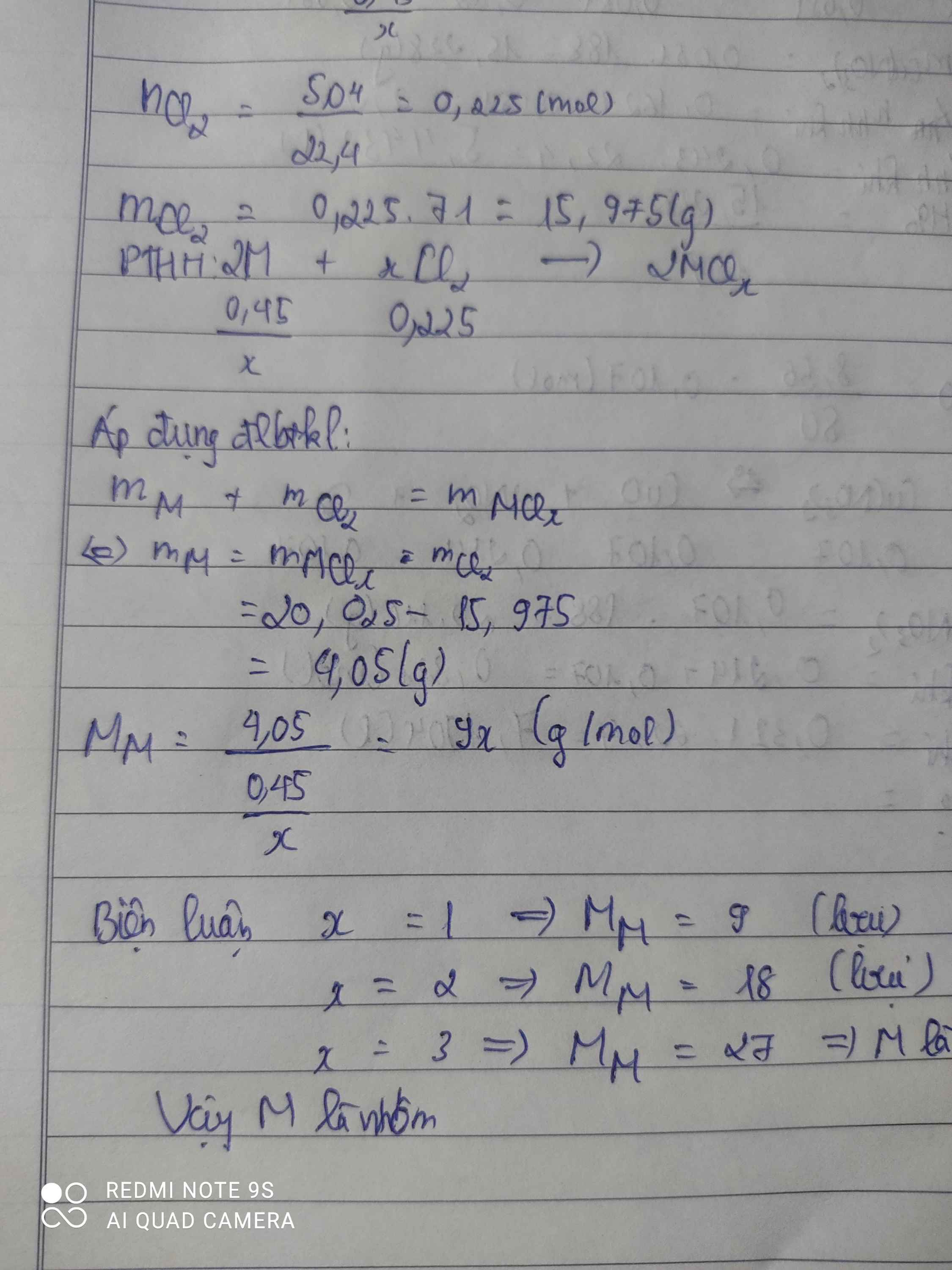Cho 2,7 gam kim loại M tác dụng hoàn toàn với clo dư sau phản ứng thu được 13,35 gam muối xác định M

Những câu hỏi liên quan
1) Xác định tên kim loại A và M khi:a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
Đọc tiếp
1) Xác định tên kim loại A và M khi:
a) Hòa tan hoàn toàn 2,7 gam kim loại A (hóa trị III) trong dung dịch HCl dư sau phản ứng thu được 13,35 gam muối.
b) Hòa tan hoàn toàn 4,8 gam kim loại M trong dung dịch HCl dư sau phản ứng thu được 4,48 lit khí (đktc).
\(a,n_A=\dfrac{2,7}{M_A}\left(mol\right)\\ n_{ACl_3}=\dfrac{13,35}{M_A+106,5}\)
PTHH: \(2A+6HCl\rightarrow2ACl_3+3H_2\)
\(\dfrac{2,7}{M_A}\)-------------->\(\dfrac{2,7}{M_A}\)
\(\rightarrow\dfrac{2,7}{M_A}=\dfrac{13,35}{M_A+106,5}\\ \Leftrightarrow M_A=27\left(g\text{/}mol\right)\)
=> A là Al
\(b,n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(2M+2nHCl\rightarrow2MCl_n+nH_2\) (n là hoá trị của M, n ∈ N*)
\(\dfrac{0,4}{n}\)<---------------------------0,2
\(\rightarrow M_M=\dfrac{4,8}{\dfrac{0,2}{n}}=12n\left(g\text{/}mol\right)\)
Vì n là hoá trị của M nên ta có bảng
| n | 1 | 2 | 3 |
| MM | 12 | 24 | 36 |
| Loại | Mg | Loại |
Vậy M là Mg
Đúng 1
Bình luận (0)
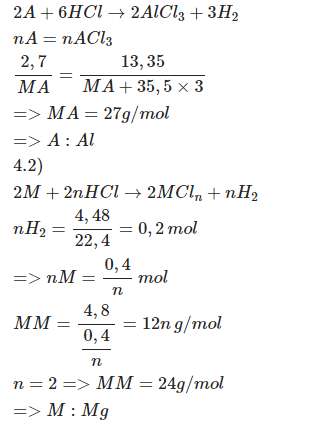
\(\Rightarrow\) \(M:mg\)
Bài 1: Cho 16 gam kim loại M hóa trị II tác dụng hết với Oxi, sau phản ứng thu được 20 gam oxit. Xác định kim loại M đem phản ứng.
Bài 2: Cho 16,2 gam kim loại R hóa trị III tác dụng với clo có dư thu được 80,1 gam muối. Xác định kim loại đem phản ứng.
Bài 1:
\(n_M=\dfrac{16}{M_M}\left(mol\right)\)
PTHH: 2M + O2 --to--> 2MO
\(\dfrac{16}{M_M}\)---------->\(\dfrac{16}{M_M}\)
=> \(\dfrac{16}{M_M}\left(M_M+16\right)=20\)
=> MM = 64 (g/mol)
=> M là Cu
Bài 2:
\(n_R=\dfrac{16,2}{M_R}\left(mol\right)\)
PTHH: 2R + 3Cl2 --to--> 2RCl3
\(\dfrac{16,2}{M_R}\)------------>\(\dfrac{16,2}{M_R}\)
=> \(\dfrac{16,2}{M_R}\left(M_R+106,5\right)=80,1\)
=> MR = 27 (g/mol)
=> R là Al
Đúng 2
Bình luận (0)
1
ADDDLBTKL ta có
\(m_{O_2}=m_{MO}-m_M\\
m_{O_2}=20-16=4g\\
n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\\
pthh:2M+O_2\underrightarrow{t^o}2MO\)
0,25 0,125
\(M_M=\dfrac{16}{0,25}=64\left(\dfrac{g}{mol}\right)\)
=> M là Cu
2
ADĐLBTKL ta có
\(m_{Cl_2}=m_{RCl_3}-m_R\\
m_{Cl_2}=80,1-16,2=63,9g\\
n_{Cl_2}=\dfrac{63,9}{71}=0,9\left(mol\right)\\
pthh:2R+3Cl_2\underrightarrow{t^o}2RCl_3\)
0,6 0,9
\(M_R=\dfrac{16,2}{0,6}=27\left(\dfrac{g}{mol}\right)\)
=> R là Al
Đúng 1
Bình luận (0)
\(1 ) 2M+O_2\rightarrow 2MO n_M=n_{MO}\Leftrightarrow \dfrac{16}{M_M}=\dfrac{20}{m_M+16} \Rightarrow m_m = 64(g/mol) \rightarrow M : Cu \)
\(2) 2R+3Cl_2\rightarrow 2RCl_3 n_R=nn_{RCl_3}\Leftrightarrow \dfrac{16,2}{M_R}=\dfrac{80,1}{M_R+35,5.3}\Rightarrow M_R = 27(g/mol)\rightarrow R:Al \)
Đúng 2
Bình luận (0)
Cho kim loại M tác dụng vừa đủ với 5,04 lit Clo (dkc), sau khi phản ứng xảy ra hoàn toàn ta thu được 20, 025 gam muối. Xác định tên của kim dùng.
\(n_{Cl_2}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\)
PTHH: \(2M+nCl_2\underrightarrow{t^o}2MCl_n\)
0,225-->\(\dfrac{0,45}{n}\)
=> \(M_{MCl_n}=M_M+35,5n=\dfrac{20,025}{\dfrac{0,45}{n}}\)
=> MM = 9n (g/mol)
Xét n = 1 => L
Xét n = 2 => L
Xét n = 3 => MM = 27(g/mol) => M là Nhôm (Al)
Đúng 4
Bình luận (1)
Gọi x là hoá trị của M (x:nguyên, dương)
\(2M+xCl_2\rightarrow\left(t^o\right)2MCl_x\\ n_{Cl_2}=\dfrac{5,04}{22,4}=0,225\left(mol\right)\\ \Rightarrow n_{MCl_x}=\dfrac{0,225.2}{x}=\dfrac{0,45}{x}\left(mol\right)\\ \Rightarrow M_{MCl_x}=\dfrac{20,025}{\dfrac{0,45}{x}}=44,5x\left(\dfrac{g}{mol}\right)\)
Xét các TH x=1;x=2;x=3 => Thấy x=3 là thoả mãn
=> MClx là MCl3 và KLR sẽ bằng 133,5
=> M là Nhôm (Al=27)
Đúng 2
Bình luận (0)
cho 2,7 gam kim loại A tác dụng với khí clo thu 13,35 gam muối clorua kim loại . Xác định kim loại A và thể tích khí clo cần dùng ( điều kiện tiêu chuẩn ).
Muối: ACln có A + 35,5n = 13,35/2,7/A = 4,94A hay A = 9n.
Vậy n = 3 và A = 27 (Al).
VCl2 = 1,5.0,1.22,4 = 3,36 lít.
Đúng 0
Bình luận (0)
cho 2,7 gam kim loại A tác dụng với khí clo thu 13,35 gam muối clorua kim loại . Xác định kim loại A và thể tích khí clo cần dùng ( điều kiện tiêu chuẩn ).
mCl2= 13,35 - 2,7 = 10,65 g
nCl2= 10,65/71 = 0,15 mol
VCl2= 0,15 x 22.4 = ..... (lít)
2A + nCl2 -> 2ACln (n là hoá trị KLoai nhé)
nA= 0,15x2/n = 0,3/n (mol)
MA= 2,7 / (0,3/n) = 9n
Biện luận: n = 3 => MA= 27 => A là nhôm
Mấy cái này dễ lắm lắm đó bạn, học cho kĩ nhé chứ vầy mà k biết làm thì mình cũng k biết sao :)
Đúng 0
Bình luận (0)
bn đã nói vậy thì mình cũng nói thật . từ trước đến giờ mình có quen làm những bài tập tính toán về môn hóa như thế này đâu , minh ko hok giỏi hóa ![]()
Đúng 0
Bình luận (0)
Cho 7,35 gam hỗn hợp hồn 2 kim loại kẽm,sắt tác dụng với khí Clo vừa đủ để phản ứng xảy ra hoàn toàn,sau phản ứng thu được 17,645 gam hỗn hợp muối X
a)Xác định % các chất có trong hỗn hợp X?
b)Cho hỗn hợp muối X tác dụng hoàn toàn với lượng dư dung dịch AgNO3.Thu được a gam kết tủa.Xác định giá trị của a?
Xem chi tiết
cho M gam kim loại R có hóa trị II tác dụng với Clo dư,sau phản ứng thu được 13,6 gam muối,mặt khác,để hòa tan M gam kim loại R cần vừa đủ 200ml dung dịch HCL có nồng độ 1M
a, viết pthh
b,xác định kim loại R
giúp mình với ạ
R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)
Đúng 2
Bình luận (0)
Cho 10,8 gam kim loại M phản ứng hoàn toàn với khí clo dư, thu được 53,4 gam muối. Kim loại M là
A. Al
B. Mg
C. Fe
D. Zn
Đáp án : A
Giả sử M có hóa trị x :
2M + xCl2 -> 2MClx
2M 2(M + 35,5x) (g)
10,8 53,4 (g)
=> 2M.53,4 = 10,8.2(M + 35,5x)
=> M = 9x
Nếu x = 3 thì M = 27g (Al)
Đúng 0
Bình luận (0)
Cho 10,8 gam kim loại M phản ứng hoàn toàn với khí clo dư, thu được 53,4 gam muối. Kim loại M là
A. Zn
B. Al
C. Fe.
D. Mg