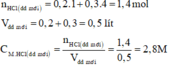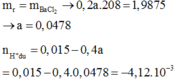Trộn 200ml dung dịch HCL 1.5M với 300ml dung dịch HCL 2.5M.Tính nồng độ mol của dung dịch mới

Những câu hỏi liên quan
Trộn 200ml dung dịch HCl 1M với 300ml dung dịch HCl 0,5M. Tính nồng độ mol của dung dịch HCl sau khi trộn.
\(V_{\text{dd}}=0,2+0,3=0,5\left(l\right)\\ n_{HCl}=0,2.1+0,3.0,5=0,35\\ C_M=\dfrac{0,35}{0,5}=0,7M\)
Đúng 6
Bình luận (0)
200ml = 0,2(l)
=> nHCl (1) = 0,2 .1 = 0,2 (mol)
300ml = 0,3 (l)
=> nHCl(2) = 0,3 . 0,5 = 0,15 (mol)
=> CM (sau khi trộn) = n/V = (0,15+0,2) / (0,2+0,3 ) = 0,35 / 0,5 = 0,7 M
Đúng 4
Bình luận (0)
Pha trộn 200ml dung dịch HCl 1M với 300ml dung dịch HCl 2M. Nếu pha trộn không làm co giãn thể tích thì dung dịch mới có nồng độ mol/l là:
A. 1,5M
B. 1,2M
C. 1,6M
D. 0,15M
Khi trộn 200ml dung dịch HCl 1M với 300ml dung dịch HCl 4M thì thu được dung dịch mới có nồng độ là
A. 2M
B. 2,5M
C. 2,8M
D. 3,0M
Nồng độ mol của chất trong dung dịch thu được khi trộn 200ml dung dịch HCl 2M và 300ml dung dịch HCl 4M là?
\(\sum\)nHCl=0,2.2+0,3.4=1,6(mol)
CM dd HCl=\(\dfrac{1,6}{0,5}=3,2M\)
Đúng 0
Bình luận (0)
1/ Trộn 200ml dung dịch NaOH 0,4M với 400ml dung dịch HCl 0,3M. Tính nồng độ mol/ lít của các ion có trong dung dịch thu đc
2/ Trộn 200ml dung dịch KCl 1,5M với 300ml dung dịch K2SO4 2M. Tính nồng độ mol/ lít của các ion có trong dung dịch thu đc
Bài 1:
Ta có: \(n_{OH^-}=n_{Na^+}=n_{NaOH}=0,2.0,4=0,08\left(mol\right)\)
\(n_{H^+}=n_{Cl^-}=n_{HCl}=0,4.0,3=0,12\left(mol\right)\)
PT ion: \(OH^-+H^+\rightarrow H_2O\)
_____0,08_____0,12 (mol)
⇒ nOH- (dư) = 0,04 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\left[Na^+\right]=\frac{0,08}{0,6}\approx0,133M\\\left[Cl^-\right]=\frac{0,12}{0,6}=0,2M\\\left[OH^-\right]=\frac{0,04}{0,6}\approx0,066M\end{matrix}\right.\)
Câu 2:
Ta có: \(\Sigma n_{K^+}=n_{KCl}+2n_{K_2SO_4}=0,2.1,5+0,3.2.2=1,5\left(mol\right)\)
\(n_{Cl^-}=n_{KCl}=0,2.1,5=0,3\left(mol\right)\)
\(n_{SO_4^{2-}}=0,3.2=0,6\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\left[K^+\right]=\frac{1,5}{0,5}=3M\\\left[Cl^-\right]=\frac{0,3}{0,5}=0,6M\\\left[SO_4^{2-}\right]=\frac{0,6}{0,5}=1,2M\end{matrix}\right.\)
Bạn tham khảo nhé!
Trộn lẫn 200ml dung dịch H2SO4 0,05M với 300ml dung dịch HCl 0,1M ta được dung dịch D .
a)tính nồng độ mol / l của H2SO4 , HCl và ion H+ trong dung dịch D . b)Tính pH của dung dịch D . c) Lấy 150ml dung dịch D trung hòa bởi 50ml dung dịch KOH . Tính nồng độ dung dịch KOH đem dùngtìm nồng độ mol/l của các ion trong dung dịch thu được khi
a, trộn 300ml dung dịch \(CuCl_2\) 1M vào 200ml dung dịch \(BaCl_2\) 0,5M
b, trộn 200ml dung dịch NaCl 1M vào 300ml dung dịch HCl 1M
a) Ta có: \(\left\{{}\begin{matrix}n_{CuCl_2}=0,3\left(mol\right)\\n_{BaCl_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left[Cu\right]=\dfrac{0,3}{0,5}=0,6\left(M\right)\\ \Rightarrow\left[Ba\right]=\dfrac{0,1}{0,5}=0,2\left(M\right)\\ \Rightarrow\left[Cl\right]=\dfrac{0,3.2+0,1.2}{0,5}=1,6\left(M\right)\)
Đúng 0
Bình luận (0)
Cho 300ml dung dịch Ba(OH)2 0,5M tác dụng vừa đủ với 200ml ddhcl.
a.Tính nồng độ mol dung dịch hcl cần dùng.
b.Tính nồng độ mol của dung dịch sau phản ứng.
\(a.300ml=0,3l\\ n_{Ba\left(OH\right)_2}=0,3.0,5=0,15mol\\ Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
0,15 0,3 0,15
\(200ml=0,2l\\ C_{M_{HCl}}=\dfrac{0,3}{0,2}=1,5M\\ b.C_{M_{BaCl_2}}=\dfrac{0,15}{0,3+0,2}=0,3M\)
Đúng 2
Bình luận (2)
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
Đọc tiếp
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
![]()
![]()
![]()
![]()