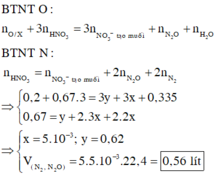Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với với oxi không khí, sau phản ứng thu được 39,2 g hỗn hợp A gồm (CuO, FeO , Fe2O3 và Fe3O4) . Hòa tan hoàn toàn A trong dd H2SO4 loãng, dư . Tính khối lượng muối sunfat thu được.

Những câu hỏi liên quan
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. 1. Tính số mol H2SO4 đã tham gia phản ứng 2. Tính khối lượng muối sunfat thu được. b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
Đọc tiếp
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. 1. Tính số mol H2SO4 đã tham gia phản ứng 2. Tính khối lượng muối sunfat thu được.
b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
a, Ta có: $n_{O}=0,6(mol)$
Suy ra $n_{H^+/pu}=1,2(mol)\Rightarrow n_{H_2SO_4}=0,6(mol)$
Bảo toàn khối lượng ta có: $m_{muoi}=29,6+0,6.96=87,2(g)$
Đúng 1
Bình luận (0)
Theo gt ta có: $n_{H_2}=0,044(mol);n_{H_2/(2)}=0,033(mol)$
Gọi CTTQ của oxit là $M_xO_y$
Ta có: \(M_{M_xO_y}=58y\)
Mặt khác $m_{M}=2,552-0,044.16=1,848(g)\Rightarrow M_{M}=28n$
Vậy M là Fe
Do đó CT của oxit cần tìm là Fe3O4
Đúng 1
Bình luận (0)
Cho 39,2 gam hỗn hợp M gồm Fe, FeO, Fe3O4, Fe2O3, CuO và Cu (trong đó oxi chiếm 18,367% về khối lượng) tác dụng vừa đủ với 250 ml dung dịch H2so4 nồng độ a mol/l. Sau khi phản ứng xong, thu được 0,4 mol SO2 (sản phẩm khử duy nhất). Tính a. Biết axit lấy dư 20%
n O = 39,2.18,367%/16 = 0,45(mol)
Bảo toàn e :
n SO4 2-(trong muối) = n e cho = 2n O + 2n SO2 = 0,45.2 + 0,4.2 = 1,7(mol)
Bảo toàn nguyên tố với S :
n H2SO4 pư = n SO4 2-(trong muối) + n SO2 = 1,7 + 0,4 = 2,1(mol)
=> n H2SO4 đã dùng = 2,1/(100% -20%) = 2,625(mol)
=> a = CM H2SO4 = 2,625/2,5 = 1,05(M)
Đúng 2
Bình luận (0)
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. --Tính số mol H2SO4 đã tham gia phản ứng -- Tính khối lượng muối sunfat thu được.b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc).---Xác định công thức của oxit kim loại đã dùng?
Đọc tiếp
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư.
--Tính số mol H2SO4 đã tham gia phản ứng
-- Tính khối lượng muối sunfat thu được.
b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc).
---Xác định công thức của oxit kim loại đã dùng?
1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi \(\rightarrow\) (hỗn hợp oxit ) + axit \(\rightarrow\) muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=> \(n_O=\frac{9,6}{16}=0,6mol\)
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 \(\rightarrow\) xM + yH2O (1)
\(n_{H_2}=\frac{985,6}{22,4.1000}=0,044\left(mol\right)\)
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl \(\rightarrow\) 2MCln + nH2 (2)
\(n_{H_2}=\frac{739,2}{22,4.1000}=0,033\left(mol\right)\)
(2) => \(\frac{1,848}{M}.n=2.0,033\)
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1) \(\frac{x}{y}=\frac{n_M}{n_{H_2}}=\frac{0,033}{0,044}=\frac{3}{4}\)
=> oxit cần tìm là Fe3O4
Đúng 0
Bình luận (0)
1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi ![]() (hỗn hợp oxit ) + axit
(hỗn hợp oxit ) + axit ![]() muối + H2O
muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=> ![]()
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 ![]() xM + yH2O (1)
xM + yH2O (1)
![]()
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl ![]() 2MCln + nH2 (2)
2MCln + nH2 (2)
![]()
(2) => ![]()
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1) ![]()
=> oxit cần tìm là Fe3O4
Đúng 0
Bình luận (0)
ta có VH2 = 985,6ml=0,9856l
VH2 sau phản ứng= 739,2ml=0,7392l
Trong phản ứng ta thấy cứ mỗi mol H2 tác dụng vs 1 mol O tạo thành H2o nên số mol O=H2
no=nh2=V:22,4= 0,9856:22,4=0,044 mol
=> m0=n.M=0,044.16=0,704g
mR=2,552-0,704=1,848g
gọi a là hóa tri kim loại R
2R+2aHCl => 2RCla+aH2
2 2a 2 a
0,066:a 0,033
nH2=V:22,4=0,7392:22,4=0,033
từ pt => n R=0,066:a
mặt khác có mR=1,848g
<=> 1,848=0,066:a.R
<=>28a=R
vì R là kim loại nên a nhân giá trị 1,2,3
ta nhân a=2 =>R=56
vậy R là Fe
gọi cthh của R là FexOy
ta có
nFe=x=m:M=1,848:56x=0,033 mol(1)
nO=y=m:M=0,704:16y=0,044(2)
x:y=(1):(2)=0,033:0,044=3:4
vây cthh là Fe3O4
bạn xem kĩ nha
Đúng 0
Bình luận (0)
Để hòa tan hoàn toàn 28,8 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe cần vừa đủ 180 gam dung dịch HCl 18,25%. Sau phản ứng thu được V lít khí H2 và dung dịch B. Cho toàn bộ lượng H2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 1,6 gam.a) Nếu cô cạn dung dịch B thì thu được bao nhiêu gam muối khan.b) Nếu hỗn hợp A ban đầu tỉ lệ mol Fe2O3 : FeO 1:1. Tính nồng độ phần trăm của mỗi chất có trong dung d...
Đọc tiếp
Để hòa tan hoàn toàn 28,8 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO và Fe cần vừa đủ 180 gam dung dịch HCl 18,25%. Sau phản ứng thu được V lít khí H2 và dung dịch B. Cho toàn bộ lượng H2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 1,6 gam.
a) Nếu cô cạn dung dịch B thì thu được bao nhiêu gam muối khan.
b) Nếu hỗn hợp A ban đầu tỉ lệ mol Fe2O3 : FeO = 1:1. Tính nồng độ phần trăm của mỗi chất có trong dung dịch B.
Hòa tan hoàn toàn 57,6 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO, Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít H2 (đktc) và dung dịch B. Cho toàn bộ H2 sinh ra tác dụng hết với CuO dư ở điều kiện nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. a) Nếu cô cạn dung dịch B, ta thu được bao nhiêu gam muối khan? b) Nếu hỗn hợp A ban đầu có tỉ lệ mol Fe2...
Đọc tiếp
Hòa tan hoàn toàn 57,6 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO, Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít H2 (đktc) và dung dịch B. Cho toàn bộ H2 sinh ra tác dụng hết với CuO dư ở điều kiện nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam.
a) Nếu cô cạn dung dịch B, ta thu được bao nhiêu gam muối khan?
b) Nếu hỗn hợp A ban đầu có tỉ lệ mol Fe2O3 : FeO = 1 : 1. Tính nồng độ phần trăm các chất có trong dung dịch B.
c) Hỗn hợp X cũng chứa Fe3O4, Fe2O3, FeO, Fe. Nếu dùng 100 gam X cho tác dụng với 2 lít dung dịch HCl 2M. Chứng minh rằng hỗn hợp X tan hết.
a) \(n_{HCl}=\dfrac{360.18,25\%}{36,5}=1,8\left(mol\right)\)
Sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam.
\(n_{H_2}=n_{O\left(trongCuO\right)}=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H: \(n_{HCl}=2n_{H_2}+2n_{H_2O}\Rightarrow n_{H_2O}=0,7\left(mol\right)\)
=> \(n_{O\left(trongA\right)}=0,7\left(mol\right)\)
\(m_{muối}=m_{Fe}+m_{Cl}=\left(57,6-0,7.16\right)+1,8.35,5=110,3\left(g\right)\)
b) B gồm FeCl3 và FeCl2
Gọi x,y lần lượt là số mol của FeCl2 và FeCl3
\(\left\{{}\begin{matrix}3x+2y=1,8\\162,5x+127y=110,3\end{matrix}\right.\)
=> \(x=\dfrac{1}{7};y=\dfrac{24}{35}\)
\(m_{ddB}=m_A+m_{ddHCl}-m_{H_2}=417,2\left(g\right)\)
=> \(C\%_{FeCl_3}=\dfrac{\dfrac{1}{7}.162,5}{417,2}.100=5,56\%\)
\(C\%_{FeCl_2}=\dfrac{\dfrac{24}{35}.127}{417,2}.100=20,87\%\)
c) \(n_{HCl\left(bđ\right)}=2.2=4\left(mol\right)\)
Nếu trong X chỉ chứa Fe3O4 thì :
\(n_{HCl}=8n_{Fe_3O_4}=8.\dfrac{100}{232}=3,45\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe2O3 thì :
\(n_{HCl}=6n_{Fe_3O_4}=6.\dfrac{100}{160}=3,75\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa FeO thì :
\(n_{HCl}=2n_{FeO}=2.\dfrac{100}{72}=2,78\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe thì :
\(n_{HCl}=2n_{Fe}=2.\dfrac{100}{56}=3,57\left(mol\right)< n_{HCl\left(bđ\right)}\)
=> HCl luôn dư và X luôn tan hết
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 57,6 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO, Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít H2 (đktc) và dung dịch B. Cho toàn bộ H2 sinh ra tác dụng hết với CuO dư ở điều kiện nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam.
a) Nếu cô cạn dung dịch B, ta thu được bao nhiêu gam muối khan?
b) Nếu hỗn hợp A ban đầu có tỉ lệ mol Fe2O3 : FeO 1 : 1....
Đọc tiếp
Hòa tan hoàn toàn 57,6 gam hỗn hợp A gồm Fe3O4, Fe2O3, FeO, Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít H2 (đktc) và dung dịch B. Cho toàn bộ H2 sinh ra tác dụng hết với CuO dư ở điều kiện nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. a) Nếu cô cạn dung dịch B, ta thu được bao nhiêu gam muối khan? b) Nếu hỗn hợp A ban đầu có tỉ lệ mol Fe2O3 : FeO = 1 : 1. Tính nồng độ phần trăm các chất có trong dung dịch B. c) Hỗn hợp X cũng chứa Fe3O4, Fe2O3, FeO, Fe. Nếu dùng 100 gam X cho tác dụng với 2 lít dung dịch HCl 2M. Chứng minh rằng hỗn hợp X tan hết. Ghi rõ pt và giải rõ a b c giúp e vs ạ
Bạn xem bài của bạn Thảo Phương : https://hoc24.vn/cau-hoi/hoa-tan-hoan-toan-576-gam-hon-hop-a-gom-fe3o4-fe2o3-feo-fe-trong-dung-dich-hcl-thi-can-dung-360-gam-dung-dich-hcl-1825-de-tac-dung-vua-du-sau-p.1336663119282
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 17,44 gam hỗn hợp X gồm Fe, Fe3O4, Fe2O3, CuO, Cu, Mg, MgO (trong đó oxi chiếm 18,35% về khối lượng) trong dung dịch chứa 0,804 mol HNO3 loãng (dư 20% so với lượng cần cho phản ứng), kết thúc các phản ứng thu được dung dịch Y và V lít (đktc) hỗn hợp khí Z gồm N2 và N2O (tỷ lệ số mol tương ứng là 2:3). Cho dung dịch NaOH tới dư vàoY rồi đun nóng, không có khí thoát ra. Giá trị của V là A. 0,56. B. 0,448. C. 1,39. D. 1,12.
Đọc tiếp
Hòa tan hoàn toàn 17,44 gam hỗn hợp X gồm Fe, Fe3O4, Fe2O3, CuO, Cu, Mg, MgO (trong đó oxi chiếm 18,35% về khối lượng) trong dung dịch chứa 0,804 mol HNO3 loãng (dư 20% so với lượng cần cho phản ứng), kết thúc các phản ứng thu được dung dịch Y và V lít (đktc) hỗn hợp khí Z gồm N2 và N2O (tỷ lệ số mol tương ứng là 2:3). Cho dung dịch NaOH tới dư vàoY rồi đun nóng, không có khí thoát ra. Giá trị của V là
A. 0,56.
B. 0,448.
C. 1,39.
D. 1,12.
Hòa tan hoàn toàn 17,44 gam hỗn hợp X gồm Fe, Fe3O4, Fe2O3, CuO, Cu, Mg, MgO (trong đó oxi chiếm 18,35% về khối lượng) trong dung dịch chứa 0,804 mol HNO3 loãng (dư 20% so với lượng cần cho phản ứng), kết thúc các phản ứng thu được dung dịch Y và V lít (đktc) hỗn hợp khí Z gồm N2 và N2O (tỷ lệ số mol tương ứng là 2:3). Cho dung dịch NaOH tới dư vàoY rồi đun nóng, không có khí thoát ra. Giá trị của V là A. 0,56 B. 0,448 C. 1,39 D. 1,12
Đọc tiếp
Hòa tan hoàn toàn 17,44 gam hỗn hợp X gồm Fe, Fe3O4, Fe2O3, CuO, Cu, Mg, MgO (trong đó oxi chiếm 18,35% về khối lượng) trong dung dịch chứa 0,804 mol HNO3 loãng (dư 20% so với lượng cần cho phản ứng), kết thúc các phản ứng thu được dung dịch Y và V lít (đktc) hỗn hợp khí Z gồm N2 và N2O (tỷ lệ số mol tương ứng là 2:3). Cho dung dịch NaOH tới dư vàoY rồi đun nóng, không có khí thoát ra. Giá trị của V là
A. 0,56
B. 0,448
C. 1,39
D. 1,12
Hòa tan hoàn toàn 17,44 gam hỗn hợp X gồm Fe, Fe3O4, Fe2O3, CuO, Cu, Mg, MgO (trong đó oxi chiếm 18,35% về khối lượng) trong dung dịch chứa 0,804 mol HNO3 loãng (dư 20% so với lượng cần cho phản ứng), kết thúc các phản ứng thu được dung dịch Y và V lít (đktc) hỗn hợp khí Z gồm N2 và N2O (tỷ lệ số mol tương ứng là 2:3). Cho dung dịch NaOH tới dư vàoY rồi đun nóng, không có khí thoát ra. Giá trị của V là A. 0,56 B. 0,448 C. 1,39 D. 1,12
Đọc tiếp
Hòa tan hoàn toàn 17,44 gam hỗn hợp X gồm Fe, Fe3O4, Fe2O3, CuO, Cu, Mg, MgO (trong đó oxi chiếm 18,35% về khối lượng) trong dung dịch chứa 0,804 mol HNO3 loãng (dư 20% so với lượng cần cho phản ứng), kết thúc các phản ứng thu được dung dịch Y và V lít (đktc) hỗn hợp khí Z gồm N2 và N2O (tỷ lệ số mol tương ứng là 2:3). Cho dung dịch NaOH tới dư vàoY rồi đun nóng, không có khí thoát ra. Giá trị của V là
A. 0,56
B. 0,448
C. 1,39
D. 1,12