Sục 1,792 lít CO2 ( đktc ) vào dung dịch chứa 2 lít dung dịch Ca(OH)2 0,05M . Tính nồng độ chất trong dung dịch thu được .
Tính nồng độ mol của chất tan trong dung dịch thu được trong các thí nghiệm sau:
a/ Sục 448 ml CO2 (đktc) vào 400 ml dung dịch Ca(OH)2 0,02M.
b/ Sục 4,032 lít SO2 (đktc) vào 200 ml dung dịch Ba(OH)2 1M.
Hấp thụ hoàn toàn 1,792 lít khí CO2 (đktc) vào 100 ml dung dịch Ca(OH)2 0,5M, thu được dung dịch X. Coi thể tích dung dịch không thay đổi, nồng độ mol của chất tan trong dung dịch X là
A. 0,4M
B.0,15M
C. 0,3M
D. 0,6M
Sục rất từ từ V lít CO2 (đktc) vào 184g dung dịch Ca(OH)2 20% thì thu được 30g kết tủa. Tính V và nồng độ phần trăm của các chất có trong dung dịch sau phản ứng
$n_{Ca(OH)_2} = \dfrac{185.20\%}{74} = 0,5(mol)$
$n_{CaCO_3} = 0,3(mol)$
TH1 : Ca(OH)2 dư
Ca(OH)2 + CO2 → CaCO3 + H2O
0,3..............0,3.........0,3........................(mol)
V = 0,3.22,4 = 6,72 lít
$m_{dd} = 0,3.44 + 185 - 30 = 168,2(gam)$
$C\%_{Ca(OH)_2\ dư} = \dfrac{(0,5 - 0,3).74}{168,2}.100\% = 8,8\%$
TH2 : Có tạo muối axit
Ca(OH)2 + CO2 → CaCO3 + H2O
0,3..............0,3.........0,3........................(mol)
Ca(OH)2 + 2CO2 → Ca(HCO3)2
0,2.............0,4...............0,2.........................(mol)
V = (0,3 + 0,4).22,4 = 15,68 lít
$m_{dd} = 0,7.44 + 185 - 30 = 185,8(gam)$
$C\%_{Ca(HCO_3)_2} = \dfrac{0,2.162}{185,8}.100\% = 17,4\%$
Theo gt ta có: $n_{Ca(OH)_2}=\frac{92}{185}(mol)$
+, Xét trường hợp 1: Chỉ tạo muối $CaCO_3$
$\Rightarrow n_{CO_2}=n_{CaCO_3}=0,3(mol)\Rightarrow V=6,72(l)$
Bảo toàn khối lượng ta có: $m_{dd}=167,2(g)$
$\Rightarrow \%C_{Ca(OH)_2}=8,73\%$
+, Xét trường hợp 2: Tạo 2 muối
Bảo toàn Ca ta có: $n_{Ca(HCO_3)_2}=\frac{73}{370}(mol)$
Bảo toàn C ta có: $n_{CO_2}=\frac{257}{370}(mol)\Rightarrow V_{CO_2}=15,56(l)$
$\Rightarrow \%m_{Ca(HCO_3)_2}=17,3\%$
Sục 3,92 lít CO2 (đktc) vào dung dịch chứa Ca(OH)2 0,012M và NaOH 0,027M. Sau phản ứng, thu được dung dịch chỉ chứa hai chất tan có cùng nồng độ mol và a gam kết tủa. Giá trị lớn nhất của a là
A. 7.
B. 8.
C. 9.
D. 10.
Sục V lít khí CO2 (đktc) vào 2 lít dung dịch Ca(OH)2 0,05M , thu được 7,5 gam kết tủa . Gía trị V là
A. 1,68 lít
B. 2,88 lít
C. 2,24 lít và 2,8 lít
D. 1,68 lít và 2,8 lít
Đáp án : D
Ta có : n CaCO3 = 7,5 /100 = 0,075 mol
n Ca(OH)2 = 0,1 mol
ta thấy : nCaCO3 ≠ nCa(OH)2 => có 2 trường hợp
TH1 : chỉ xảy ra phản ứng tạo CaCO3 và Ca(OH)2 dư
CO2 + Ca(OH)2 → CaCO3 + H2O
0,075 0,075
=> VCO2 = 0,075.22,4 = 1,68 lít
TH2 : xảy ra 2 phản ứng tạo muối CaCO3và Ca(HCO3)2
CO2 + Ca(OH)2 → CaCO3 + H2O
0,075 0,075
2CO2 + Ca(OH)2 → Ca(HCO3)2
0,05 0,025
=> tổng nCO2 = 0,075 + 0,05 = 0,125 mol
=> VCO2 = 0,125.22,4 = 2,8 lít
=> Đáp án D
CÁCH KHAC : Sử dụng phương pháp đồ thị
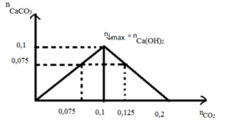
Dựa vào đồ thị => n CO2 = 0,075 mol hoặc n CO2 = 0,125 mol
=> VCO2 = 0,075.22,4 =1,68 lít hoặc VCO2 = 0,125.22,4 = 2,8 lít
1. Hấp thụ hoàn toàn 2,688 lít CO2(đktc) vào 100ml dung dịch Ca(OH)2 1M thu được dung dịch X. Tính khối lượng muối tan trong dung dịch X.
2. Hấp thụ hoàn toàn 5,04 lít CO2(đktc) vào dung dịch chứa 250ml dung dịch Ba(OH)2 0,5M thu được dung dịch X. Tính khối lượng muối sau phản ứng.
\(n_{CO_2}=\dfrac{2.688}{22.4}=0.12\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0.1\cdot1=0.1\left(mol\right)\)
\(T=\dfrac{0.12}{0.1}=1.2\)
=> Tạo 2 muối
\(n_{CaCO_3}=a\left(mol\right),n_{Ca\left(HCO_3\right)_2}=b\left(mol\right)\)
Ta có :
\(a+b=0.1\)
\(a+2b=0.12\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.08\\b=0.02\end{matrix}\right.\)
\(m_{Ca\left(HCO_3\right)_2}=0.02\cdot162=3.24\left(g\right)\)
\(n_{CO_2}=\dfrac{5.04}{22.4}=0.225\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0.25\cdot0.5=0.125\left(mol\right)\)
\(T=\dfrac{0.225}{0.125}=1.8\)
=> Tạo ra 2 muối
\(n_{BaCO_3}=a\left(mol\right),n_{Ba\left(HCO_3\right)_2}=b\left(mol\right)\)
Ta có :
\(a+b=0.125\)
\(a+2b=0.225\)
\(\Rightarrow\left\{{}\begin{matrix}a=0.025\\b=0.1\end{matrix}\right.\)
\(m_{Muối}=0.025\cdot197+0.1\cdot259=30.825\left(g\right)\)
sục từ từ 0,896 lít Co2 vào 800ml dung dịch A gồm KOH 0,05M và Ca(OH)2 0,02M thu được m gam kết tủa và dung dịch A .Tính Cm dung dịch A và m
\(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(n_{KOH}=0,8.0,05=0,04\left(mol\right)\)
\(n_{Ca\left(OH\right)_2}=0,02.0,8=0,016\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3\(\downarrow\) + H2O
______0,016---->0,016---->0,016___________(mol)
2KOH + CO2 --> K2CO3 + H2O
0,04--->0,02----->0,02_____________________(mol)
K2CO3 + CO2 + H2O --> 2KHCO3
0,004<---0,004----------->0,008_______________(mol)
mCaCO3 = 0,016.100 = 1,6 (g)
A chứa K2CO3: 0,016 mol và KHCO3: 0,008 mol
\(\left\{{}\begin{matrix}C_{M\left(K_2CO_3\right)}=\dfrac{0,016}{0,8}=0,02M\\C_{M\left(KHCO_3\right)}=\dfrac{0,008}{0,8}=0,01M\end{matrix}\right.\)
Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào 50 ml dung dịch Ca(OH)2. Thu được dung dịch X. Tính nồng độ dung dịch X.
Dung dịch X chứa NaOH 0,2M và Ca(OH)2 0,1M. Sục 7,84 lít khí CO2 (đktc) vào 1,0 lít dung dịch X thì lượng kết tủa thu được là
A. 0 gam.
B. 5 gam.
C. 15 gam.
D. 10 gam.