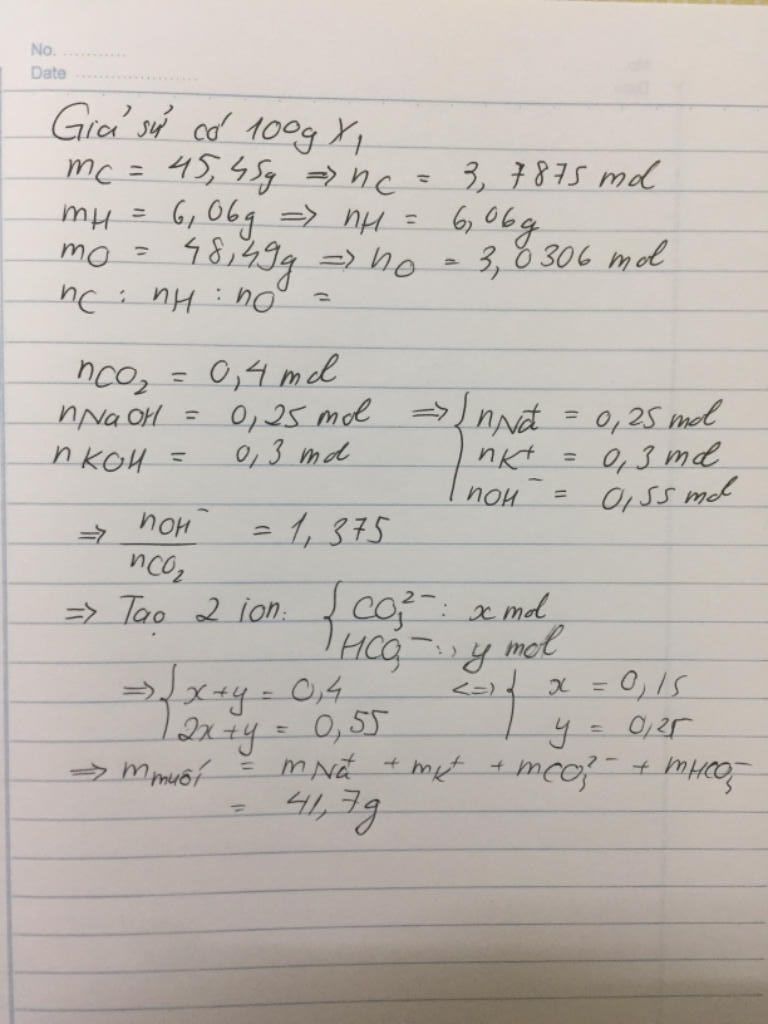Hấp thụ hoàn toàn 1,568 (l) CO2 (đktc) và 500 ml dung dịch NaOH 0,16 M thu được dung dịch X. Thêm 250 ml dung dịch Y gồm BaCl2 0,16M và Ba(OH)2 a M vào dung dịch X thu được 3,94 g kết tủa và dung dịch Z. Tính a.
Bài 16: Hợp chất của cacbon
Cho 10 g hỗn hợp gồm CaCO3 và MgCO3 vào 100 ml dung dịch HCl 1,5M. Kết thúc phản ứng, thể tích khí CO2 thu được là bao nhiêu ?
Cho thật chậm dung dịch chứa hỗn hợp 0,01 mol Na2CO3 và 0,01 mol KHCO3 vào dung dịch chứa hỗn hợp 0,04 mol HCl và 0,03 mol NaHSO4. Tính thể tích khí CO2 ở đktc
cho thật chậm dd chứa hỗn hợp 0,01mol Na2CO3 và 0,,01mol KHCO3 vào dd chứa hỗn hợp 0.04mol HCl và 0,03mol NaHSO4.Thể tích khí CO2 sinh ra đktc?
*Tk
Đúng 0
Bình luận (0)
Sục CO2 vào 200 ml hỗn hợp dung dịch gồm KOH 1M và Ba(OH)2 0,75M. Sau khi CO2 bị hấp thụ hoàn toàn thấy tạo 23,64 g kết tủa. Tính thể tích CO2 đã dùng (đktc).
Sục CO2 vào 200 ml dung dịch gồm KOH 1M và Ba(OH)2 0,75M. Sau khi khí bị hấp thụ hoàn toàn thấy tạo 23,64 gam kết tủa. T?
Đúng 0
Bình luận (0)
Sục V (l) CO2 (đktc) vào dung dịch Ba(OH)2 thu được 9,85 g kết tủa. Lọc bỏ kết tủa rồi cho dung dịch H2SO4 dư vào nước lọc thì thu thêm được 1,65 g kết tủa nữa. Tính giá trị của V.
nBaCO3 = 9,85/197 = 0,05 mol
nBaSO4 = 1,65/233 = 0,007 mol
TH1: Dd là Ba(HCO3)2
=> nBa(HCO3)2 = nBaSO4 = 0,007 mol (bảo toàn Ba)
=> nCO2 = 0,05 +0,007.2 = 0,064 mol
=> VCO2 = 0,064.22,4 = 1,437 l
TH2: Dd là Ba(OH)2
=> nBa(OH)2 = nBaSO4 = 0,007 mol (bảo toàn Ba)
=> nCO2 = 0,05 mol
=> VCO2 = 0,05.22,4 = 1,12 l
*tk (lazi)
nBaSO4 = 1,65/233 = 0,007 mol
TH1: Dd là Ba(HCO3)2
=> nBa(HCO3)2 = nBaSO4 = 0,007 mol (bảo toàn Ba)
=> nCO2 = 0,05 +0,007.2 = 0,064 mol
=> VCO2 = 0,064.22,4 = 1,437 l
TH2: Dd là Ba(OH)2
=> nBa(OH)2 = nBaSO4 = 0,007 mol (bảo toàn Ba)
=> nCO2 = 0,05 mol
=> VCO2 = 0,05.22,4 = 1,12 l
*tk (lazi)
Đúng 0
Bình luận (0)
Cho thật chậm dung dịch chứa 0,02 mol HCl và 0,02 mol NaHSO4 vào dung dịch chứa hỗn hợp 0,02 mol Na2CO3 và 0,012 mol K2CO3. Tính thể tích khí CO2 sinh ra ở đktc.
Thêm từ từ dung dich chứa 0,02 mol HCl và 0,02 mol NaHSO4 vào dung dịch chứa hỗn hợp 0,02 mol Na2CO3 và 0,012 mol K2CO3. Thể tích khí CO2 sinh ra là?
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 8,96 (l) khí CO2 (đktc) vào 500 ml dung dịch NaOH xM. Sau phản ứng thu được dung dịch X có chứa
36,9 g chất tan. Tính giá trị của x.
Gọi x là số mol Na2CO3
y là số mol NaHCO3
Ta có PT:
CO2 + 2NaOH ---> Na2CO3 + H2O
..x...........2x.................x.............x
CO2 + NaOH ---> NaHCO3
..y...........y...................y
n\(CO_2\)=\(\frac{8,96}{22,4}\)=0,4(mol)
⇔x + y = 0,4 (1)
mct = m\(Na_2CO_3\) + m\(NaHCO_3\)
= 104x + 84y = 36,9 (2)
Giải (1) và (2) ta có:
x = 0,15
y = 0,25
nNaOH = 2x + y = 0,55(mol)
CM NaOH = \(\frac{0,55}{0,5}\)= 1,1M
=> x=1,1
Đúng 0
Bình luận (0)
Hấp thụ hoàn toàn 1,568 (l) khí CO2 (đktc) vào 500 ml dung dịch NaOH 0,16M thu được dung dịch X.Thêm 250 ml dung dịch Y gồm BaCl2 0,16M và Ba(OH)2 a M vào dung dịch X thu được 3,94 g kết tủa và dung dịch Z. Tìm giá trị a thoả mãn đề bài.
nNaOH= 0,08 mol; nCO2= 0,07 mol; nBaCl2= 0,04mol; nba(OH)2= 0,25a mol; nBaCO3= 0,02 mol
*Thí nghiệm 1: Phản ứng của CO2 với NaOH
nOH- : nCO2= 0,08 : 0,07 = 1,14 nên tạo 2 muối là NaHCO3 và Na2CO3
CO2 + NaOH → NaHCO3
CO2+ 2NaOH → Na2CO3+ H2O
Đặt nNaHCO3=x mol; nNa2CO3= y mol
→ x+y= 0,07; x+ 2y= 0,08 → x= 0,06; y= 0,01
*Thí nghiệm 2: Phản ứng của X với dung dịch Y chứa Ba(OH)2 và BaCl2
Ta thấy nCO2= 0,07 > nBaCO3= 0,02 mol < nBa(ddY)= (0,04 + 0,25a)
Chứng tỏ sau phản ứng còn dư các chất tan của Ba và muối -HCO3
Do đó trong Z không có NaOH hoặc Ba(OH)2 hoặc Na2CO3
(Chú ý: các chất kể trên tác dụng được với muối -HCO3 hoặc hợp chất tan của kim loại Ba, nên chúng không thể tồn tại trong dung dịch Z)
Coi như chỉ xảy ra các phản ứng:
Ba(OH)2 + 2 NaHCO3 → BaCO3 + Na2CO3 + 2H2O
0,25a 0,5a 0,25a 0,25a
BaCl2 + Na2CO3 → BaCO3+ 2NaCl
(0,25a + 0,01)→ (0,25a + 0,01) mol
Ta có: nBaCO3= 0,25a + 0,25a + 0,01 = 0,02 mol → a = 0,02M
*TK
Đúng 1
Bình luận (0)
Dung dịch X có chứa a mol Na2CO3 và b mol NaHCO3. Nhỏ từ từ 0,15 mol dung dịch HCl vào dung dịch X thì sau phản ứng thu được dung dịch Y và thoát ra 0,045 mol khí. Nhỏ tiếp dung dịch nước vôi trong dư vào dung dịch Y thì thu được 15 g kết tủa. Tính giá trị của a và b
CO32- + H+ = HCO3-
a-------a----------a
H+ + HCO3- = CO2 + H2O
0.045--0.045----0.045
=> a = 0.15 - 0.045 = 0.105
nCaCO3 = 0.15
HCO3- + OH- = CO32- + H2O
0.15--------0.15---0.15
0.15 = 0.105 - 0.045 +b
=b = 0.09
Đúng 0
Bình luận (0)
Sục V (l) CO2 (đktc) vào 200 ml dung dịch hỗn hợp KOH 0,5M và Ba(OH)2 0,375M thu được 11,82 g kết tủa. Tính giá trị của V
nKOH = 0,2.0,5 = 0,1 (mol)
nBa(OH)2 = 0,2.0,375 = 0,075 (mol) => nBa2+ = 0,075 (mol)
Tổng mol OH- = nKOH + 2nBa(OH)2 = 0,25 (mol)
nBaCO3 = 11,82 : 197 = 0,06 (mol)
Ta thấy nBaCO3 < nBa2+ nên có thể xảy ra 2 TH sau:
TH1: Hấp thụ CO2 vào chỉ tạo muối CO32- => CO2 pư hết, OH- hết hoặc dư. Mọi tính toán theo số mol sản phẩm.
PT ion: CO2 + 2OH- ---> CO32- + H2O (1)
Ba2+ + CO32- ---> BaCO3↓ (2)
BTNT "C": nCO2 = nBaCO3 = 0,06 (mol)
=> VCO2(đktc) = 0,06.22,4 = 1,344 (lít)
TH2: Hấp thụ CO2 vào tạo cả muối CO32- và HCO3-. Cả CO2 và OH- đều phản ứng hết
nCO32- = nBaCO3 = 0,06 (mol)
CO2 + 2OH- ---> CO32- + H2O (3)
0,06<-- 0,12 <---- 0,06 (mol)
CO2 + OH- ---> HCO3- (4)
0,13<--(0,25-0,12) --> 0,13
có: nOH- (3) = nCO32- = 0,06 (mol)
=> nOH- (4) = Tổng mol OH- bđ - nOH- (3) = 0,25 - 0,12 = 0,13 (mol)
=> Tổng mol CO2 pư (3) +(4) = 0,06 + 0,13 = 0,19 (mol)
=> VCO2(đktc) = 0,19.22,4 = 4,256 (lít)
*Tk
Đúng 0
Bình luận (0)