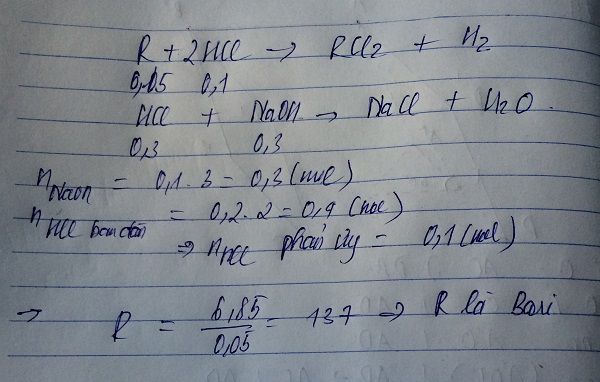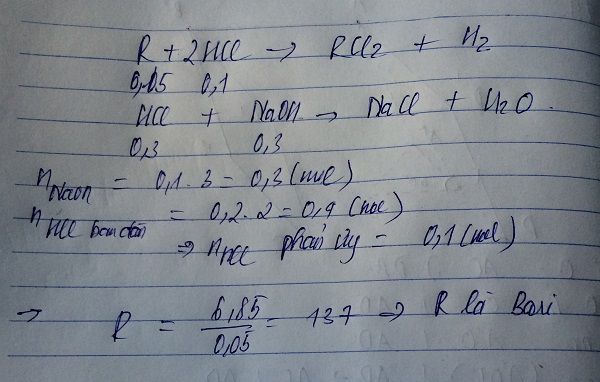hòa tan hoàn toàn 6,85 (g) 1 kim loại htri II R bằng 200(ml) dung dịch HCl 2M. Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M . Xđ kim loại trên

Những câu hỏi liên quan
hòa tan hoàn toàn một kim loại kiềm thổ R vào 200ml dung dịch HCl 2M.Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M xác định tên kim loại đó.....trân thành cẳm ơn
Đề thiếu m
NaOH + HCl = NaCl + H2O
0,3 - - - - 0,3
=>số mol HCl pư là 0,1 mol
=>số mol OH- = số mol H+ = số mol HCl = 0,1 mol
=>số mol kiềm thổ là 0,05 mol
=>R = 6,85 / 0,05 = 137 => Ba
Đúng 0
Bình luận (0)
hòa tan hoàn toàn một kim loại kiềm thổ R vào 200ml dung dịch HCl 2M.Để trung hòa lượng axit dư cần 100ml dung dịch NaOH 3M xác định tên kim loại đó.....trân thành cẳm ơn
<a href="http://tchiase.info/office-2016-tai-office-2016-professional-plus-full-crack/">tải office 2016</a>
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 1,44 gam kim loại hóa trị II trong 200 ml dung dịch H2SO4 0,5M. Để trung hòa lượng axit dư phải dùng hết 80 ml dung dịch KOH 1M. Kim loại cần tìm là
A. Magie
B. Canxi
C. Bari
D. Beri
Hòa tan hoàn toàn 1,44 gam kim loại hóa trị II trong 200 mL dung dịch H2SO4 0,5M. Để trung hòa lượng axit dư phải dùng hết 80 mL dung dịch KOH 1M. Kim loại cần tìm là
A. Magie.
B. Canxi.
C. Bari.
D. Beri.
Hòa tan hoàn toàn 1,44 gam kim loại hóa trị II trong 200 mL dung dịch H2SO4 0,5M. Để trung hòa lượng axit dư phải dùng hết 80 mL dung dịch KOH 1M. Kim loại cần tìm là
A. Magie.
B. Canxi.
C. Bari.
D. Beri.
Đáp án A
M + H2SO4 → MSO4 + H2 (1)
2KOH + H2SO4 → K2SO4 + 2H2O (2)
![]()
Mà
![]()
![]()
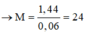
M là Magie
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8,4 gam kim loại R (hóa trị không đổi) vào 200 ml dung dịch HCl 2,5M. Để trung hòa lượng axit dư sau phản ứng phải dùng 80gam dung dịch NaOH 10%
a) Xác định kim loại R
b) Trộn 2,1 gam MgCO3 và 8,4 gam R trên rồi cho tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít hỗn hợp 2 khí (ở đktc) có tỉ khối so với H2 bằng 31. Xác định V
Cho 11,7 gam một kim loại X hóa trị II vào 350 ml dung dịch HCl 1M, khi phản ứng kết thúc ta thấy kim loại vẫn còn dư. Mặt khác để hòa tan hoàn toàn lượng kim loại trên phải cần chưa đến 200 ml dung dịch HCl 2M. Tìm X.
nHCl = 0,35 . 1 = 0,35 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,175 0,35 0,175 0,175 (mol)
nHCl (pứ 2 ) = 0,2 . 2 = 0,4 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,2 0,4
\(nX=0,175+0,2=0,375\left(mol\right)\)
=> \(MX=\dfrac{11,7}{0,375}=\) 31,2 .-. k ra là s
Đúng 3
Bình luận (0)
hòa tan hoàn toàn 6,85 g một kim loại kiềm thổ R bằng 200ml dung dịch HCl 2M . để trung hòa lượng ã dư cần 100 ml dung dịch NaOH 3M . xác định tên kim loại trên
Gọi KL là M
PTHH: M+ 2HCl----->MCl2 +H2(1)
HCl+NaOH---->NaCl +H2O(2)
Ta có
n\(_{NaOH}=0,1.3=0,3\left(mol\right)\)
Theo pthh2
n\(_{HCl}=n_{NaOH}=0,3\left(mol\right)\)
Mặt khác
n\(_{HCl}=0,2.2=0,4\left(mol\right)\)
=>n\(_{HCl}pư1=0,4-0,3=0,1\left(mol\right)\)
Theo pthh1
n\(_M=\frac{1}{2}n_{HCl}=0,05\left(mol\right)\)
M\(_M=\frac{6,85}{0,05}=137\)
=> M là Bari...Kí hiệu K
Đúng 0
Bình luận (1)
Hòa tan 1,3g một kim loại R trong 100ml dung dịch H2SO4 0,3M. Để trung hòa lượng axit dư cần 200ml dung dịch NaOH 0,1M. Xác định kim loại R?
\(n_{NaOH} =0,2.0,1 = 0,02(mol)\\ 2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O\\ n_{H_2SO_4\ dư} = \dfrac{1}{2}n_{NaOH} = 0,01(mol)\\ \Rightarrow n_{H_2SO_4\ pư} = 0,1.0,3 - 0,01 = 0,02(mol)\)
Gọi n là hóa trị của kim loại R
\(2R + nH_2SO_4\to R_2(SO_4)_3 + nH_2\\ n_R = \dfrac{2}{n}n_{H_2SO_4} = \dfrac{0,04}{n}(mol)\\ \Rightarrow \dfrac{0,04}{n}.R = 1,3\\ \Rightarrow R = \dfrac{65}{2}n\)
Với n = 2 thì R = 65(Zn)
Đúng 1
Bình luận (1)