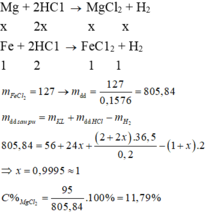Cho x g MgCl2 vào 150 g dd MgCl2 40% được dd mới có nồng độ 60% Tính giá trị của x .

Những câu hỏi liên quan
1,Thêm 200 g nước vào dd chứa 50 g mgcl2 thì thấy nồng độ của dd thu được là 6%. Xác định nồng độ phần trăm của dd mgcl2 ban đầu.
cho 2,3 g kim loai na vào dd h2so4 4,9% thu đc v lít khí h2(đktc) và dd x. lần lượt cho vào dung dịch X 60 g ba(oh)2 14,25% và 30g dd mgcl2 19% thu đc dd y và kết tủa a. lọc a nung trong không khí đến m k đổi thu được m gam chất rắn.a) tính m? b) tính nồng độ phần trăm của dung dịch y
PTHH: \(2Na+H_2SO_4\rightarrow Na_2SO_4+H_2\uparrow\) (1)
\(Na_2SO_4+Ba\left(OH\right)_2\rightarrow2NaOH+BaSO_4\downarrow\) (2)
\(2NaOH+MgCl_2\rightarrow2NaCl+Mg\left(OH\right)_2\downarrow\) (3)
\(Mg\left(OH\right)_2\xrightarrow[]{t^o}MgO+H_2O\) (4)
Ta có: \(\left\{{}\begin{matrix}n_{Na_2SO_4}=\dfrac{1}{2}n_{Na}=\dfrac{1}{2}\cdot\dfrac{2,3}{23}=0,05\left(mol\right)\\n_{BaCl_2}=\dfrac{60\cdot14,25\%}{208}=0,05\left(mol\right)\\n_{MgCl_2}=\dfrac{30\cdot19\%}{95}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) PT (2) p/ứ hết; PT (3) có MgCl2 dư 0,01 mol
\(\Rightarrow n_{MgO}=n_{Mg\left(OH\right)_2}=n_{BaSO_4}=0,05\left(mol\right)\)
\(\Rightarrow m_{rắn}=m_{MgO}+m_{BaSO_4}=0,05\cdot\left(40+233\right)=13,65\left(g\right)\)
b) Theo các PTHH: \(\left\{{}\begin{matrix}n_{NaCl}=n_{Na}=0,1\left(mol\right)\\n_{Mg\left(OH\right)_2}=0,05\left(mol\right)=n_{H_2SO_4}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{NaCl}=0,1\cdot58,5=5,85\left(g\right)\\m_{ddH_2SO_4}=\dfrac{0,05\cdot98}{4,9\%}=100\left(g\right)\\m_{Mg\left(OH\right)_2}=0,05\cdot58=2,9\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{Na}+m_{ddH_2SO_4}+m_{ddBaCl_2}+m_{ddMgCl_2}-m_{BaSO_4}-m_{Mg\left(OH\right)_2}=177,75\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{NaCl}=\dfrac{5,85}{177,75}\cdot100\%\approx3,29\%\\C\%_{MgCl_2\left(dư\right)}=\dfrac{0,01\cdot95}{177,75}\cdot100\%\approx0,53\%\end{matrix}\right.\)
Đúng 1
Bình luận (1)
Hòa Tan hoàn toàn 7,2 g kim loại Mg vào 200 ml dd axit clohidric ( HCL ) sau phản ứng thu được magie clorua MgCl2 và khí hidro ( đktc )
a viết PTHH
b tính khối lượng magie clorua tạo thành
c tính nồng độ mol của dd axit đã dùng
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, \(m_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Theo PT: \(n_{MgCl_2}=n_{Mg}=0,3\left(mol\right)\Rightarrow m_{MgCl_2}=0,3.95=28,5\left(g\right)\)
c, \(n_{HCl}=2n_{Mg}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,2}=3\left(M\right)\)
Đúng 2
Bình luận (0)
Cho 150 gam dd NaOH 20% vào 80 gam dung dịch MgCl2 59,375%. Sau phản ứng thu được kết tủa A và dd B. Xác định:
a) Khối lượng kết tủa A
b) Nồng độ % của các chất trong dd B
\(\begin{cases} m_{NaOH}=\dfrac{150.20\%}{100\%}=30(g)\\ m_{MgCl_2}=\dfrac{80.59,375\%}{100\%}=47,5(g) \end{cases} \Rightarrow \begin{cases} n_{NaOH}=\dfrac{30}{40}=0,75(mol)\\ n_{MgCl_2}=\dfrac{47,5}{95}=0,5(mol) \end{cases}\\ PTHH:2NaOH+MgCl_2\to Mg(OH)_2\downarrow+2NaCl\\ \text {Vì }\dfrac{n_{NaOH}}{2}<\dfrac{n_{MgCl_2}}{1} \text {nên }MgCl_2 \text { dư}\\ a,n_{Mg(OH)_2}=\dfrac{1}{2}n_{NaOH}=0,375(mol)\\ \Rightarrow m_{Mg(OH)_2}=0,375.58=21,75(g)\\ b,n_{NaCl}=m_{NaOH}=0,75(mol)\\ \Rightarrow m_{CT_{NaCl}}=0,75.58,5=43,875(g)\\ m_{dd_{NaCl}}=150+80-21,75=208,25(g)\\ \Rightarrow C\%_{NaCl}=\dfrac{43,875}{208,25}.100\%\approx 21,07\%\)
Đúng 2
Bình luận (0)
1, Cho 100g đe K2CO3 13,8% tác dụng với 120 g đe MgCl2 9,5% thu được m g kết tủa và dd A
a, XĐinh giá trị của m
b, Xđịnh nồng độ % mỗi chất trong A
2, Cho 6,72 g kim loại X tác dụng Cl2 dư sau phản ứng thu được 33,375 g muối
a, xđịnh tên kim loại
b, viết pt pứ X lần lượt với O2, dd H2SO4 l, dd CuSO4,NaOH, Na2SO4, MgSO4 ( nếu có )
bài 1
\(n_{K_2CO_3}=\dfrac{100.13,8\%}{138.100\%}=0,1\left(mol\right)\)
\(n_{MgCl_2}=\dfrac{120.9,5\%}{95.100\%}=0,12\left(mol\right)\)
\(K_2CO_3+MgCl_2-->MgCO_3\downarrow+2KCl\)
\(\dfrac{0,1}{1}< \dfrac{0,12}{1}\Rightarrow\) K2CO3 hết MgCl2 dư
\(m_{MgCO_3}=0,1.84=8,4\left(g\right)\)
dd A :KCl và MgCl2 dư
\(m_{dd}=100+120-8,4=211,6\left(g\right)\)
\(C\%KCl=\dfrac{0,2.74,5}{211,6}.100\%\approx7,04\%\)
\(C\%MgCl_{2dư}=\dfrac{\left(0,12-0,1\right).95}{211,6}.100\%\approx0,9\%\)
Đúng 0
Bình luận (0)
bài 2
a) \(2X+nCl_2-->2XCl_n\)
a.......................................a
\(aX=6,72\left(1\right)\)
\(a\left(X+35,5n\right)=33,375\left(2\right)\)
\(\dfrac{\left(1\right)}{\left(2\right)}=\dfrac{aX}{a\left(X+35,5n\right)}=\dfrac{X}{X+35,5n}=\dfrac{6,72}{33,375}\)
\(\Rightarrow7,14n=0,78X\)
nếu n=1=>X=9,15(loại)
nếu n=2=>X=18,3(loại
nếu n=3=>X=27(chọn)
=> X là Al
b)
\(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\)
\(2Al+3CuSO_4-->Al_2\left(SO_4\right)_3+3Cu\)
\(2Al+2NaOH+2H_2O-->2NaAlO_2+3H_2\uparrow\)
Đúng 0
Bình luận (0)
Cho 4.8 gam Mg tác dụng vừa đủ với dd HCl 10% thu đc muối MgCl2 và H2
a) tính thể tích khis thu đc ở đktc
b) khối lương của dd HCl đã dùng
c) tính nồng độ % của dd muối thu đc. Cho Mg 24, H:1, Cl:35,5
2) cho 7,8g Kali vào 100g nước . Tính nồng độ % của dd thu đc ( cho k:39, H:1, O:16)
Giúp ah mik Cần trước 10h
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH :
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
0,2 0,4 0,2 0,2
\(a,V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(b,m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(m_{ddHCl}=\dfrac{14,6.100}{10}=146\left(g\right)\)
\(c,m_{MgCl_2}=0,2.95=19\left(g\right)\)
\(m_{ddMgCl_2}=4,8+146-\left(0,2.2\right)=150,4\left(g\right)\)
\(C\%_{MgCl_2}=\dfrac{19}{150,4}.100\%\approx12,63\%\)
2.
\(n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\uparrow\)
0,2 0,2 0,1
\(m_{KOH}=0,2.56=11,2\left(g\right)\)
\(m_{ddKOH}=7,8+100-\left(0,1.2\right)=107,6\left(g\right)\)
\(C\%=\dfrac{11,2}{107,6}.100\%\approx10,4\%\)
Đúng 2
Bình luận (1)
Hoà tan hoàn toàn hh X gồm Fe và Mg bằng một lượng vừa đủ dd HCl 20%, thu đươc dd Y. Nồng độ của FeCl2 trong dd Y là 15,76%. Nồng độ phần trăm của MgCl2 trong dd Y là
A. 24,24%.
B. 11,79%.
C. 28,21%.
D. 15,76%.
Cho4.8g Mg tacs dungj vs 200g HCL. Thu đc muối MGCL2 và h2
a. tính Thể tích khí H2 thu được (đktc)
b. Tính nồng độ mol của dd HCl cần dùng
c. Tính khối lượng MgCl2 thu được.
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) \(n_{H2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
Câu b : hình như đề bị sai bạn xem lại giúp mình
c) \(n_{MgCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{MgCl2}=0,2.95=19\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
n\(_{H2}\)=\(\dfrac{4,8}{24}=0,2\left(mol\right)\)
Mg + 2HCl \(\rightarrow\)MgCl2 + H2
0,2 \(\rightarrow\) 0,4 \(\rightarrow\) 0,2 \(\rightarrow\) 0,2
a) VH2 = 0,2 . 22,4
=4,48 (l )
c) mMgCl2 = n.M = 0,2.95 = 19 (g)
Đúng 1
Bình luận (0)
Cho 4.8 gam kim loại magie vào 200ml dd axit clohiric (hcl) sau phản ứng thu được magie clorua(MgCl2) và khí hidro a) tính thể tích khí video thu được ở đktc b) tính nồng độ mol dd HCL? c) nếu trung hòa dd HCL trên bằng dd KOH 5.6% (D= 1.045g/ml).Tính thể tích dd KOH cần dùng
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
a, \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,4}{0,2}=2\left(M\right)\)
c, PT: \(HCl+KOH\rightarrow KCl+H_2O\)
Theo PT: \(n_{KOH}=n_{HCl}=0,4\left(mol\right)\)
\(\Rightarrow m_{ddKOH}=\dfrac{0,4.56}{5,6\%}=400\left(g\right)\)
\(\Rightarrow V_{ddKOH}=\dfrac{400}{1,045}\approx382,78\left(ml\right)\)
Đúng 2
Bình luận (0)